- Indan
-
Strukturformel 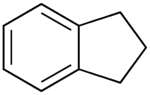
Allgemeines Name Indan Andere Namen - Hydrinden
- 1H-Benzol-2,3-cyclopenten
- 1H-Benzolpentaninden
- Cyclopentenbenzol
- 2,3-Dihydroinden
Summenformel C9H10 CAS-Nummer 496-11-7 PubChem 10326 Kurzbeschreibung farblose Flüssigkeit[1]
Eigenschaften Molare Masse 118,18 g·mol−1 Aggregatzustand flüssig
Dichte 0,97 g·cm–3[1]
Schmelzpunkt Siedepunkt 178 °C[2]
Löslichkeit praktisch unlöslich in Wasser[1], leicht löslich in Ethanol und Diethylether[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 

Gefahr
H- und P-Sätze H: 226-304 EUH: keine EUH-Sätze P: 301+310-331 [3] EU-Gefahrstoffkennzeichnung [1] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 10-65 S: 23-24/25-62 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Indan ist eine chemische Verbindung aus der Gruppe der bizyklischen aromatischen Kohlenwasserstoffe.
Inhaltsverzeichnis
Gewinnung und Darstellung
Indan kommt verbreitet im Steinkohlenteer, im Urteer und als Strukturelement in Indenharz vor. Es kann aus Inden durch eine katalytische Hydrierung über Platin-Katalysatoren mittels Wasserstoff oder durch Reduktion mit metallischen Natrium in Ethanol hergestellt werden.[2][4]
Eigenschaften
Indan ist eine farblose Flüssigkeit mit aromatischem Geruch, die bei Normaldruck bei 178 °C siedet. Die Verdampfungswärme beträgt 49,2 kJ·mol-1.[5] Der Feststoff kann in zwei polymorphen Kristallformen vorliegen. Die Umwandlungstemperatur der Form II zu Form I liegt bei −199 °C.[6] Form I schmilzt bei −51 °C.[6]. Die Schmelzwärme beträgt 8,6 kJ·mol-1, die Umwandlungswärme von Form II zu Form I 0,8 kJ·mol-1.[6]
Zusammenstellung der wichtigsten thermodynamischen Eigenschaften Eigenschaft Typ Wert [Einheit] Bemerkungen Standardbildungsenthalpie ΔfH0liquid −11,7 kJ·mol−1[5] Standardentropie S0liquid 234,35 J·mol−1·K−1[6] als Flüssigkeit Verbrennungsenthalpie ΔcH0liquid −4982.5 kJ·mol−1[7] Wärmekapazität cp 190,25 J·mol−1·K−1 (25 °C)[6]
130,7 J·mol−1·K−1 (25 °C)[8]als Flüssigkeit
als GasTripelpunkt Ttriple 221,77 K [9] Kritische Temperatur Tc 684,9 K [10] Kritischer Druck pc 39,5 bar [10] Die Temperaturabhängigkeit der Verdampfungsenthalpie lässt sich entsprechend der Gleichung ΔVH0=A·exp(−β·Tr)(1−Tr)β (ΔVH0 in kJ/mol, Tr =(T/Tc) reduzierte Temperatur) mit A = 65,1 kJ/mol, β = 0,2866 und Tc = 684,9 K im Temperaturbereich zwischen 302 K und 339 K beschreiben.[11]
Verwendung
Indan kann durch Dehydrierung in Inden überführt werden. Derivate (Indane) finden vielfältige Anwendung als Antibiotika, Herztherapeutika, Insektizide und Duftstoffe (Moschus).[12] Ein bekanntes Derivat des Indans ist Ninhydrin.
Verwandte Verbindungen
Weblinks
Einzelnachweise
- ↑ a b c d e Eintrag zu Indan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 14. November 2009 (JavaScript erforderlich).
- ↑ a b c Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag Leipzig 1965, Seite 561.
- ↑ a b Datenblatt Indan bei Sigma-Aldrich, abgerufen am 5. April 2011.
- ↑ S. Hauptmann, J. Graefe, H. Remane: Lehrbuch der organischen Chemie, Deutscher Verlag für Grundstoffindustrie Leipzig 1980, S. 263.
- ↑ a b Roux, M.V.; Temprado, M.; Chickos, J.S.; Nagano, Y.: Critically Evaluated Thermochemical Properties of Polycyclic Aromatic Hydrocarbons in J. Phys. Chem. Ref. Data 37 (2008) 1855-1996,doi:10.1063/1.2955570.
- ↑ a b c d e Stull, D.R.; Sinke, G.C.; McDonald, R.A.; Hatton, W.E.; Hildenbrand, D.L.: Thermodynamic properties of indane and indene in Pure Appl. Chem. 2 (1961) 315-322,doi:10.1351/pac196102010315.
- ↑ Good, W.D.: The enthalpies of combustion and formation of indan and seven alkylindans in J. Chem. Thermodyn. 3 (1971) 711-717,doi:10.1016/S0021-9614(71)80095-2.
- ↑ Dorofeeva O.V.: Thermodynamic Properties of Gaseous Polycyclic Aromatic Hydrocarbons Containing Five-Membered Rings in Institute for High Temperatures, USSR Academy of Sciences, Preprint No.1-263 (in Russian), Moscow, 1989.
- ↑ Stull, D.R.; Sinke, G.C.; McDonald, R.A.; Hatton, W.E.; Hildenbrand, D.L.: Thermodynamic properties of indane and indene in Symposium uber Thermodynamik, 1959, 1-9.
- ↑ a b Tsonopoulos, C.; Ambrose, D.: Vapor-Liquid Critical Properties of Elements and Compounds. 3. Aromatic Hydrocarbons in J. Chem. Eng. Data 40 (1995) 547-558, doi:10.1021/je00019a002.
- ↑ Majer, V.; Svoboda, V.: Enthalpies of Vaporization of Organic Compounds: A Critical Review and Data Compilation, Blackwell Scientific Publications, Oxford, 1985, 300.
- ↑ Römpp CD 2006, Georg Thieme Verlag 2006.
Wikimedia Foundation.
