- Polymer
-
Ein Polymer [polyˈmeːr] (griech. πολύ poly „viel“; μέρος méros „Teil“) ist eine chemische Verbindung aus Ketten- oder verzweigten Molekülen (Makromolekülen), die wiederum aus gleichen oder gleichartigen Einheiten, den sogenannten Monomeren, bestehen. Das Adjektiv polymer bedeutet entsprechend „aus vielen gleichen Teilen aufgebaut“. Synthetische Polymere sind in der Regel Kunststoffe.
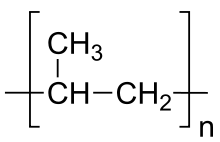 Die sich wiederholende Einheit des Polymers Polypropylen
Die sich wiederholende Einheit des Polymers Polypropylen
Inhaltsverzeichnis
Alternative Definition
„[Polymere sind] Stoffe, deren Molekulargewichte bei gleicher prozentualer atomarer Zusammensetzung in einem ganzzahligen Verhältnis zueinander stehen und auch gleichen inneren Aufbau aufweisen. Dabei ist die gleiche innere Struktur über das ganze Makromolekül verteilt. Weiter umfasst die Definition eines Polymers die Eigenschaft, dass ein Polymermolekül aus n Einheiten sich nicht von einem Polymermolekül aus n-1- oder n+1-Grundbausteinen unterscheiden lässt.“
– Kunz[1]
Durch diese Definition werden auch anorganische Makromoleküle und anorganische Verbindungen der Form [— A- — B+ — A- — B+ —] erfasst. Solche anorganische Polymere werden von den Elementen Bor, Silicium (Silikone, Polysiloxane und Polysilazane), Aluminium, Titan, Germanium, Phosphor (Polyphosphazene), Arsen, Schwefel oder Sauerstoff gebildet.
Einteilung
Polymere können nach der Anzahl der Grundmonomere eingeteilt werden. Wichtig ist jedoch, dass mindestens eine monomere Substanz die Kette aufbaut.
- Homopolymer: das Polymer besteht nur aus einer Monomerart wie bei Polyethylen, Polypropylen, Polyvinylchlorid oder Polyamid PA6.
- Copolymere sind aus verschiedenen Monomeren aufgebaut wie Polyester, Polyurethane und auch einige Polyamide (PA 66).
- Polymerlegierungen entstehen durch Mischen von unterschiedlichen Polymeren und Copolymeren.
Außerdem unterscheidet man organische und anorganische Polymere. Die organischen Polymere lassen sich weiter unterteilen in
- Biopolymere oder „natürliche“ Polymere: die Grundbausteine der lebenden Organismen.
- chemisch modifizierte Polymere entstehen durch die Weiterverarbeitung von Biopolymeren, beispielsweise Nitrocellulose, Celluloid oder Stärkederivate
- synthetische Polymere sind die durch Polymerisationsverfahren industriell oder im Labormaßstab hergestellten, dazu gehören Polyethylen, Polystyrol, Polyvinylchlorid.
Mischungen mehrerer Polymere werden als Polymerblends bezeichnet. Diese sind als makroskopisch homogene Mischung von zwei oder mehr verschiedenen Polymeren definiert.[2] Hergestellt werden sie meist durch intensive mechanische Vermischung von geschmolzenen Polymeren, wobei sich ein homogenes Material ergibt. Beim Abkühlen der Schmelze bleiben die Polymerketten fein verteilt und sorgen so dafür, dass das Eigenschaftsprofil des Blends eine auf Dauer erhalten bleibende Überlagerung der Eigenschaften der einzelnen Polymere ist.[3]
Ein abweichende Einteilung führt zur Gruppe der Geopolymere.
Polymerphysik
Die Einteilung der Polymerwerkstoffe erfolgt nach DIN 7724 aufgrund des Temperaturverlaufes des Schubmoduls und des Zugverformungsrestes bei Raumtemperatur. Sie beruht auf dem mechanischen Verhalten im Gebrauchstemperaturbereich und der Existenz eines Schmelzbereiches (Fließbereiches):
Außerdem unterscheidet man noch zwischen teilkristallinen und amorphen Polymeren. Diese Eigenschaften werden maßgeblich durch den Verzweigungsgrad beeinflusst. Der strukturelle Aufbau der teilkristallinen Polymere wird im Artikel Kristallisation (Polymer) beschrieben. Amorphe Polymere und Schmelzen werden theoretisch beschrieben durch das Freely-Jointed-Chain-Modell oder das Wormlike-Chain-Modell.
In der Polymerphysik beschäftigt man sich unter anderem mit
- der Rheologie, also dem Fließverhalten und der Viskosität,
- der Kristallisation und Kristallisationskinetik,
- Oberflächeneigenschaften von Polymeren.
Polymerchemie
Die Kettenbildung, also die Verbindung einzelner Monomere untereinander zu Polymeren erfolgt durch verschiedene Arten von Polyreaktionen wie Polymerisation, Polykondensation oder Polyaddition. Polymere aus unterschiedlich gebauten Monomeren nennt man Heteropolymere oder Copolymere. Bei den meisten Kunststoffen wird das Polymerrückgrat aus Kohlenstoffketten gebildet.
Man unterscheidet isotaktische Polymere, bei denen alle Substituenten einer Polymerkette die gleiche stereoelektronische Konformation haben, wie isotaktisches Polystyrol mit der Konfiguration R-R-R-R-R-… oder S-S-S-S-S-… Bei ataktischen Polymeren sind die Substituenten wahllos geordnet, als eine Art Racemat. Als syndiotaktisch bezeichnet man Polymere, deren Substituenten abwechselnd aus R und S bestehen.
- Beispiele und Kurzwort
- Synthetische Polymere auf Kohlenstoffbasis:
- Polyethylen – PE
- Polypropylen – PP
- Polyvinylchlorid – PVC
- Polystyrol (PS), besser bekannt in geschäumtem Zustand als Styropor® (BASF AG)
- Polytetrafluorethylen (PTFE), Handelsname ist Tefal oder Teflon® (E. l. Du Pont de Nemours and Company)
- Polymethylmethacrylat (PMMA), unter dem Handelsnamen Plexiglas® (Evonik Industries AG)
- Die Gruppe der Polyamide, als PA66 unter dem Handelsnamen Nylon®, als PA6 unter dem Handelsnamen Perlon® oder als PA12G unter dem Handelsnamen Lauramid®
- Polyester, zu dieser Produktgruppe gehören auch
- Polycarbonate (PC) mit Handelsnamen Lexan oder Makrolon® (Bayer AG) und
- Polyethylenterephthalat (PET)
- Polyethylenglykol (PEG)
- Dendrimere sind stark verzweigte Strukturen mit Selbstähnlichkeit
- Synthetische Polymere auf anderer Basis:
- Silikone, genauer Poly(organo)siloxane
- Biopolymere:
Ökologische Erwägungen
Gesundheitsrisiken gehen vom Polymer selbst praktisch nie aus. Das Beispiel dafür ist PVC, das erst bei der Verbrennung das giftige und stark ätzende Gas Chlorwasserstoff freisetzt, das sich in Wasser als Salzsäure löst. Bei Schwelbränden entstehen in größeren Mengen polychlorierte Dibenzodioxine und -furane. Das Polymer PVC selbst ist lebensmittelkompatibel und wird auf Grund seiner ausgezeichneten Gasdichtigkeit in der Medizin zum Beispiel für Blutkonserven verwendet.
Weitere Umweltprobleme können durch Zusatzstoffe entstehen, die praktisch in jedem Kunststoffgegenstand enthalten sind, z.B. Weichmacher. Diese Zusatzstoffe werden überwiegend bei PVC eingesetzt, um seine mechanischen Eigenschaften dem Einsatz anzupassen. Dabei können sich durch die massenhafte Anwendung von PVC auch die Weiterentwicklungen als zweifelhaft erweisen. Für das Weich-PVC „Igelit“ wurde in den 1940er Jahren Trikresylphosphat eingesetzt. Der Ersatz dieser Substanz durch Phthalate, anfangs Dibutylphthalat (DPB), später Dioktylphthalat (DOP), führte in neuerer Zeit zur Erkenntnis, dass auch diese unter dem Umweltaspekt durch ihre mengenmäßige Anwesenheit erhebliche Probleme mit sich bringen.
Temperaturbeständige Polymere
Die Temperaturbeständigkeit hängt von der Struktur der verwendeten Monomere, der Stabilität der Bindungen zwischen den Monomeren und den Wechselwirkungen der Polymerketten untereinander ab. Bei amorphen Polymeren sollten die Glastemperatur und bei teilkristallinen Polymeren die Glas- und Schmelztemperatur möglichst hoch sein. Zum Erreichen der Temperaturbeständigkeit müssen C-H-Bindungen und C-C-Bindungen durch Bindungen zwischen Kohlenstoff und Heteroatomen wie Fluor, Stickstoff oder Sauerstoff bzw. durch stabilere aromatische Bindungen ersetzt werden. Die Temperaturbeständigkeit kann bei diesen Polymeren bis zu mehreren hundert °C betragen.
Beispiele sind:- Fluorpolymere wie Polytetrafluorethylen (PTFE), auch als Teflon bekannt, oder Perfluoralkoxylalkan (PFA) mit einer Temperaturbeständigkeit bis 290 °C.
- Polyaryle, bei denen aromatische Ringe über Sauerstoff- oder Schwefelatome bzw. CO- oder SO2-Gruppen verknüpft sind. Hierzu gehören Polyphenylensulfide, Polyethersulfone und Polyetherketone.
- Aromatische Polyester (Polyarylate) und Polyamide (Polyaramide) wie Poly-m-phenylenisophthalamid (PMI).
- Heterocyclische Polymere wie Polyimide, Polybenzimidazole und Polyetherimid, siehe hierzu auch Kunststoffe für Hochtemperaturanwendungen
Leitfähige Polymere und Polymerelektronik
Eine Voraussetzung für die elektrische Leitfähigkeit von Polymeren ist das Vorhandensein von konjugierten Pi-Elektronensystemen. Allerdings sind solche Polymere zunächst immer noch Isolatoren, bestenfalls Halbleiter. Die Leitfähigkeit, vergleichbar mit der von metallischen Leitern, setzt erst dann ein, wenn die Polymere oxidativ oder reduktiv dotiert werden. Die ersten Untersuchungen hierzu erfolgten am Polyacetylen, dessen Leitfähigkeit über die Dotierung mit Arsenpentafluorid oder Iod erreicht wurde. Außerdem steigt die Leitfähigkeit mit zunehmender Kristallinität des Polymers. Weitere Beispiele für leitfähige Polymere sind dotiertes Polypyrrol, Polyphenylensulfid, Polythiophen sowie metallorganische Komplexe mit makrocyclischen Liganden wie Phthalocyanin. Eine oxidative Dotierung erreicht man mit Arsenpentafluorid, Titantetrachlorid, Brom oder Iod, eine reduktive Dotierung dagegen mit Natrium-Kalium-Legierungen oder Dilithiumbenzophenonat. Beim Dotieren entstehen Ladungen auf den Polymerketten, die durch die π-Konjugation über die Ketten delokalisiert sind. Die Erklärung für die Leitfähigkeit von Polymeren ist allerdings sehr komplex. So hat man versucht, den Ladungstransport entlang einer Polyenkette mit dem Soliton-Konzept bzw. mit dem Modell der Bipolaronen (auf einem kleinen Raum zusammengehaltene Ladungspaare) zu beschreiben.
Leitende, also elektrisch aktive Polymere werden zum Aufbau von polytronischen Anwendungen verwendet. Anders als in der Molekularelektronik wird die Information nicht in einzelnen Molekülen, sondern in verschieden dotierten Volumina verarbeitet.
Solche elektronischen Anwendungen sind:
- Funktionsschichten: UV-Filter
- Displays: OFETs, OLEDs
- RFID-Tags
- Solarzellen
- Sensoren und Aktoren
- Brennstoffzellen
- Akkus
- Elektrolytkondensatoren
Eine andere Anwendung ist die Verarbeitung von Polymeren mit Hilfe der Elektronik beim Elektrospinnen.
→ Siehe auch: Polymerelektronik
Supramolekulare Polymere
Ein relativ neuer Bereich der Polymerchemie umfasst supramolekulare Polymere, also Polymere, deren Bausteine nicht durch kovalente Bindungen, sondern durch vergleichsweise schwache intramolekulare Bindungen, wie etwa Wasserstoffbrückenbindungen, Ionenbindungen, Metall-Ligand-Wechselwirkungen, Van-der-Waals- oder hydrophobe Wechselwirkungen zusammengehalten werden.[4] Diese intramolekularen Bindungen können leicht zerbrochen werden (bei erhöhter Temperatur), können sich jedoch auch schnell wieder zurückbilden (beim Abkühlen). Aufgrund dieser Reversibilität zählen supramolekulare Polymere als neue Klasse selbstheilender Materialien.[5] Eine weitere Folge der schwachen intramolekularen Bindungen ist die geringe Viskosität von Schmelzen supramolekularer Polymere, was bei der Herstellung und Verarbeitung von Vorteil sein kann, aber auch bei bestimmten Anwendungen, wie dem Tintenstrahldrucken.
Während kovalent gebundene Polymere eine große Rolle in der Natur spielen (DNA, Polypeptide, Cellulose), sind relativ wenige natürlich vorkommende supramolekulare Polymere bekannt. Ein Beispiel supramolekularer Polymerisation in der Natur ist die Selbstassemblierung des Tabakmosaikvirus.
Literatur
- Manfred D. Lechner, Klaus Gehrke, Eckhard H. Nordmeier: Makromolekulare Chemie. Ein Lehrbuch für Chemiker, Physiker, Materialwissenschaftler und Verfahrenstechniker. 3. überarbeitete und erweiterte Auflage. Birkhäuser, Basel u. a. 2003, ISBN 3-7643-6952-3.
- J. Kahovec, R. B. Fox, K. Hatada: Nomenclature of regular single-strand organic polymers (IUPAC Recommendations 2002). In: Pure and Applied Chemistry. 74, 10, 2002, ISSN 0033-4545, S. 1921–1956, doi:10.1351/pac200274101921, online-Fassung.
- Ulf W. Gedde: Polymer Physics. Chapman & Hall, London u. a. 1995, ISBN 0-412-62640-3.
- H. Cherdron, F. Herold, A. Schneller: Technisch wichtige temperaturbeständige Polymere, Chemie in unserer Zeit, 23. Jahrg. 1989, Nr. 6, S. 181 – 192, ISSN 0009-2851.
- Klaus Menke, Siegmar Roth: Metallisch leitfähige Polymere I und II, Chemie in unserer Zeit, 20. Jahrg. 1986, Nr.1, S. 1-10, Nr. 2, S. 33-43, ISSN 0009-2851
Weblinks
 Commons: Polymere – Sammlung von Bildern, Videos und Audiodateien
Commons: Polymere – Sammlung von Bildern, Videos und Audiodateien Wiktionary: Polymer – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Wiktionary: Polymer – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen- VDMA-Polymerelektronik
- Chemischer Hintergrund
- Einführung und Ausblick in die Chemie der Polymere (engl.)
Einzelnachweis
- ↑ Kunz: Polymerisationstechnik. Skript, TU Clausthal, Version 2005, S. 11.
- ↑ IUPAC, Compendium of Chemical Terminology 2nd Edition, 1997
- ↑ Blends (Chemgapedia)
- ↑ T. F. A. de Greef, E. W. Meijer: Materials Science: Supramolecular Polymers. In: Nature. 453, S. 171–173.
- ↑ Materialforschung - Selbstheilung durch Licht orf.at abgerufen am 21. April 2011; Mark Burnworth, et al.:Optically healable supramolecular polymers. in: Nature, Volume 472,S.334–337,doi:10.1038/nature09963
Wikimedia Foundation.
