- Acebutolol
-
Strukturformel 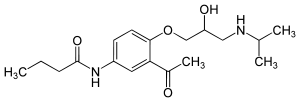
1:1-Gemisch von zwei Stereoisomeren Allgemeines Freiname Acebutolol Andere Namen - (±)-Acebutolol
- (RS)-Acebutolol
- DL-Acebutolol
- rac-Acebutolol
- (RS)-3-Acetyl-4-(2-hydroxy-3-
isopropylaminopropoxy)butyranilid - (±)-3-Acetyl-4-(2-hydroxy-3-
isopropylaminopropoxy)butyranilid - DL-3-Acetyl-4-(2-hydroxy-3-
isopropylaminopropoxy)butyranilid - rac-3-Acetyl-4-(2-hydroxy-3-
isopropylaminopropoxy)butyranilid
Summenformel C18H28N2O4 CAS-Nummer - 37517-30-9
- 34381-68-5 (Hydrochlorid)
PubChem 1978 ATC-Code C07AB04
DrugBank DB01193 Arzneistoffangaben Wirkstoffklasse Wirkmechanismus Blockade von β-Rezeptoren mit geringer β1-Selektivität und vorhandener intrinsischer Aktivität
Verschreibungspflichtig: Ja Eigenschaften Molare Masse 336,43 g·mol−1 Schmelzpunkt Sicherheitshinweise Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln GHS-Gefahrstoffkennzeichnung [2] 
Achtung
H- und P-Sätze H: 312-332 EUH: keine EUH-Sätze P: 280 [2] EU-Gefahrstoffkennzeichnung [2]
Xn
Gesundheits-
schädlichR- und S-Sätze R: 20/21/22 S: 36 LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Acebutolol ist eine organische chemische Verbindung, die zu den Aromaten und Amiden zählt. Die Substanz wird als Arzneistoff der Gruppe der Betablocker eingesetzt.
Inhaltsverzeichnis
Klinische Angaben
Acebutolol gehört zu der Gruppe der mittellangwirksamen Betablocker, mit einer Halbwertszeit von 4 bis 12 Stunden und einer Wirkdauer von bis zu 24 Stunden. Die Bioverfügbarkeit von Acebutolol beträgt 60 % und es weist eine geringe Selektivität für β1-Adrenozeptoren gegenüber anderen β-Adrenozeptoren auf. Es wird über die Niere ausgeschieden und sollte daher nicht bei Patienten mit Niereninsuffizienz gegeben werden.
Intrinsische sympathominetische Aktivität
Die Besonderheit von Acebutolol und einigen anderen Betablockern (Oxprenolol und Pindolol) besteht in der intrinsischen sympathomimetischen Aktivität (ISA).
Sonstige Informationen
Stereochemie
Acetolol hat ein chirales Zentrum, arzneilich verwendet wird das Racemat. Die beiden Enantiomere eines chiralen Arzneistoffes zeigen fast immer eine unterschiedliche Pharmakologie und Pharmakokinetik, was früher aus Unkenntnis über stereochemische Zusammenhänge oft ignoriert wurde.[4] Das aktive Stereoisomer (Eutomer) ist (S)-Form von Acebutolol.[5]
Literatur
- T. Karow / R. Lang-Roth Allgemeine und spezielle Pharmakologie und Toxikologie 2003 S.62 - S.66
- G. Herold Innere Medizin 2004
Einzelnachweise
- ↑ Thieme Chemistry (Hrsg.): Römpp Online. Version 3.1. Georg Thieme Verlag, Stuttgart 2007.
- ↑ a b c Datenblatt Acebutolol hydrochloride bei Sigma-Aldrich, abgerufen am 18. März 2011.
- ↑ Acebutolol bei ChemIDplus
- ↑ Ariëns, EJ. (1984): Stereochemistry, a basis for sophisticated nonsense in pharmacokinetics and clinical pharmacology. In: Eur J Clin Pharmacol. 26(2); 663–668; PMID 6092093.
- ↑ Joni Agustiana, Azlina Harun Kamaruddina, Subhash Bhatiaa: Single enantiomeric -blockers—The existing technologies, Process Biochemistry 45 (2010) 1587–1604.
Handelsnamen
Prent (D)
Acebutolol in Kombination mit Mefrusid: Sali-Prent (D), Acebutolol in Kombination mit Nifedipin: Tredalat (D)

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- ATC-C07
- Gesundheitsschädlicher Stoff
- Arzneistoff
- Betablocker
- Beta-Aminoalkohol
- Anilid
- Keton
- Phenolether
Wikimedia Foundation.
