- Lenalidomid
-
Strukturformel 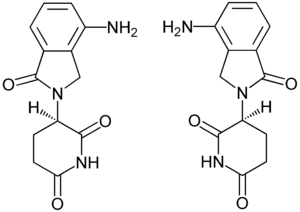
(R)-Form (links) und (S)-Form (rechts) Allgemeines Freiname Lenalidomid Andere Namen - IUPAC: (RS)-3-(7-Amino-3-oxo- 1H-isoindol-2-yl) piperidin-2,6-dion
- (±)-3-(7-Amino-3-oxo- 1H-isoindol-2-yl)piperidin-2,6-dion
- rac-3-(7-Amino-3-oxo-1H-isoindol- 2-yl)piperidin-2,6-dion
Summenformel C13H13N3O3 CAS-Nummer 191732-72-6 PubChem 216326 ATC-Code L04AX04
DrugBank DB00480 Kurzbeschreibung fast weißes bis blass-gelbes Pulver [1]
Arzneistoffangaben Wirkstoffklasse Verschreibungspflichtig: ja Eigenschaften Molare Masse 259,26 g·mol−1 Löslichkeit in organischen Lösungsmitteln besser löslich, zeigt jedoch die beste Löslichkeit in 0,1 N HCl-Pufferlösung [1]
Sicherheitshinweise Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln EU-Gefahrstoffkennzeichnung [2] Keine Einstufung verfügbarR- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Lenalidomid (Handelsname: Revlimid®, Hersteller: Celgene) ist ein Arzneistoff aus der Gruppe der Immunmodulatoren. Es ist strukturell mit dem Thalidomid verwandt und wird wie dieses zur Behandlung des Multiplen Myeloms eingesetzt. Lenalidomid wurde 2003 vom Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittelagentur als Arzneimittel für seltene Leiden (Orphan-Arzneimittel) ausgewiesen und als solches im Gemeinschaftsregister der Europäischen Union eingetragen.[3][4]
Lenalidomid ist in den USA, der Europäischen Union, der Schweiz, in Argentinien und Kanada für eine Kombinationstherapie mit Dexamethason bei Patienten mit einem multiplen Myelom zugelassen, die bereits eine Standardtherapie erhalten haben. Darüber hinaus ist Lenalidomid in Verbindung mit Dexamethason in Australien zur Behandlung von Patienten mit multiplem Myelom zugelassen, deren Krankheit sich nach einer Therapie verschlimmerte.[5][6] [7] [8] Lenalidomid ist in den USA, Kanada und Argentinien ebenfalls zugelassen für die Behandlung von transfusionsabhängigen Patienten mit einem Myelodysplastischen Syndrom der Risikoklasse „niedrig“ oder „intermediär-1“ (5q-minus-Syndrom) mit weiteren zytogenetischen oder ohne weitere zytogenetische Aberrationen.
In verschiedenen Studien wird zur Zeit überprüft, inwieweit Lenalidomid zur Erhaltungstherapie bzw. Therapie der Chronisch Lymphatischen Leukämie eingesetzt werden kann.[9]
Inhaltsverzeichnis
Wirkungsmechanismus
Lenalidomid gehört wie auch Thalidomid zu einer Gruppe peroral bioverfügbarer immunmodulierender Substanzen (engl. immunmodulatory drugs), die das Pharmaunternehmen Celgene unter der Marke IMiDs® eingetragen hat. Seine Wirkung beruht auf verschiedenen Mechanismen:
- Hemmung der Proliferation bestimmter hämatopoetischer Tumorzellen
- Hemmung der Produktion entzündungsfördernder (proinflammatorischer) Zytokine, insbesondere TNF-α und Interleukin-6 und -12
- Antiangiogenese
- Stimulation von T-Zellen und natürlichen Killerzellen (NK-Zellen) und in Folge Verbesserung der durch diese Zellen vermittelte Immunität gegen Tumorzellen
- Erhöhung der natürlichen Killer-T-Zellen (NKT-Zellen)
- Steigerung der Blutbildung (Erythropoese)
Sicherheitsvorkehrungen und Anwendungsbeschränkungen
Erste Zwischenergebnisse einer US-amerikanischen Studie an Primaten zeigen, dass Lenalidomid teratogen wirken kann.[10] Lenalidomid ist strukturverwandt mit Thalidomid, einer bekanntermaßen beim Menschen teratogen wirkenden Substanz, die schwere lebensbedrohende Geburtsschäden verursacht. Aufgrund dieser Tatsache hatte Celgene bereits im vergangenen Jahr vor der Einführung von Lenalidomid in den deutschen Markt zusammen mit den zuständigen Behörden und Patientenverbänden ein umfassendes Sicherheitsprogramm aufgestellt, das mit der Einleitung und Durchführung einer Lenalidomid-Behandlung verbunden ist und u.a. den Kontakt Schwangerer mit dem Wirkstoff verhindern soll.
Sicherheitsprogramm
Bei der Anwendung von Lenalidomid müssen wichtige Aspekte beachtet werden. Weil Lenalidomid vermutlich auch beim Menschen fruchtschädigend wirkt, gehört ein Schwangerschaftsverhütungsprogramm für gebärfähige Frauen und deren Partner sowie für Männer dazu. Eine mögliche Myelosuppression macht die wöchentlichen Blutbildkontrollen in den ersten acht Behandlungswochen erforderlich. Weiterhin zu beachten sind das erhöhte Risiko venöser Thromboembolien mit dem möglichen Einsatz einer antithrombotischen Prophylaxe und die Dosisreduktion bei Niereninsuffizienz. In Deutschland ist die Abgabe lenalidomidhaltiger Arzneimittel durch den § 3a Arzneimittelverschreibungsverordnung reguliert und unterliegt der amtlichen Überwachung, deshalb muss der Arzt für die Verordnung das so genannte T-Rezept verwenden. Der Arzt muss versichern, die Sicherheitsmaßnahmen gemäß der aktuellen Fachinformation einzuhalten, insbesondere auch, erforderlichenfalls ein Schwangerschafts-Präventionsprogramm durchzuführen. Ferner muss er auf der Verschreibung vermerken, ob die Behandlung innerhalb oder außerhalb (Off-Label-Use) der jeweils zugelassenen Anwendungsgebiete erfolgt.
Nebenwirkungen
Als häufigste Nebenwirkungen werden Abnahme der weißen Blutkörperchen (Neutropenie), der Blutplättchen (Thrombozytopenie) und der roten Blutkörperchen (Anämie), Müdigkeit, Kraftlosigkeit, Übelkeit, Verstopfung, Durchfall, Muskelkrämpfe, Schwellungen in Armen und Beinen und Hautausschlag beobachtet.
Chemische Eigenschaften
Lenalidomid ist chiral und kann daher in den optisch aktiven enantiomeren Formen (S)-(−) und (R)-(+) vorliegen, pharmazeutisch verwendet wird das Racemat [1:1-Gemisch von (S)-(−)-Form und (R)-(+)-Form]. Lenalidomid ist in 0,1 N Salzsäure-Pufferlösung gut löslich.
Einzelnachweise
- ↑ a b FDA Drug Details Revlimid® (Lenalidomide)
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Orphan Designation (EU/3/03/177) by the European Commission (englisch).
- ↑ Orphan Designation (EU/3/07/494) by the European Commission (englisch).
- ↑ Produktinformation der Europäischen Arzneimittelagentur (englisch).
- ↑ Europäische Arzneimittelagentur: Zusammenfassung des EPAR für die Öffentlichkeit (deutsch).
- ↑ Dimopoulos, Meletios et al.: Lenalidomide plus Dexamethasone for Relapsed or Refractory Multiple Myeloma. In: N Engl J Med. Nr. 357, 2007, S. 2123-2132 (Abstract).
- ↑ Weber, Donna M. et al.: Lenalidomide plus Dexamethasone for Relapsed Multiple Myeloma in North America. In: N Engl J Med. Nr. 357, 2007, S. 2133-2142 (Abstract).
- ↑ Studien Klinik I für Innere Medizin, Uniklinik Köln
- ↑ [1] Rote Hand Info von Celgene Juni 2008.
Handelsnamen
Revlimid (EU, CH, USA)

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- ATC-L04
- Arzneistoff
- Orphan-Arzneimittel
- Aminobenzol
- Piperidin
- Indolin
- Imid
Wikimedia Foundation.
