- Myasthenia gravis
-
Klassifikation nach ICD-10 G70 Myasthenia gravis und sonstige neuromuskuläre Krankheiten G70.0 Myasthenia gravis ICD-10 online (WHO-Version 2011) Die Myasthenia gravis pseudoparalytica (von griech. mys „Muskel“, -asthenie „Schwäche“, lat. gravis „schwer“ pseudo „falsch“ und paralysis „Lähmung“; Kürzel: MG) gehört zu einer Gruppe von neurologischen Erkrankungen, die durch eine gestörte Signalübertragung zwischen Nerv und Muskel gekennzeichnet sind, und als Störungen der neuromuskulären Erregungsübertragung oder als myasthene Syndrome zusammengefasst werden. Die Myasthenia gravis ist eine Autoimmunerkrankung, die durch Autoantikörper an der motorischen Endplatte der quergestreiften Muskulatur (Skelettmuskulatur) verursacht wird. Das Krankheitsbild ist gekennzeichnet durch eine belastungsabhängige Muskelschwäche der Skelettmuskulatur, die typischerweise im Tagesverlauf zunimmt und sich nach Erholungsphasen bessert.
Inhaltsverzeichnis
Myasthenia gravis beim Menschen
Häufigkeit
Die Myasthenia gravis ist eine relativ seltene Erkrankung. Die Krankheitshäufigkeit (Prävalenz) liegt bei etwa 100 bis 200 Erkrankungen pro 1 Million Einwohner. Die Krankheit kann sich in jedem Lebensalter manifestieren, sie hat jedoch zwei Manifestationsgipfel. Der erste Gipfel liegt zwischen der zweiten und dritten Lebensdekade mit Bevorzugung des weiblichen Geschlechts, der zweite Gipfel zwischen der sechsten und achten Lebensdekade mit Bevorzugung des männlichen Geschlechts.[1] Die Myasthenia gravis kommt bei Frauen häufiger vor (Verhältnis 3:2).[2] In Nordamerika und Europa sind 10 bis 14 % der Patienten jünger als 10 Jahre. Die Krankheitshäufigkeit hat seit Beginn der epidemiologischen Erhebungen um 1950 zu dieser Erkrankung zugenommen; in den 1990er Jahren lag die Krankheitshäufigkeit etwa viermal höher. Diese Zunahme wird auf den zunehmenden Bekannheitsgrad der Erkrankung, auf bessere diagnostische Verfahren, die Abnahme der Mortalität und Veränderungen in der Altersstruktur der Bevölkerung zurückgeführt.[3]
Ursache
Weder Ursachen noch Auslöser dieser Erkrankung sind heute vollständig erforscht bzw. zu erklären. Es wird vermutet, dass es neben den bekannten Antikörpern AChR-AK (Acetylcholin-Rezeptor-Antikörper) und MuSK-AK (Muskelspezifische Rezeptor-Tyrosinkinase-Antikörper) noch weitere Myasthenie-relevante Antikörper geben könnte. Nachgewiesen sind lediglich bestehende Zusammenhänge zu Myasthenie-relevanten Antikörpern und zum Thymus und der kausalen Basis der Erkrankung, der gestörten Signalübertragung zwischen Nerv und Muskel. Ungeklärt ist auch der Auslöser der schwankenden Symptomatik bei Umwelteinflüssen, Infekten, Entzündungen, seelischen und psychischen Belastungen. [4]
Krankheitsentstehung
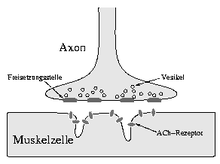
Die Myasthenia gravis ist eine Autoimmunerkrankung, d. h. der Körper bildet Autoantikörper, welche mit den Acetylcholinrezeptoren (AChR) interagieren. Die Wechselwirkung zwischen dem Transmitter Acetylcholin und dessen Rezeptor wird verhindert oder erschwert. Deshalb kann der elektrische Impuls (das Aktionspotential) vom Nerven nicht mehr auf den Muskel übertragen werden, der Muskel wird nicht erregt. Darüber hinaus verringert sich die Anzahl der Acetylcholinrezeptoren, da durch die Bindung der Antikörper an den Acetylcholinrezeptoren selbige durch eine Immunaktivität abgebaut werden. Dabei zerfällt die Struktur der subsynaptischen Membran in Bruchstücke. Durch Endozytose entsteht ein Autophagosom. Transportvesikel mit Verdauungsenzymen verschmelzen mit den Autophagosomen. Die Acetylcholinrezeptoren werden durch diese Immunreaktion alle zwei bis drei Tage abgebaut. Die Struktur der motorischen Endplatten wird verändert. Die subsynaptischen Einfaltungen (junctional folds) werden flacher und der synaptische Spalt wird breiter. Dies hat zur Folge, dass bei der Ausschüttung des Acetylcholins, Acetylcholin aus dem synaptischen Spalt diffundiert oder es von dem Enzym Cholinesterase hydrolysiert wird, bevor es einen Acetylcholinrezeptor besetzen kann. Die Erkrankung kann in jedem Alter auftreten, ist aber bei Frauen zwischen 20 und 40 Jahren gehäuft. Bei MG sind Veränderungen des Thymus sehr häufig nachweisbar. Man vermutet, dass der Thymus bei der Erkrankung eine wichtige Rolle spielt. Gelegentlich ist die MG durch ein Thymom bedingt, das die schädlichen Autoantikörper produziert. In diesen Fällen kann durch eine chirurgische Entfernung der Thymusdrüse der Krankheitsverlauf positiv beeinflusst werden.
Klinische Erscheinungen
Am Morgen und nach Ruhepausen ist die Leistungsfähigkeit am besten, doch nach wenigen wiederholten Bewegungen sind verschiedene Muskeln oder auch ganze Muskelgruppen erschöpft. Häufig treten die Symptome abends stärker auf. Von den Lähmungen bzw. anfänglich nur Einschränkungen der Beweglichkeit sind besonders kleine Muskeln betroffen, prinzipiell können aber alle quergestreiften (willkürlich bewegbaren) Muskeln betroffen sein.
Muskelgewebe ohne motorische Endplatten, wie der Herzmuskel und die glatte Muskulatur, sind nicht von der Krankheit betroffen. Die Beteiligung Letzterer ist allerdings wissenschaftlich bisher nie ausgeschlossen worden. Ein Hinweis auf Beteiligung könnte die Wirksamkeit der Pyridostigmin-basierten Myasthenie-Medikamente auf die Darmtätigkeit sein, da der Darm (bis auf Schließmuskulatur) aus glatter Muskulatur besteht. Ein weiterer Hinweis könnte auch die darmverursachte Obstipation sein, die zu den Symptomen des ebenfalls autoimmun-verursacht vermuteten Lambert-Eaton-Rooke-Syndrom (LEMS) gehört.
In etwa 50% der Fälle macht sich die Myasthenia gravis zuerst an den Augen, Augenlidern und/oder den äußeren Augenmuskeln bemerkbar: Durch Ermüden der Lidhebermuskeln kommt es zum typischen „Schlafzimmerblick“ (Ptosis), weil die Lider nicht mehr hochgehalten werden können. Die Patienten legen den Kopf zurück, um unter den Lidern hindurchschauen zu können. Typische Frühsymptome sind daher Ptosis sowie Diplopie (Doppelbilder), oder auch eine mangelnde oder unmögliche Schließfähigkeit eines oder beider Augenlider. Als "Signe des cils" (Zilienzeichen) bezeichnet man in diesem Zusammenhang das Sichtbarbleiben der Wimpern bei schwachem Lidschluß (auch zu beobachten bei peripherer Fazialisparese). Weitere typischerweise früh betroffene Muskelgruppen sind die mimische Muskulatur, die Mund- und Zungenmuskulatur („lachendes“ starres Gesicht, verwaschenes oder unmögliches Sprechen), die Hals- und Nackenmuskulatur (Kopfhalteschwäche), die Kau- und die Rachenmuskulatur (Schluckstörung bis hin zur Unfähigkeit Speichel abzuschlucken). Bei weiterem Fortschreiten sind in den meisten Fällen die Arme stärker betroffen als die Beine. Ferner kann die Atemmuskulatur so stark beeinträchtigt werden, dass Betroffene nur im Sitzen schlafen können oder in fortgeschrittenem Stadium beatmet werden müssen. Auch die Schluckmuskulatur kann so stark betroffen sein, dass eine unterstützende oder vollständige Versorgung über eine Magensonde indiziert ist.
Gleichgewichts-, degenerative Gedächtnis- oder Sensibilitätsstörungen sind keine Anzeichen einer MG.
Zur Charakteristik der Symptome ist zu sagen, dass sie wechselnd, nicht statisch und starr sind. Wechselnd sowohl in Bezug auf Uhrzeit, auslösende Stärke der Belastung und der „Auswahl“ aktuell betroffener Muskeln bzw. Muskelgruppen – z. B. linke Hand rechtes Auge, einmal zusammen, einmal einzeln oder früh oder abends. Die Symptome sind nicht vorhersehbar und meist plötzlich „hereinbrechend“. Manche Muskeln bzw. Muskelgruppen sind lediglich in ihrer Beweglichkeit eingeschränkt, bei anderen kann wiederum die ganze Kraft fehlen, sie überhaupt zu bewegen. Da diese Wechselhaftigkeit des Verlaufs bei einem einzelnen Betroffenen bzw. im Vergleich von Patient zu Patient so vielfältig ist, kann eigentlich von einer generellen Klinik (Erscheinungsform) nicht gesprochen werden.
Verlaufsformen
- "Klassische" AChR-Antikörper-MG
- MuSK-Antikörper-positive-MG
- Kv1.4-Antikörper-positive-MG, einem Kalziumkanal-Antikörper
- MG mit Beteiligung weiterer Antikörper wie z.B. MGT30 oder RyR
- Seronegative MG, d.h.ohne Antikörperbeteiligung
- Alters-MG, mit häufigeren Titin-Antikörpern
- MG im Kindesalter mit häufigeren Fällen nicht nachweisbarer Antikörper
- Neonatale MG bei Neugeborenen
Erstsymptomatik
- Über 50 % beginnend mit okulärer Symptomatik (z. B. Lidschwäche und/oder Doppelbilder)
- Etwa 14 % beginnend mit Schluck- und Sprechstörungen
- Etwa 8 % beginnend mit Arm- bzw. Beinschwächen (z. B. unklarer Fußheber-Paresen)
- Sehr seltener Beginn bei der Rumpf- und Wirbelsäulenmuskulatur
Komplikationen
Lebensbedrohlich ist in einer Krise das akute Versagen der Atemmuskeln. Bei dieser akuten Verschlechterung der Symptome mit Atemproblemen spricht man von einer „myasthenen Krise“ oder bei Überdosierung von Cholinesterasehemmern wie Pyridostigmin, von einer „cholinergenen Krise“. Sehr hilfreich ist hier der Nothilfe-Ausweis, der medizinische Maßnahmen und Ansprechpartner beschreibt. (Ausweise werden von der „Deutschen Myasthenie Gesellschaft“ bzw. von betreffenden Pharmaherstellern ausgegeben). Im Falle beider Krisen ist rasche Aufnahme und kompetente Behandlung auf einer Intensivstation gefordert, da die Mortalitätsrate immer noch recht hoch ist (nach Literatur 4–13 %).
Durch Verschlucken (Schluckstörung) kann es zu einer schweren Lungenentzündung kommen, einer Aspirationspneumonie.
Symptomverstärkend sind:
- Infekte, Entzündungen, Fieber, Hitze, Vibrationen
- Interkurrente Erkrankungen (Schilddrüse)
- extreme Belastungen (seelisch, körperlich)
- auch Belastungen wie Narkosen, vor allem bei der Wahl myasthenie-kontra-indizierter Narkotika
- hormonelle Schwankungen
- Fehlbehandlungen bzw. -dosierungen bei der medikamentösen Therapie (das Zuviel oder Zuwenig, was symptomatisch auch schwankt)
- Verschiedene Medikamente (myasthenie-kontra-indizierte Schmerzmittel, Antibiotika, Psychopharmaka, Hormonprodukte, Röntgenkontrastmittel usw.) [5]
Eine nicht unerhebliche Komplikation entsteht ebenfalls mit der Tatsache, dass die Diagnose MG sehr spät (statistisch nach 2,7 Jahren) gestellt wird. Aufgrund erwähnter Wechselhaftigkeit der Symptome, sowie der anfänglichen schwachen Ausprägung von Symptomen, werden diese häufig übersehen oder fehlinterpretiert, so dass es sogar zu erheblichen diagnostischen Missverständnissen und Fehldiagnosen kommt. Einerseits bedeutet das für die Betroffenen zusätzliche Symptomverschlechterung aufgrund des Fehlens der dringlichen medikamentösen Behandlung sowie eine zusätzliche psychische Belastung wegen der nicht seltenen Odyssee durch medizinische Einrichtungen.
Untersuchungsmethoden
Die Diagnose wird vor allem aus:
- klinischem Bild,
- dem Nachweis von Acetylcholinrezeptor-Antikörpern (AChR-AK),
- der sofortigen, kurzen (nur einige Minuten anhaltenden) Besserung nach Verabreichung von Acetylcholinesterase-Inhibitoren und durch
- elektrophysiologische Untersuchungen
gestellt. Abhängig von der Schwere der Erkrankungen unterteilt man die MG in verschiedene Stadien (nach Osserman und Genkins):
Stadium Bezeichnung befallene Körperregionen I rein okuläre Myasthenia gravis nur Augenmuskeln IIa leichte Generalisierung ganzer Körper IIb mittelschwere Generalisierung ganzer Körper III schwere akute Generalisierung ganzer Körper mit Atemmuskulatur IV schwere chronische Generalisierung Der „Besinger-Score“ dient der klinischen Verlaufsbeurteilung.
Einzelne Untersuchungsmethoden sind:
- Simpson-Test (Ermüden der Augenlider im längeren Aufblick)
- Suche nach Doppelbildern
- Intensive, über das „normale Maß“ der Standard-Neurologie hinausgehende Belastungstests verschiedener Muskelgruppen - Voraussetzung zur Erstellung eines aussagekräftigen MG-Score
- Prostigmintest, Tensilon-Test (vorübergehendes Verschwinden von Symptomen nach intravenöser Injektion), richtungsweisend für eine Neuro-Transmitter-Erkrankung, aber nicht alleinig, spezifisch für eine MG
- Eisbeuteltest, ähnlich wie beim eben erwähnten Medikamententes, kann auch eine aufgelgte Eiskompresse, z.B. auf ein gerade schwer schließbares Augenlid oder selbiges das gerade herab hängt, das Symptom abmildern. Sollte die Kälte das Symptom beeinflussen, ist dies richtungsweisend
- Repetitive Serienstimulation einzelner Nerven (RSN) – elektropysiologischer Test, bei dem bei Betroffenen unter der künstlichen Simulation (Nachahmung) von Muskelbelastung, ein Dekrement² nachgewiesenen werden kann.
- Einzelfaser-EMG - ähnlich, wie die Stimulation elektropysiologisch, allerdings sehr aufwendig und im Falle der Seronegativen MG kein Nachweis möglich
- Elektromyographie (Dekrement zeichen - Abnahme der Amplitude der evozierten Reizantwortpotentiale im Erfolgsmuskel)
- Histologischer Nachweis von Lymphoidzellen in Muskelbiopsaten
- Labor-Diagnostik - Nachweis von Acetylcholinrezeptor-Antikörpern und /oder von Anti-MuSK-Antikörpern im Blut
- Belastungstests im Rahmen einer Schluck-Diagnostik durch myasthenie-erfahrene logopädische Therapeuten, apparativ mittels einer Videoendoskopie und/oder bildgebender Schluckstudie
- bildgebende Diagnostik (CT mit Kontrastmittel) der Lungenregion um die Thymusdrüse
² Dekrement - Spezielle abnehmende Form einer Amplitude, aus der eine abnehmbare Muskelbelastbarkeit abgelesen werden kann. Das gegenteilige Inkrement, ist eine spezielle zunehmende Form einer Amplitude. Sollte sich dieses in einer Serienstimulation zeigen, ist neben der Myasthenia gravis, an ein LEMS (Lambert Eaton Myathenes Syndrom) differenzialdiagnostisch zu denken. Hier ist dann ein Test der Kalziumkanal-Antikörper (VGCC-AK) zu erwägen. Das LEMS ist wie die MG eine muskelschwächende Erkrankung.
Zur Labor-Diagnostik ist anzumerken, dass in 50 % der okulären und etwa 10–15 % der generalisierten Fälle keine AChR-AK und in der Hälfte dieser Fälle auch keine MuSK-AK oder andere Antikörper nachweisbar sind. Es handelt sich dann um eine seronegative MG. Auch hier ist die Diagnosestellung erschwert, und ist für myasthenie-erfahrene Neurologen, anhand des Verlaufs zu beurteilen.
Zu den elektrophysiologischen Untersuchungen ist zu sagen, dass eine gewisse Erfahrung zur Diagnostik notwendig ist. Zu Fehlerquellen gehören zu wenig untersuchte Muskeln, eine zu kalte Muskulatur und/oder ein durch den Untersucher zu wenig belasteter Muskel oder gar lediglich nur durch den Patienten während der Untersuchung betätigten Muskels sowie mangels Unwissen, z. B. zum rechtzeitigen Absetzen (falls medizinisch vertretbar) von beeinflussenden medikamentösen Therapien (z. B Pyridostigmin, den Cholinesterasehemmern. Auch kann erst ein im ersten Moment grenzwertiges Dekrement (7–9 %), nach erneuter Messung 2 und 5 Minuten posttetanisch, als pathologisch beurteilt werden.
Differenzial-Diagnostik
Gegenüber der Myasthenia Gravis sind vor allem auszuschließen:
- Lambert-Eaton-Rooke-Syndrom LEMS
- Amyotrophe Lateralsklerose ALS
- Multiple Sklerose MS
- Allgemeinere Muskelschwächen, verursacht durch z. B. Anorexie, Kachexie oder auch anderer seelischer, psychiatrischer oder neurologischer Erkrankungen
- Hirnerkrankungen, Durchblutungsstörungen, Stoffwechselstörungen
bzw. manifestieren sich abzugrenzende Sonderformen:
- neonatale Myasthenie (Neugeborene)
- medikamentös, boreolös bzw. durch Gifte erzeugte myasthene Symptome
- Myasthene Syndrome (kongenitale Myasthenie-Syndrome), die keine Autoimmunerkrankungen sind
Therapie
- Durch Cholinesterasehemmer, z. B. Neostigmin-Nasenspray oder Pyridostigmin-Tabletten bzw. -Injektionslösungen, die den Abbau des Transmitters Acetylcholin (ACh) hemmen, wird die Konzentration des ACh im synaptischen Spalt erhöht und damit der Autoantikörper kompetitiv verdrängt.
- Immunsuppressive Behandlung mit Glucocorticoiden oder Azathioprin kann die Antikörperwirkung abgeschwächt werden. Bei schweren oder kritischen Verläufen werden eine Plasmapherese oder hochdosierte Immunglobulingaben eingesetzt.
- Chirurgische Entfernung des Thymus oder eines Thymoms (Thymektomie)
- Umstellung auf nicht-Lungen-aspirierende Kost, vorbeugende Schlucktherapie und in schweren Fällen Ernährung per PEG (Magensonde), apparativer Sekret-Absaugung und/oder Tracheostoma (→ Tracheotomie)
- Sollten die Doppelbilder konstant bleiben, schafft ein augenärztlich ausgemessenes Prismenglas in einer Brille oder eine mittels Wasserfilm auf ein Glas einer vorhandenen Sehbrille ansaugbare bzw. anklebbare Prismenfolie einen Ausgleich.
Verlauf und Heilungsaussicht
Bleiben nur die Augenmuskeln betroffen, ist die Prognose gut und mit medikamentöser Therapie beherrschbar. Die Ausbreitung auf den gesamten Körper (Generalisierung) war hingegen vor einigen Jahren noch unheilbar. Durch moderne Medikamente ist in diesen Fällen die Prognose in den letzten Jahren deutlich besser geworden. Das bedeutet aber eine lebenslange Medikation. Weitere Maßnahmen, wie z.B. erwähnte PEG oder Tracheostoma wirken lebensverlängernd, können aber einen erheblichen Verlust an Lebensqualität bedeuten. Bei zu später oder gar fehlender Diagnosestellung, schweren Verläufen und Krisen (siehe Komplikationen) kann die Lebenszeit verkürzt sein.
Die Thymektomie führt vor allem bei jungen Patienten oft zu einem Rückgang der Symptome. In diesem Fall ist einige Jahre nach der Thymusentfernung evtl. auch das Absetzen der immunsuppressiven Medikamente möglich und somit eine deutliche Besserung, manchmal wird auch eine Remission erreicht.
Myasthenia gravis bei Tieren
Die Myasthenia gravis kommt vor allem bei Haushunden vor. Hier werden eine angeborene und eine erworbene Form unterschieden. Die Pathogenese ist die gleiche wie beim Menschen, also eine Autoimmunerkrankung, die sich gegen die Acetylcholinrezeptoren richtet. Die Behandlung erfolgt wie beim Menschen.
Angeborene Myasthenia gravis
Die angeborene Myasthenia gravis ist relativ selten und tritt gehäuft bei einigen Hunderassen (Jack Russell Terrier, Glatthaar Foxterrier, Springer-Spaniel) auf. Die Erkrankung wird autosomal-rezessiv vererbt und tritt typischerweise in der 6. bis 8. Lebenswoche auf.
Erworbene Myasthenia gravis
Die erworbene Myasthenia gravis ist häufiger und vermutlich multifaktoriell bedingt, wobei wohl ebenfalls eine genetische Prädisposition vorliegt. Thymome kommen ebenfalls als Auslöser in Betracht. Die Altersprädisposition ist zweiphasisch, mit einem Häufigkeitsmaximum bei Junghunden (1.-4. Lebensjahr) und einem bei alten Hunden (ab 9. Lebensjahr).
Klinisch äußert sie sich zumeist in lokalen Muskelstörungen. Häufig (etwa 80 % der Fälle) ist vor allem die Speiseröhre betroffen und es entwickelt sich ein Megaösophagus. Klinisch zeigt sich ein häufiges Regurgitieren. Hier besteht ein besonders hohes Risiko für eine Aspirationspneumonie. Auch die Rachenmuskulatur kann involviert sein, was sich in Stimmveränderungen äußert. Eine dritte häufige Lokalisation sind wie beim Menschen die Augenmuskeln. In diesem Fall ist der Lidschlussreflex vermindert und schnell ermüdbar. Die generalisierte Form äußert sich in schneller Ermüdbarkeit, steifem Gang bis hin zu einer Paraparese der Hintergliedmaßen oder Tetraparese. Auch ein Megaösophagus ist häufig. Eine myasthenische Krise mit akuter Para- oder Tetraparese und Megaösophagus kann ebenfalls auftreten.
Die Diagnose kann sicher nur mit dem Nachweis der Autoantikörper gestellt werden. Bei einem Megaösophagus oder bei Thymomen kann eine Röntgenaufnahme des Brustkorbs wichtige Hinweise geben. Differentialdiagnostisch müssen andere Polyneuropathien, Botulismus (selten beim Hund), Polymyositis, Zeckenparalyse (selten) und Azetylcholin- oder Organophosphat-Vergiftungen ausgeschlossen werden (Siehe auch VETAMIN D).
Geschichte
MG ist seit dem 17. Jahrhundert bekannt. Der erste dokumentierte Fall wurde in englisch-amerikanischer Kolonialpost gefunden. Er stammt aus dem Jahr 1644 und beschreibt die Schwäche des Indianerhäuptlings Opechankanough zu gehen (Universität zu Virginia, Neurologie, Charlottesville). Die englische Erstbeschreibung erfolgte 1672 durch den Oxforder Arzt Thomas Wills im lateinisch verfassten „De Anima Brutorum“ (was allerdings bis 1903 unbeachtet blieb). Die erste modernere Fallbeschreibung verfasste der Londoner Arzt Samuel Wilks 1877. Deutsche Fallberichte erschienen im 19. Jahrhundert durch den Heidelberger Wilhelm Erb und Hermann Oppenheim. 1893 verfasste Samuel Goldflam in Warschau die bis dahin umfassendste Publikation.
Friedrich Jolly führte nachweisende elektrophysiologische Untersuchungen durch und prägte ab 1895, den bis heute üblichen Namen „Myasthenia gravis pseudoparalytica“. Nach ersten neuen Erkenntnissen über den Zusammenhang mit der Thymusdrüse, Anfang des 20. Jahrhunderts führte 1912 Sauerbruch die erste Thymektomie durch. Ab 1934 gab es durch einen bisher unbekannten Konsiliarus und die englische Assistenzärtzin Mary Walker die erste wirksame medikamentöse Therapie und damit einen Hinweis auf eine gestörte Übertragung zwischen Nerv und Muskel. Dieser kausale Zusammenhang wurde allerdings erst nach 1960 nachgewiesen. Bereits 1960 wies John Simpson hypothetisch auf eine autoimmune Genese hin. Der Nachweis der AChR-Antikörper gelang erst 1974. [7]
Literatur
- Publikationen der „Deutschen Myasthenie Gesellschaft“ e.V.
- Publikationen der „Deutschen Gesellschaft für Neurologie“ (Deutsche Gesellschaft für Neurologie)
- Publikationen der Fa. Temmler (pdf Zurück zur Bewegung)
- Hohenegger M: Allgemein-Anästhesie bei Myasthenia gravis; intensiv 2006; 14:72-75
- Wolfgang Köhler und Jörn P. Sieb: Myasthenia gravis (UNI-MED Science) - (Oktober 2003)
- Conti-Fine BM, Milani M, Kaminski HJ: Myasthenia gravis: past, present, and future. J Clin Invest. 2006 Nov;116(11):2843-54. PMID 17080188
- Juel VC, Massey JM: Myasthenia gravis. Orphanet J Rare Dis. 2007 Nov 6;2:44. PMID 17986328
Einzelnachweise
- ↑ Phillips LH: The epidemiology of myasthenia gravis. Semin Neurol 2004 Mar;24(1):17-20. PMID 15229788 In: Shawn J Bird: Clinical manifestations of myasthenia gravis. UpToDate Version 17.2 (2009)
- ↑ Claus Werner Wallesch: Neurologie: Diagnostik und Therapie in Klinik und Praxis. Elsevier 2005, S. 841. ISBN 3-437-23390-4
- ↑ J. Dörr, F. Zipp: Myasthenia gravis: Aktuelle Aspekte der Pathogenese, Diagnostik und Therapie. Nervenheilkunde 2007; 26: 587-595 Zusammenfassung, Volltext
- ↑
- Publikationen der „Deutschen Myasthenie Gesellschaft“ e.V.
- Publikationen der „Deutschen Gesellschaft für Neurologie“ ([1] → MG)
- ↑ http://www.medicalforum.ch/pdf/pdf_d/2003/2003-37/2003-37-121.PDF
- ↑
- Das EMG-Buch und periphere Neurologie in Frage und Antwort - Von Christian Bischoff, Wilhelm J. Schulte-Mattler, Bastian Conrad, Georg-Thieme-Verlag 2005 S. 288 ff
- Schluckstörungen - Diagnostik und Rehabilitation - David Buchholz, Gudrun Bartolome, Hubertus Feussner, Christian Hannig, Heidrun Schröter-Morasch, Stefanie Neumann, Christian Pehl, Mario Prosiegel, Anita Wuttge-Hannig - Mitwirkende Personen Gudrun Bartolome, Veröffentlicht von Elsevier GmbH Deutschland, 2006
- Publikationen der „Deutschen Myasthenie Gesellschaft“ e.V.
- uni-goettingen.de
- Publikationen der „Deutschen Gesellschaft für Neurologie“
- ↑
- In „Neuromuscul Disorder“ UK.2005 Dec;15(12):878-86. Epub 2005 Nov 9, „The early history of myasthenia gravis“ von Hughes T. (Green College, University of Oxford)
- In „Neurol. Clinics“ 1994 May;12(2):231-42, „The history of myasthenia gravis.“ von Pascuzzi RM. (Department of Neurology, Indiana University School of Medicine, Indianapolis.)
- Publikationen der „Deutschen Myasthenie Gesellschaft“ e.V.
- Myasthenia Gravis - Wolfgang Köhler und Prof. Dr. Jörn P. Sieb (Hrsg.)UNI-MED Science, 3., neubearb. Auflage 2008, 160 Seiten, 98 Abb., Hardcover, ISBN 978-3-8374-1042-6
Weblinks
- S1-Leitlinie Myasthenia gravis der Deutschen Gesellschaft für Neurologie. In: AWMF online (Stand 01.10.2008)
- Seiten der Deutschen Myasthenie-Gesellschaft
- Patientenbroschüre Zurück zur Bewegung

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- Hundekrankheit
- Erbkrankheit des Hundes
- Krankheitsbild in der Neurologie
- Autoimmunerkrankung
Wikimedia Foundation.