- Neumutation
-
Eine Mutation (v. lat. mutatio „Veränderung“, „Wechsel“) ist eine Veränderung des Erbgutes eines Organismus durch Veränderung der Abfolge der Nukleinbasen oder durch Veränderung der Chromosomenzahl, die nicht auf Rekombination oder Segregation beruht. Dieser Begriff wird daher nur für einen Teilbereich aller möglichen Chromosomenaberrationen verwendet. Durch eine Mutation wird die in der DNA gespeicherte Information verändert und dadurch können einzelne Merkmale (der Phänotyp) verändert werden.
Das „durchschnittliche Ausmaß“ der Mutationen bei der Vererbung innerhalb einer Population nennt man Diversifikation. Ein Organismus mit einer Mutation wird als Mutant oder Mutante bezeichnet.
Inhaltsverzeichnis
Arten der Mutation
Unterscheidung nach Erblichkeit
-
- Keimbahnmutationen
- sind Mutationen, die an die Nachkommen über die Keimbahn weitergegeben werden; sie betreffen Eizellen oder Spermien und werden durch Zellteilung an alle anderen Zellen weitergegeben. Diese Mutationen sind sehr wichtig für die Evolution, da sie von einer Generation zur nächsten übertragbar sind.
-
- somatische Mutationen
- sind Mutationen, die alle anderen Körperzellen aber nicht die Keimzellen betreffen können. Sie haben daher auch nur Auswirkungen auf die Zellen des Organismus, in denen sie stattfinden, d. h. somatische Mutationen werden nicht vererbt. Wenn diese somatischen Mutationen nur vereinzelt auftreten, haben sie keine oder nur geringe Folgen. Wird ihr Auftreten jedoch durch Mutagene wie z. B. energiereiche Strahlung oder Umweltgifte verstärkt, haben sie ein großes Gefahrenpotential. So können sich dadurch unter anderem normale Körperzellen in ungebremst wuchernde Krebszellen umwandeln. Auch bei dem Alterungsprozess eines jeden Organismus spielen somatische Mutationen eine entscheidende Rolle. Sie haben daher in der praktischen Medizin eine zunehmende Bedeutung.
Unterscheidung nach Ursache
-
- Spontanmutationen
- sind Mutationen ohne äußere Ursache, wie der chemische Zerfall eines Nukleotids (Cytosin desaminiert oxidativ z.B. spontan zu Uracil) oder der Tunneleffekt (Protonen-Tunneln in DNA[1]).
-
- induzierte Mutationen
- sind durch Mutagene (mutationsauslösende Stoffe) oder ionisierende Strahlen erzeugte Mutationen.
-
- Replikationsfehler
- DNA-Polymerasen haben unterschiedlich hohe Fehlerraten. Bevorzugt wird ein ATP eingebaut, da das Molekül am häufigsten in der Zelle vorkommt.
-
- Unzureichende Proof-reading-Aktivität
- Manche DNA-Polymerasen haben die Möglichkeit Fehleinbaue selbständig zu erkennen und zu korrigieren. Die DNA-Polymerase α der Eukaryoten besitzt jedoch z.B. keine proof-reading-Aktivität (proof-reading = "Korrekturlesen").
-
- Fehler bei prä- und postreplikativen Reparaturmechanismen
- Beim Einbau/Finden eines ungewöhnlichen Nukleotids, etwa von Uracil in der DNA, wird dieses entfernt, bei einer Fehlpaarung zwischen 2 DNA-typischen Nukleotiden muss sich das Reparaturenzym entscheiden mit 50%iger Fehlerwahrscheinlichkeit.
-
- inäquales Crossing-over
- sind Fehlpaarungen bei der Meiose durch auf einem Strang naheliegende ähnliche oder identische Sequenzen, wie etwa Satelliten-DNA oder Transposons.
-
- Integration oder Herausspringen von Transposons
- Springende Elemente können in Gene oder genregulatorische Bereiche integrieren. Beim Herausspringen hinterlassen sie Spuren, sogenannte footprints.
Unterscheidung nach Veränderung
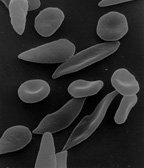 Die Sichelzellenanämie wird durch eine Mutation im Gen einer Hämoglobin-Untereinheit ausgelöst. Sie führt zu sichelförmigen roten Blutkörperchen, hier zusammen mit normalen Formen.
Die Sichelzellenanämie wird durch eine Mutation im Gen einer Hämoglobin-Untereinheit ausgelöst. Sie führt zu sichelförmigen roten Blutkörperchen, hier zusammen mit normalen Formen.-
- 1. die Genmutation
- eine erbliche Änderung, die nur das einzelne Gen betrifft. Man unterscheidet zwischen Raster- und Punktmutation. Bei der Punktmutation wird lediglich eine organische Base im genetischen Code verändert (mutiert). Die Rastermutation jedoch führt zum Einschub oder Entfernen einer Base und verändert somit die gesamte Struktur des Gens. Deshalb hat die Rastermutation weit höhere Auswirkungen. Mutationen in Genen deren Genprodukte für die Aufrechterhaltung eine intakten DNA erforderlich sind, zum Beispiel Tumorsuppressorgene, können weitere Mutationen nach sich ziehen (Mutatorphänotyp).
-
- 2. die Chromosomenmutation oder Segmentmutation
- ebenfalls eine erbliche Änderung, die einzelne Chromosomen in ihrer Struktur betrifft. Der im Mikroskop sichtbare Bau einzelner Chromosomen ist verändert. So können Chromosomenstücke verloren gehen oder Teile eines anderen Chromosoms eingebaut sein. Ein Beispiel ist das Katzenschrei-Syndrom, bei dem ein Abschnitt des Chromosoms 5 verloren gegangen ist. Dadurch fehlen zahlreiche Gene, die zu einer starken Veränderung und Schädigung im Phänotyp führen.
-
- 3. die Genommutation oder numerische Chromosomenaberration
- eine nicht-erbliche Änderung, bei der ganze Chromosomen oder gar Chromosomensätze vermehrt werden (Aneuploidie, Polyploidie) oder ganze Chromosomen verloren gehen. Ein bekanntes Beispiel beim Menschen ist das Downsyndrom. Hier ist das Chromosom 21 dreifach vorhanden.
Mit der Entdeckung des alternativen Splicings kommt ein weiterer Mutationstyp hinzu: die veränderte Regulation des Splicings, die letztlich auch im Erbgut, aber meist an anderer Stelle, verankert ist. Gleiches gilt für Mutationen der die Expression regulierenden Regionen in Gennähe.
Unterscheidung nach Folgen für den Organismus
-
- letale Mutationen
- sind Mutationen, die nach ihrem Auftreten einen Organismus unabhängig von seiner jeweiligen Lebensphase in jedem Falle töten.
-
- konditional-letale Mutationen
- sind Mutationen, deren Veränderung des Genprodukts einen Organismus nur bei bestimmten Wachstumsbedingungen tötet.
-
- Loss-of-function-Mutationen
- Hierbei wird das Genprodukt durch eine Mutation im Gen funktionslos. Ist der Funktionsverlust vollständig, spricht man von Nullallel oder einem amorphen Allel. Bleibt ein Teil der Wildtypfunktion erhalten bezeichnet man es als hypomorphes Allel.
-
- Gain-of-Function-Mutationen
- Hierbei gewinnt ein Gen an Aktivität und wird dann auch als hypermorph bezeichnet. Entsteht durch die Mutation ein komplett neuer Phänotyp, dann bezeichnet man das Allel auch als neomorph.
-
- Eine Gain-of-function-Mutation, die einen sichtbaren Phänotyp hervorruft, wird als "dominant" bezeichnet. Wenn ein Gain-of-function-Allel einen Phänotyp ausschließlich im homozygoten Zustand zeigt, spricht man jedoch von einer rezessiven Gain-of-Function-Mutation. [4]
-
- neutrale Mutationen
- können den Phänotyp verändern, haben aber keine Fitnesskonsequenzen.
-
- stille Mutationen
- sind Mutationen, die keinerlei Folgen für den Organismus haben.
Folgen
Keine Folgen - bei stillen Mutationen
Die meisten Mutationen führen dazu, dass eine Veränderung in einem DNA-Abschnitt keine Konsequenzen nach sich zieht, wenn die Stelle, die verändert wurde, nicht für eine genetisch relevante Information benutzt wird. Aber auch wenn die veränderte Stelle benutzt wird, kann es sein, dass der Informationsgehalt des Gens sich nicht verändert hat, da eine Reihe von Aminosäuren identisch kodiert sind (siehe: genetischer Code). Daher werden diese Mutationen stille oder stumme Mutationen genannt.
Solche Arten von Mutationen führen dazu, dass innerhalb einer Gruppe von Organismen funktional gleiche Gene unterschiedliche genetische „Buchstaben“ innerhalb ihrer Nukleotid-Sequenz besitzen. Diese Unterschiede, die Polymorphismen heißen, lassen sich ausnutzen, um Verwandtschaftsbeziehungen zwischen Individuen abzuleiten, oder auch um eine durchschnittliche Mutationsrate abzuschätzen.
Zusätzlich kommt noch zum Tragen, dass nicht nur beim diploiden Chromosomensatz oft mehrere Gene die gleichen genetischen Eigenschaften codieren, sodass sich eine Mutation aus diesem Grunde nicht sofort bemerkbar machen muss.
Negative Folgen
Besonders größere Veränderungen im Erbgut führen oft zu nachteilhaften Veränderungen im Stoffwechsel oder auch zu Fehlbildungen und anderen Besonderheiten.
Es gibt verschiedene Erbkrankheiten, die entweder vererbt sind oder durch Mutation neu auftreten können. Beispiele dafür sind:
- die Sichelzellenanämie, eine Blutkrankheit, bei der sich die äußere Form der roten Blutkörperchen ändert, was u. a. verringerte Sauerstoffaufnahme zur Folge hat,
- die Phenylketonurie, wobei der Abbau der Aminosäure Phenylalanin gestört ist, wodurch Schädigungen des kindlichen Gehirns hervorgerufen werden können,
- der Albinismus und
- die Mukoviszidose oder zystische Fibrose, die häufigste genetisch bedingte Krankheit Nordeuropas. Bei ihr ist das CFTR-Gen, das die Konsistenz der Drüsensekrete steuert, defekt. Wenn das Sekret zu zäh ist, kann es (je nach Drüse) die Atemwege oder die Ausführungsgänge der Drüsen verstopfen.
- Außerdem Formen von Minderwuchs, bei denen die Arme und Beine ungewöhnlich kurz sind, während der Körper ansonsten wie üblich gebaut ist,
- die Rot-Grün-Blindheit und
- die Bluterkrankheit, bei der die Blutgerinnung praktisch nicht einsetzt.
Positive Folgen
Der Entwicklungslehre Darwins zufolge ist die Mutation mit für die Artenvielfalt auf der Erde verantwortlich. Mutationen sind so (aber nicht nur) ein natürliches Phänomen und ermöglichen erst die Entwicklung der Arten (siehe: Evolutionslehre). Obwohl die Mutation die Dynamik der Evolution ausmacht, ist nur in den selteneren Fällen mit einer Veränderung im Genom ein Vorteil für das Individuum zu erwarten.
Durch Austausch der Basenpaare werden Proteine verändert oder einfach nur anders reguliert, was eine Änderung im Körperbau, oder in Körperfunktionen und oder im Verhalten des Organismus bewirken kann, die ihm Vorteile gegenüber seinen unveränderten Artgenossen bietet. Wenn diese Mutation an die Nachkommen vererbt wird, hat sie eine erste Voraussetzung erfüllt, dass sie sich einst „durchsetzen“ kann.
Der Mensch macht sich zudem den genomverändernden Effekt ionisierende Strahlen zunutze, um Mutationen künstlich auszulösen. Eine Anwendung besteht in der Bestrahlung von Blumen- und Pflanzensamen, um bisher unbekannte Formen zu erzeugen und wirtschaftlich zu nutzen. Das Verfahren hat meist aufgrund der breitgestreuten, zu umfangreichen und ungezielten Veränderung des Erbmaterials eine sehr geringe Erfolgsquote.
Beispiele
- Manx-Katzen sind durch Genmutation infolge extremer Inzucht entstanden. Neben der Schwanzlosigkeit bestehen Skelettmissbildungen und weitere Fehlbildungen. Manx-Katzen sind in diesem mutierten Gen "M" nie reinerbig, es liegt also bei ihnen die Kombination "Mm" vor, d.h. es besteht ein autosomal unvollkommen dominanter Erbgang mit variabler Expressivität (Ausprägung). Bei Tieren mit der reinerbigen Gen-Kombination "MM" sterben die Feten schon im Mutterleib.
- Die Sphynx-Katze hat keinerlei Fell. Diese Rasse wird seit 1966 aus einer in Kanada geborenen, natürlich mutierten Katze vom Menschen weitergezüchtet. Bei der gegenwärtigen Gesetzgebung in allen Ländern führt der Wunsch nach immer neuen Rasseattraktionen dazu, dass man auch Tiere weiter züchtet, die unter natürlichen Bedingungen nicht lebensfähig wären.
- In der Pflanzenzucht ermöglichen Mutationen große Fortschritte. Aus Gräsern mit kleinen Samen wurden ertragreiche Getreidesorten gezüchtet. Ohne Pflanzenzucht und Mutationen wäre es nicht möglich, die Weltbevölkerung zu ernähren.
- Laktose-Toleranz beim Menschen. Genetiker haben festgestellt, dass der Mensch ursprünglich generell mit einer genetisch determinierten (verankerten), nur auf die Kindheit begrenzten Laktosetoleranz (Milch- bzw. Milchzuckerverträglichkeit) ausgestattet war. Nach Ansicht der Forscher muss vor ca. 10.000 Jahren (nach anderen Quellen ca. 8.000 Jahren) beim Menschen im kaukasischen Raum eine Mutation aufgetreten sein, die die Laktosetoleranz auf die gesamte Lebensspanne ausgedehnt hat. Somit zeigen alle Nachkommen dieses Menschen zeit ihres Lebens keine gesundheitliche Beeinträchtigung beim Verzehr von Milch, wie sie andererseits noch heute unter anderem bei Asiaten oder Afrikanern auftritt, die damals von dieser Mutation nicht betroffen waren und es deshalb auch heute nicht sind (siehe Lactoseintoleranz).
- Gehirnentwicklung des Menschen. Die Gene Microcephalin und ASPM steuern beim Menschen das Größenwachstum des Gehirns und insbesondere das der Hirnrinde. Offensichtlich ist die Entwicklung des menschlichen Gehirns jedoch keineswegs abgeschlossen. Forscher um Bruce Lahn vom Howard Hughes Medical Institute der University of Chicago (USA) haben herausgefunden, dass zwei Mutationen in der jüngeren menschlichen Stammesgeschichte dem Gehirn ermöglichten, sich den veränderten Anforderungen besser anzupassen. Die Haplogruppe D als Ergebnis einer Mutation des Microcephalins entstand vor 37 000 Jahren im menschlichen Genom und verbreitete sich etwa gleichzeitig mit den ältesten Funden, die von der Beschäftigung des Menschen mit Kunst, Musik und Religion zeugen. Diese Mutation findet man heute bei etwa 70% aller Menschen. Bei einer weiteren Mutation entstand vor circa 5 800 Jahren die Haplogruppe D des ASPM und breitete sich etwa gleichzeitig mit ersten Zivilisation in Mesopotamien aus, von der auch die ältesten Schriftfunde der Menschheitsgeschichte stammen. Diese zweite Mutation hat sich bis heute bei etwa 30% der Weltbevölkerung durchgesetzt. Beide durch Mutation entstandenen Genvarianten kommen nun nach Angaben der Forscher besonders in Europa und den angrenzenden Gebieten Asiens und Afrikas vor. Die Parallelität der beschriebenen Ereignisse werden von den Wissenschaftlern dahingehend interpretiert, dass auf Grund positiver Selektion der evolutionäre Erfolg der beiden Mutationen mit ihrem günstigen Einfluss auf die Entwicklung des menschlichen Gehirns und dessen Leistungsfähigkeit in Zusammenhang steht.
- Erkrankungsrisiko bei Brustkrebs. Im Sommer 2006 haben Forscher um Naznee Rahman vom britischen Institut of cancer research in Surrey ein neues Brustkrebsgen mit der Bezeichnung BRIP-1 identifiziert. Dieses Gen kodiert ein Protein, welches an der Reparatur von DNA-Schäden beteiligt ist. Eine zugleich entdeckte, selten vorkommende Mutation dieses Gens bewirkt, dass das BRPI-1-Protein diese Schutzfunktion nicht mehr ausführen kann. Bei einem Vorliegen dieser Mutation haben Frauen ein doppelt so hohes Brustkrebsrisiko, wie andere mit einer normalen Version dieser Erbanlage. Mutationen der schon länger bekannten Gene BRCA1 und BRCA2 erhöhen dagegen das Erkrankungsrisiko um den Faktor 10 bis 20. [5]
Gartenbau
Im Gartenbau wird eine Mutation, aus der eine neue Sorte entsteht, auch „Abart“ oder „Sport“ genannt.
Literatur
- Wilfried Janning & Elisabeth Knust: Genetik: allgemeine Genetik, molekulare Genetik, Entwicklungsgenetik, Georg Thieme Verlag, Stuttgart / New York 2004, ISBN 3-13-128771-3
- Raymond Devoret (2001): Mutation. In: Encyclopedia of Life Sciences. doi:10.1038/npg.els.0001882 (Volltextzugriff)
- http://www.spektrum.de/artikel/836427 Dennis Drayna: Genspuren der Menschheitsgeschichte, Spektrum der Wissenschaft, Januar 2006, s. 30 ff.
Einzelnachweise
- ↑ Löwdin, P.-O.: Proton Tunneling in DNA and its Biological Implications. Reviews of Modern Physics 35 (3), 724-732 (1963).
- ↑ [1] Theodor Dingermann, Rudolf Hänsel, Ilse Zündorf: Pharmazeutische Biologie: Molekulare Grundlagen und klinische Anwendung, Springer, 2002, ISBN 3540428445, ISBN 9783540428442, S. 425
- ↑ Alberts et al., Molecular Biology of the Cell, 4. Aufl. 2002, S. 527
- ↑ http://kups.ub.uni-koeln.de/volltexte/2008/2294/ Ying Wang: Organisation of the cytoskeleton of the Drosophila oocyte, Kurzfassung in Deutsch, letzter Satz
- ↑ Truncating mutations in the Fanconi anemia J gene BRIP1 are low-penetrance breast cancer susceptibility alleles - Nature Genetics
-
Wikimedia Foundation.


