- Oxalylchlorid
-
Strukturformel 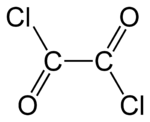
Allgemeines Name Oxalylchlorid Andere Namen - Oxalsäuredichlorid
- Oxalyldichlorid
Summenformel C2Cl2O2 CAS-Nummer 79-37-8 PubChem 65578 Kurzbeschreibung farblose Flüssigkeit mit stechendem Geruch[1]
Eigenschaften Molare Masse 126,93 g·mol−1 Aggregatzustand flüssig
Dichte 1,48 g·cm−3 (20 °C)[1]
Schmelzpunkt Siedepunkt 63–64 °C[1]
Dampfdruck Löslichkeit - Zersetzung in Wasser[1]
- löslich in Diethylether, Chloroform und Benzol[2]
Brechungsindex 1,434 (13 °C)[3]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 

Gefahr
H- und P-Sätze H: 331-335-314 EUH: keine EUH-Sätze P: 309+310-304+340-301+330+331 [1] EU-Gefahrstoffkennzeichnung [1] 
Giftig (T) R- und S-Sätze R: 14-23-29-34-37 S: 26-36/37/39-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C Oxalylchlorid ist eine chemische Verbindung mit der Summenformel (COCl)2. Es ist eine äußerst aggressive und stechend riechende Chemikalie. Es ist das Dichlorid der Oxalsäure, aus der es auch hergestellt wird. Die farblose Flüssigkeit ist aus wasserfreier Oxalsäure und Phosphorpentachlorid zugänglich.
Eigenschaften
Oxalylchlorid ist eine farblose, an feuchter Luft aufgrund von Hydrolyse rauchende Flüssigkeit. Es ist leicht flüchtig, jedoch bleibt beim Verdunsten/Verdampfen oft ein Rückstand an hydrolysierter Oxalsäure, die durch die Reaktion mit der Luftfeuchtigkeit entsteht.
Verwendung
Bei der Swern-Oxidation, einer selektiven Methode zur Herstellung von Aldehyden aus primären Alkoholen, dient Oxalylchlorid zur Aktivierung des Oxidationsmittels DMSO. Es wird verwendet, um aus sensiblen Alkoholen und Säuren die entsprechenden Chloralkane bzw. Säurechloride herzustellen. Trotz der geringeren Reaktivität gegenüber anderen Halogenierungsmitteln wird es aufgrund der besseren Selektivität verwendet.
Ebenfalls wird es benötigt, um Oxalsäureester herzustellen, die aus normaler Oxalsäure nicht zugänglich sind, zum Beispiel Phenyloxalate für die Peroxychemolumineszenz.
Einzelnachweise
- ↑ a b c d e f g h i Eintrag zu Oxalylchlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 29. August 2007 (JavaScript erforderlich).
- ↑ Ullrich Jahn in: Römpp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
Wikimedia Foundation.


