- PSA Wert
-
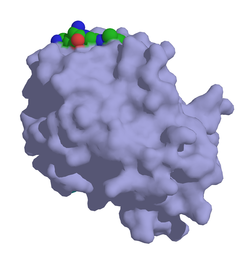
Prostataspezifisches Antigen Oberflächenmodell von PSA mit Substratfragment nach PDB 2ZCK Vorhandene Strukturdaten: 1pfa, 2psa, 2zch, 2zck, 2zcl Größe 237 Aminosäuren Bezeichner Gen-Namen KLK3; PSA Externe IDs OMIM: 176820 UniProt: P07288 Enzymklassifikation EC, Kategorie 3.4.21.77 Serinprotease MEROPS S01.162 Reaktionsart Hydrolyse Substrat Semenogelin -Tyr-+-Xaa- Produkte Spaltprodukte Das prostataspezifische Antigen (abgekürzt: PSA, auch Semenogelase oder Kallikrein-3) ist ein Enzym, das als physiologisches Sekretionsprodukt der prostatischen Ausführungsgänge dem Ejakulat beigemengt ist und der Verflüssigung des Samenkoagulums dient. Es handelt sich um eine typische Serinprotease, deren Substrat das Protein Semenogelin-1 ist, dessen Spaltung den Samen dünnflüssig macht.
PSA wird vom Drüsenepithel der Prostata und von den periurethralen Drüsen produziert und findet sich in hohen Konzentrationen im Seminalplasma (bis zu 3 mg/ml). Seine Bildung steht unter der Kontrolle von Androgenen. Die Halbwertszeit des gebundenen PSA beträgt 48 - 72 Stunden, es wird in der Leber metabolisiert, freies PSA hat eine Halbwertszeit von zwei bis drei Stunden und wird über die Niere ausgeschieden. Aus dem Seminalplasma wurde das PSA zuerst im Jahre 1979 von Wang isoliert.[1]
Mittlerweile ist PSA zum wichtigsten Marker in der Urologie geworden und ist der empfindlichste Parameter in der Diagnostik des Prostatakarzinoms. PSA gilt als Gewebemarker, nicht als reiner Tumormarker, da es naturgemäß auch beim Prostatagesunden nachweisbar ist, beziehungsweise bei der gutartigen Prostatavergrößerung (der sogenannten BPH) erhöht sein kann.
Inhaltsverzeichnis
Biosynthese
Um die Produktion des Enzyms hochzufahren, binden zunächst Androgene an den Androgenrezeptor in den Zellkernen von PSA-produzierenden Zellen im Prostataepithel. Der aktivierte Rezeptor agiert als Transkriptionsfaktor an einem Promoter des KLK3-Gens, welches für PSA codiert. Das Gen liegt beim Menschen auf Chromosom 19 und erstreckt sich über 5.850 Basenpaare und 5 Exons. Nach der Transkription entsteht mRNA mit 1.464 Basen und diese wird zu einem Precursorprotein mit 261 Aminosäuren translatiert. Posttranslationale Modifikation erzeugt das Endprodukt mit 237 Aminosäuren.[2][3]
Nachweis
PSA liegt in freier (fPSA) und gebundener Form (komplexiert an Chymotrypsin und Makroglobulin) vor. Mit konventionellen Assays wird das freie und das an Chymotrypsin gebundene PSA (tPSA) bestimmt. Der Anteil des fPSA, aber auch des komplexierten (cPSA) lässt sich getrennt messen. Nach Stamey ist in der Regel der PSA-Wert beim Karzinom (3 ng/ml Gewebe) höher als bei der BPH (0,3 ng/ml Gewebe).
PSA-Screening
Ziel des PSA-Screening ist die Erhöhung der Lebenserwartung durch Früherkennung von Prostatakrebs. Ob dieses Ziel erreicht werden kann, ist umstritten und jedenfalls bisher nicht nachgewiesen. Wer in Deutschland an Prostatakrebs stirbt, ist sogar drei Jahre älter als das durchschnittliche männliche Sterbealter. Weiter sind von den Männern über 50, die eines natürlichen Todes gestorben sind, ein Drittel nicht an Prostatakrebs verstorben, obwohl sie Prostatakrebs gehabt hatten. Männer ab ca. 70 Jahren sterben unter anderem mit Prostatakrebs, nicht an ihm.[4][5][6]
Mit der Einführung von PSA-Messungen konnte eine deutliche Verbesserung in der Diagnostik des Prostatakrebses erzielt werden. Die Verbreitung des Tests auch bei asymptomatischen Männern führte in den USA in den 1990er Jahren zu einem drastischen Anstieg der entdeckten Krebsfälle. Inzwischen ist ein Plateau erreicht. Unter den entdeckten Fällen hat der Anteil von Frühstadien deutlich zu- und die Rate an fortgeschrittenen Stadien abgenommen.
Wie bei anderen Screeningverfahren auch ist jedoch zu erwarten, dass Karzinome entdeckt wurden, die dem Patienten während seines Lebens nie Probleme bereitet hätten. Nach neueren Untersuchungen wird das Verhältnis für den Prostatakrebs auf mindestens 1:1 geschätzt, d.h. von jeweils zwei entdeckten Krebsfällen hätte einer den betroffenen Mann in dessen Leben nicht beeinträchtigt. Das Problem liegt aber darin, dass man nicht sicher voraussagen kann, wer eben doch von einer Therapie profitieren würde.
Zurzeit ist unklar, ob das PSA-Screening mehr Nutzen als Schaden für die teilnehmenden Männer bedeutet. Studien, die einen Nutzen des PSA-Screenings nachweisen sollen, laufen zurzeit. In den USA ist mit einigen Jahren Abstand zur Verbreitung des Tests eine Senkung der Sterblichkeit an Prostatakrebs eingetreten. Ob diese allerdings tatsächlich auf den Einsatz des Tests zurückzuführen ist, ist zweifelhaft. Dagegen spricht, dass es auch in England/Wales einen entsprechenden Rückgang der Sterblichkeit gab, ohne verbreitete PSA-Anwendung. Und dagegen spricht auch, dass in mehreren Studien in den USA und Kanada kein Unterschied in der Sterblichkeit zwischen „screeningintensiven“ und „screeningarmen“ Regionen gefunden werden konnte.
Zu allgemeinen Problemen von Screening-Untersuchungen und der Früherkennung von Krankheiten siehe dort.
Befundproblematik
Problematisch ist die Definition eines Grenzwertes, um die bestmögliche Unterscheidung zwischen gut- und bösartiger Veränderung der Prostata zu ermöglichen. Bei den meisten Testsystemen hat sich ein Wert von 4 ng/ml etabliert, Werte unter 4 ng/ml schließen ein Prostatakarzinom aber nicht aus – ein beträchtlicher Teil der organbegrenzten Tumore wird bei diesem Cut-off-Wert übersehen. Bei Werten über 10 ng/ml wird nur noch ein Drittel der Tumore in einem organbegrenzten Stadium diagnostiziert. Verschiedene Testsysteme sind auf dem Markt. Es sollten immer nur Werte, die mit dem gleichen Testsystem bestimmt worden sind, verglichen werden. Der positive prädiktive Wert, das heißt, die Sicherheit, das Prostatakarzinom tatsächlich vorherzusagen, liegt bei PSA-Werten zwischen 4 ng/ml und 10 ng/ml bei 25–35 %, bei Werten über 10 ng/ml bei 50–80 %. Der Tastbefund - der als digital-rektale Untersuchung der Prostata bezeichnet wird - weist in der Screeningpopulation in 1,45 bis 3,3 % der Fälle die Krebserkrankung nach, die Erkennungsrate des Prostatakarzinoms mittels PSA-Bestimmung innerhalb der Screeningpopulation liegt bei 4,6 %. Werden beide Methoden kombiniert, steigt die Erkennungsrate auf 5,8 %. Erwähnenswert ist in diesem Zusammenhang, dass auch der erfahrene Untersucher Karzinome erst ab einer Größe von 7 mm digital-rektal tasten kann.
Folgende Probleme werden diskutiert:
- Der Grenzwert, der zu einer weitergehenden Abklärung führen soll, wird mit 4,0 ng/ml angegeben, da darunter zu viele (letztlich sinnlose) Abklärungen aufgrund falsch positiver Befunde durchgeführt werden müssten. Denn das PSA ist zwar ein organspezifischer Marker, allerdings nicht krankheitsspezifisch. Das heißt, dass er beinahe ausschließlich auf eine Erkrankung der Prostata hinweist, allerdings auch bei der gutartigen, sogenannten benignen Prostatahyperplasie ebenso erhöht sein kann wie bei einer Entzündung, der sogenannten Prostatitis oder dem (selteneren) Prostatainfarkt. Mit der Einführung dieses Grenzwertes wurden somit die falsch-positiven Befundergebnisse wesentlich eingeschränkt, aber immer noch nicht ausgeschlossen.
- Andererseits haben 20 % der Patienten bei der Erstdiagnose eines Prostatakarzinoms ein PSA unter 4 ng/ml, wobei ca. 40 % dieser Karzinome einen Gleason-Score über 6 aufweisen und damit als besonders aggressiv einzuschätzen sind.
- Demnach kann man feststellen, wer Prostata-Krebs hat und wer nicht. Man kann jedoch nicht mit Sicherheit sagen, wer am Karzinom wirklich erkrankt. In diesem Bereich wird noch intensiv geforscht.
Einführung des freien PSA
Die Anstrengungen, die Aussagekraft des PSA-Screenings zu erhöhen, führten schließlich dazu, dass heute das freie PSA in die Untersuchungsroutine miteinbezogen wird: PSA ist im Blut als freies (fPSA) und als gebundenes PSA (komplexiertes PSA oder cPSA) nachweisbar; beide zusammen werden als das Gesamt-PSA (totales PSA oder tPSA) gemessen. Dieses alleine besitzt aus den oben angegebenen Gründen eine unzureichende diagnostische Aussagekraft. Der Quotient aus freiem und gebundenem PSA erhöht jedoch die Spezifität, das heißt die krankheitsspezifische Trefferquote - vor allem im Grenzbereich zwischen 4,0 und 10,0 ng/ml - da der Anteil des freien PSA bei Vorliegen eines Prostatakarzinoms kleiner ist. Je niedriger somit diese Verhältniszahl, umso höher die Wahrscheinlichkeit für das Vorliegen eines Prostatakarzinoms. Es sind derzeit (April 2005) mehr als 100 Testsysteme für PSA/FPSA auf dem Markt. Jedes Testsystem hat seinen eigenen Grenzwert für den PSA-Quotienten bei gleicher Sensitivität und Spezifität für die Entdeckung oder den Ausschluss eines Prostatakrebses.
Beispiel freies PSA
- PSA 3,9 ng/ml
- freies PSA 1,0 ng/ml
- Quotient freies PSA / Gesamt PSA 25,6 %
- Interpretation: der Quotient > 20 % spricht eher für benigne (gutartige) Prostataveränderung.
- Quotient freies PSA / Gesamt PSA 25,6 %
Weitere Verfahren zur Verbesserung der Aussagekraft des PSA
Mit Hilfe von altersabhängigen Grenzwerten, wobei etwas niedrigere Grenzwerte für jüngere Patienten gelten und etwas höhere für ältere Patienten, können unnötige Stanzbiopsien vermindert werden. Weitere Möglichkeiten sind die Beachtung der PSA-Dichte (PSA-Konzentration in Abhängigkeit des Prostatavolumens) und der PSA-Velocity (Anstiegsgeschwindigkeit des PSA) [7]
PSA-Messung zur Verlaufskontrolle
Ganz anders sieht es bezüglich der Wertigkeit des PSA zur Verlaufskontrolle nach erfolgter Therapie eines Prostatakarzinoms aus: Die Einführung der PSA-Bestimmung hat alle anderen Verfahren zur Rezidivsuche verdrängt.
- Ein Abfall erhöhter Werte in den Referenzbereich weist auf eine Remission der Erkrankung. Nach radikaler Prostataektomie gelten Patienten mit PSA-Werten unter der Messgrenze als rezidivfrei. Die PSA-Kontrollen sollten im ersten Jahr alle drei Monate, danach für weitere vier Jahre im halbjährlichen Abstand erfolgen.
- Im Anschluss an eine Strahlentherapie der Prostata kann es zu einem (oder mehrmaligen) vorübergehenden Anstieg des PSA ein bis fünf Jahre nach der Behandlung kommen, dessen Ursache bislang nicht verstanden wird, und der als PSA-bounce bezeichnet wird.
- Im Falle einer primären hormonellen Behandlung des Prostatakarzinoms erlauben die PSA-Werte innerhalb des ersten Halbjahres eine Beurteilung des Erfolgs. Die Kontrollen sollten entsprechend engmaschig weitergeführt werden, um nach einem eventuellen Wiederanstieg individuelle Behandlungsstrategien entwickeln zu können.
Eine Tumorprogression nach Therapie ohne PSA-Anstieg ist äußerst selten. Der Anstieg selbst geht der klinischen Manifestation eines Rezidivs in der Regel um Jahre voraus. Nach radikaler Prostataentfernung beträgt die Zeit vom Beginn des PSA-Anstieges bis zur Bildung von Metastasen mit Beschwerden durchschnittlich 8 Jahre.[8]
Kosten und Kostentragung
Aufgrund der oben beschriebenen, geringen Sicherheit des PSA-Tests ist der PSA-Test bei Gesunden keine Leistung der gesetzlichen Krankenkassen zur Krankheitsfrüherkennung. Bei Männern, die an Prostatakrebs erkrankt sind, ist die Verlaufskontrolle mit Hilfe des PSA-Tests sinnvoll und wird von der Krankenkasse bezahlt.
Einzelnachweise
- ↑ Wang MC et al.: Purification of a human prostato specific antigen. Investig Urol (Berl) 17/2/1979. S. 159–163. PMID 89106
- ↑ OMIM-Eintrag
- ↑ ENSEMBL-Eintrag
- ↑ http://www.prostatakrebs-bps.de/psascreening.html
- ↑ http://science.orf.at/science/news/94778
- ↑ Hanks GE, Scardino PT: Does screening for prostate cancer make sense? Sci Am 275/3/1996 S. 114-5. PMID 8701279
- ↑ Manski, D.: www.urologielehrbuch.de http://www.urologielehrbuch.de/tumormarker_psa.html
- ↑ Manski, D.: www.urologielehrbuch.de http://www.urologielehrbuch.de/prostatakarzinom_06.html
- Weymayr C, Koch K. Mythos Krebsvorsorge. Schaden und Nutzen der Früherkennung. Eichborn, 296 Seiten. ISBN 3-8218-3950-3
- Hanlon AL, Pinover WH, Horwitz EM, Hanks GE. Patterns and fate of PSA bouncing following 3D-CRT. Int J Radiat Oncol Biol Phys. 2001 Jul 15;50(4):845-9. PMID 11429210
- Whittemore AS,Lele C,Friedman GD,Stamey T, Vogelman JH, Orentreich N (1995) PSA as predictor of prostate cancer in black men and white men.J Natl Cancer Inst 87:354–360
- Kleer E,Oesterling, JE (1993) PSA and staging of localized prostate cancer.Urol Clin North Am 20: 695–705
- Catalona WJ (1994) Screening for prostate cancer. Lancet 343:1437
- Schmelz HU, Leyh H: Facharztprüfung Urologie. 1000 kommentierte Prüfungsfragen. Thieme Verlag Stuttgart New York 2004
Weblinks
- http://www.psa-entscheidungshilfe.de (Info der AOK und des DKFZ)
- Leitlinie zur PSA-Bestimmung in der Früherkennung des Prostatakarzinoms (PDF)
- "Früherkennung von Prostatakrebs: Schaden ja, Nutzen nein" (Literaturübersicht)
- Molekulare Formen des PSA in der Diagnostik des Prostatakarzinoms - mit Editorial
- NEJM (englisch)
- Stellungnahme des DNEbM zum PSA-Screening (PDF)
- Laborlexikon.de
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.