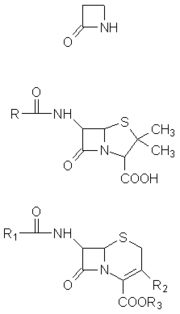
- Beta-Lactam-Antibiotikum
-
Die β-Lactam-Antibiotika sind eine Gruppe von Antibiotika/antibakteriellen Antiinfektiva, die alle in ihrer Strukturformel einen viergliedrigen Lactam-Ring aufweisen. Sie gehen auf das Penicillin zurück, das der englische Bakteriologe Alexander Fleming 1928 aus Kulturen des Schimmelpilzes Penicillium notatum extrahierte, welches zugleich den wichtigsten und bekanntesten Vertreter dieser Gruppe darstellt. Sie wirken alle bakterizid, indem sie die Peptidoglykansynthese bei der Zellteilung hemmen. Unterschiede in der Wirksamkeit begründen sich vor allem durch differente Affinität und Penetrationsfähigkeit. β-Lactam-Antibiotika werden heutzutage überwiegend halbsynthetisch erzeugt.
Um 1940 entwickelten Howard Walter Florey und Ernst Boris Chain Medikamente auf Basis des Penicillins, welche ein Jahr später zum ersten mal therapeutisch eingesetzt wurden. Dafür erhielt Fleming 1945, gemeinsam mit den zwei anderen Wissenschaftlern, den Nobelpreis für Medizin. Damals wurden Penicillinpräparate häufig falsch eingesetzt, besonders auch gegen Krankheitserreger, die von Natur aus gegen β-Lactam-Antibiotika resistent sind. Inzwischen haben viele ursprünglich empfindliche Krankheitserreger eine Antibiotikum-Resistenz gegen β-Lactampräparate entwickelt, so dass ständig der Zwang zur Entwicklung neuer Medikamente besteht.
Inhaltsverzeichnis
Nebenwirkungen
β-Lactam-Antibiotika sind in der Regel für den Menschen gut verträglich, was auf den Wirkungsmechanismus zurückzuführen ist. Sie greifen in die Zellwandsynthese von sich teilenden Bakterien ein - dieser Stoffwechselvorgang kommt beim Menschen nicht vor. Jedoch existieren inzwischen viele Allergien gegen Penicillin und verwandte Substanzen, die von leichten Hautreaktionen bis zum anaphylaktischen Schock in allen Schweregraden reichen können. Auch muss mit Kreuzallergien zwischen den einzelnen β-Lactam-Antibiotika gerechnet werden.
Einteilung in Gruppen
Man unterscheidet heute vier Gruppen von β-Lactam-Antibiotika:
- Penicilline
- β-Lactamase-sensitive (-instabile) Penicilline
- Benzylpenicillin (Penicillin G)
- Phenoxymethylpenicillin (Penicillin V)
- Propicillin
- Azidocillin
- β-Lactamase-resistente (-stabile) Penicilline
- Flucloxacillin
- Dicloxacillin
- Oxacillin
- Methicillin
- Breitbandpenicilline
- Amoxicillin
- Ampicillin
- Bacampicillin
- Mezlocillin
- Piperacillin
- β-Lactamase-sensitive (-instabile) Penicilline
- Cephalosporine
- Cephalosporine zur parenteralen Anwendung
- Cephalosporine ohne erhöhte β-Lactamase-Stabilität
- Basiscephalosporine
- Cephalosporine mit erhöhter β-Lactamase-Stabilität
- Cefuroxim
- Cefamandol
- Cefoxitin
- Cefotiam
- Breitspektrumcephalosporine
- Cefotaxim
- Cefovecin
- Ceftazidim
- Cefepim
- Cefodizim
- Ceftriaxon
- Cephalosporine ohne erhöhte β-Lactamase-Stabilität
- Oralcephalosporine
- Oralcephalosporine ohne erhöhte β-Lactamase-Stabilität
- Cefaclor
- Cefadroxil
- Cefalexin
- Loracarbef
- Oralcephalosporine mit erhöhter β-Lactamase-Stabilität
- Cefixim
- Cefuroximaxetil
- Cefetametpivoxil
- Ceftibuten
- Cefpodoximproxetil
- Oralcephalosporine ohne erhöhte β-Lactamase-Stabilität
- Cephalosporine zur parenteralen Anwendung
- β-Lactamase-Inhibitoren
- Clavulansäure in Kombination mit Amoxicillin (Bsp.: Augmentan®)
- Sulbactam
- Tazobactam in Kombination mit Piperacillin (Bsp.: Tazobac®)
- Sonstige β-Lactam-Antibiotika
- Carbapeneme
- Monobactame
- Aztreonam
Resistenzen
Während der Anwendung von β-Lactam-Präparaten entwickeln sich zwar nur selten und langsam Resistenzen gegen dieselben, jedoch stellen sie inzwischen ein ernsthaftes Problem dar. Hierbei sind drei Resistenzmechanismen zu unterscheiden:
- unempfindliche Penicillin-Bindeproteine
- Membranveränderungen
- Bildung von β-Lactamasen
- Hierbei bilden die Bakterien Enzyme, die den β-Lactam-Ring der Antibiotika öffnen und diese damit inaktivieren. Die genetische Information hierfür wird chromosomal oder plasmidal vererbt. Je nach ihrer Wirkung werden die β-Lactamasen als Penicillinasen oder Cephalosporinasen bezeichnet.
Um β-Lactamase-stabile Penicilline zu erhalten werden voluminöse Gruppen in das Penicillinmolekül eingeführt, die die β-Lactamase sterisch behindern. Ebenfalls möglich ist die Anwendung von β-Lactamase-Hemmstoffen, wie Clavulansäure, Sulbactam oder Tazobactam.
β-Lactam-Antibiotika blockieren nicht nur die Teilung von Bakterien, inklusive der Cyanobakterien, sondern auch die Teilung der Cyanellen, der photosynthetisch aktiven Organellen der Glaucocystaceae, sowie der Chloroplasten von Blasenmützenmoosen[1] , Lebermoose (Marchantia polymorpha[2]) und Moosfarne (Selaginella nipponica[3]). Auf die Teilung der Plastiden der höher entwickelten Gefäßpflanzen wie beispielswiese bei Tomaten haben sie jedoch keinen Effekt. Dies ist ein Hinweis darauf, dass bei höheren Pflanzen durch erfolgte, evolutionäre Veränderungen der Plastidteilung β-Lactam-Antibiotika auf Chloroplasten keine Wirkung mehr zeigen.[1]
Literatur
- Claus Simon, Wolfgang Stille: Antibiotika-Therapie in Klinik und Praxis. 10. Auflage. Schattauer, Stuttgart 2001, ISBN 3-7945-1970-1
- Peter Imming: Wie macht der Pilz das Penicillin? Aktuelle Forschung, Trends bei β-Lactam-Antibiotika. Biosynthese der Penicilline und Cephalosporine. Pharmazie in unserer Zeit 18(1), S. 20 – 24 (1989), ISSN 0048-3664
Einzelnachweise
- ↑ a b Kasten, B. und Reski, R. (1997): β-lactam antibiotics inhibit chloroplast division in a moss (Physcomitrella patens but not in tomato (Lycopersicon esculentum). In: J. Plant Physiol. 150, 137–140; PDF (freier Volltextzugriff, engl.)
- ↑ Tounou, E. et al. (2002): Ampicillin Inhibits Chloroplast Division in Cultured Cells of the Liverwort Marchantia polymorpha. In: Cytologia 67; 429–434; doi:10.1508/cytologia.67.429
- ↑ Izumi, Y. et al. (2003): Inhibition of plastid division by ampicillin in the pteridophyte Selaginella nipponica Fr. et Sav. In: Plant Cell Physiol. 44(2):183–189; PMID 12610221; PDF (freier Volltextzugriff, engl.)
Bitte beachte den Hinweis zu Gesundheitsthemen! - Penicilline
Wikimedia Foundation.