- Chlorameisensäurebenzylester
-
Strukturformel 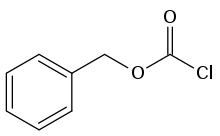
Allgemeines Name Chlorameisensäurebenzylester Andere Namen - Benzylchlorformiat
- Benzyloxycarbonylchlorid
- Z-Chlorid
- CAB
Summenformel C8H7ClO2 CAS-Nummer 501-53-1 Kurzbeschreibung farblose, stechend riechende Flüssigkeit[1]
Eigenschaften Molare Masse 170,60 g·mol−1 Aggregatzustand flüssig
Dichte 1,20 g·cm−3[2]
Schmelzpunkt Siedepunkt 179 °C[2]
Dampfdruck Löslichkeit - heftige Zersetzung mit Wasser[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [3] 

Gefahr
H- und P-Sätze H: 314-410 EUH: keine EUH-Sätze P: 273-501 [2] EU-Gefahrstoffkennzeichnung [2] 

Ätzend Umwelt-
gefährlich(C) (N) R- und S-Sätze R: 34-50/53 S: (1/2)-26-45-60-61 MAK Für (potentiell) krebserzeugende Stoffe wird generell kein MAK-Wert vergeben[4]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Chlorameisensäurebenzylester, auch Benzylchlorformiat, oft auch korrekter als Chlorkohlensäurebenzylester bezeichnet, ist eine organisch-chemische Substanz. Es gehört als Monoester der Kohlensäure zugleich zu der Stoffgruppe der Carbonsäurechloride. Bei der Synthese von Peptiden dient Benzylchlorformiat als Reagenz zur Einführung der Benzyloxycarbonyl-Schutzgruppe, die meist zum Schutz für Aminogruppen eingesetzt wird.
Inhaltsverzeichnis
Eigenschaften
Benzylchlorformiat ist eine stechend und erstickend riechende, tränenreizende Flüssigkeit. Sie ist in den meisten organischen Lösungsmitteln löslich, wird aber durch protische Lösungsmittel wie Wasser oder Alkohole solvolytisch zersetzt. Mit Alkoholen bilden sich Kohlensäureester. Mit Aminen reagiert Benzylchlorformiat zu Urethanen.
Verwendung
In der organischen Synthesechemie und besonders in der Peptidsynthese wird die Benzyloxycarbonylgruppe mit Benzylchlorformiat in Gegenwart einer schwachen Base eingeführt. Die Benzyloxycarbonylgruppe wird in Strukturformeln meist als Cbz-, Cbo-, oder Z-Gruppe (benannt nach dem Entdecker, Leonidas Zervas) abgekürzt.
Das geschützte Amin kann durch katalytische Hydrierung unter hydrogenolytischer Spaltung der Benzyl-Heteroatom-Bindung mit anschließender Decarboxylierung der so entstehenden instabilen Carbaminsäure oder Behandlung mit Säuren wieder entschützt werden.
Nomenklatur
Der gebräuchliche Name „Chlorameisensäurebenzylester“ ist nicht ganz korrekt, da es sich genau genommen um ein Derivat der Kohlensäure handelt, nicht um ein Derivat der Ameisensäure. Genau genommen handelt es sich hier um ein Monochlorid und zugleich den Monobenzylester der Kohlensäure.
Gefahrenhinweise
Da sich Benzylchlorformiat durch Luftfeuchtigkeit und auf der Haut hydrolytisch unter Bildung von Salzsäure zersetzt, wirkt es bei Kontakt stark ätzend. Eingeatmet kann es zu Lungenödemen führen.
Kommerziell erhältliches Benzylchlorformiat enthält herstellungsbedingt das als krebserregend eingestufte Benzylchlorid als Verunreinigung. Einige Hersteller, beispielsweise die Merck KGaA, bezeichnen daher auch das Benzylchlorformiat als krebserregend und geben neben den Gefahrstoffsymbolen T (giftig) und N (umweltgefährlich) die R-Sätze 45-34-50/53 und die S-Sätze 53-26-36/37/39-45-60-61 an.[1]
Siehe auch
- Alloc (Allyloxycarbonyl-Gruppe)
Literatur
- J. Clayden, N. Greeves, S. Warren, P. Wothers: Organic Chemistry. Oxford University Press, 2001
Einzelnachweise
- ↑ a b Datenblatt Chlorameisensäurebenzylester bei Merck, abgerufen am 19. Januar 2011.
- ↑ a b c d e f g Eintrag zu CAS-Nr. 501-53-1 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 16. September 2007 (JavaScript erforderlich).
- ↑ Eintrag zu CAS-Nr. 501-53-1 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ "Grenzwerte am Arbeitsplatz", Maximale Arbeitsplatz-Konzentrationswerte (MAK-Werte), Biologische Arbeitsstoff-Toleranzwerte (BAT-Werte) und Grenzwerte für physikalische Einwirkungen. Periodisch publiziert von SUVA.ch. PDF-Datei 2011.
Kategorien:- Ätzender Stoff
- Umweltgefährlicher Stoff
- Krebserzeugender Stoff
- Carbonsäurechlorid
- Kohlensäureester
- Aromat
Wikimedia Foundation.
