- Fumarsäure
-
Strukturformel 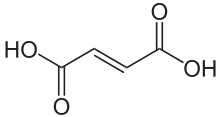
Allgemeines Name Fumarsäure Andere Namen - trans-Butendisäure
- trans-Ethylendicarbonsäure
- (E)-Butendisäure
- E 297
Summenformel C4H4O4 CAS-Nummer 110-17-8 PubChem 723 ATC-Code D05AX01
Kurzbeschreibung weiße, fast geruchlose Kristalle[1]
Eigenschaften Molare Masse 116,07 g·mol−1 Aggregatzustand fest
Dichte 1,64 g·cm−3[1]
Sublimationspunkt 200 °C[1]
Dampfdruck pKs-Wert Löslichkeit schlecht in Wasser (4,9 g·l−1)[1]
Sicherheitshinweise Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [3] 
Achtung
H- und P-Sätze H: 319 EUH: keine EUH-Sätze P: 305+351+338 [1] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [3] 
Reizend (Xi) R- und S-Sätze R: 36 S: (2)-26 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Fumarsäure ist der Trivialname einer in der Natur vorkommenden organisch-chemischen Substanz. Es ist eine ungesättigte Dicarbonsäure mit dem IUPAC-Namen trans-Butendisäure, auch trans-Ethylendicarbonsäure genannt. Ihre Salze heißen Fumarate. Die isomere cis-Form heißt Maleinsäure.
Inhaltsverzeichnis
Geschichte
Im Jahre 1937 erhielt Albert Szent-Györgyi den Medizin-Nobelpreis für seine biochemischen Arbeiten unter anderem auch zur Fumarsäure.
Vorkommen und Herstellung
Fumarsäure kommt in größeren Mengen in verschiedenen Pflanzen, Pilzen und Flechten vor. Ihren Namen erhielt sie vom Gewöhnlichen Erdrauch (Fumaria officinalis), der größere Mengen der Säure enthält. Synthetisch wird Fumarsäure durch Isomerisierung aus Maleinsäure hergestellt; dies geschieht durch Erhitzen auf über 150 °C, durch UV-Bestrahlung oder katalytisch in wässriger Lösung.
Sie entsteht in allen Organismen (z.B. in mehreren Gattungen der Mucorales) auf verschiedenen biochemischen Stoffwechselwegen:
- als Zwischenprodukt im Citratzyklus durch Oxidation der Bernsteinsäure in Gegenwart des Enzyms Succinatdehydrogenase (einer Lyase);
- im Harnstoffzyklus durch Spaltung der Argininbernsteinsäure;
- in der Biosynthese von Purinnukleotiden (aus Aspartat);
- im Nukleotidstoffwechsel bei der Darstellung von Adenosinmonophosphat aus Inosinmonophosphat;
- durch hydrolytischen Abbau von Aminosäuren wie Phenylalanin, Tyrosin
- durch Desaminierung von Asparaginsäure
Eigenschaften
Fumarsäure hat unter Normaldruck keinen Schmelzpunkt, sondern sublimiert ab etwa 287 °C. Sie bildet bei Raumtemperatur weiße, fast geruchlose, brennbare Kristalle. Die wässrige Lösung reagiert stark sauer: 1 l Wasser mit darin gelösten 4,9 g Furmarsäure besitzt einen pH-Wert von 2,1.[1] Die zweiprotonige Säure besitzt einen pKs1 von 3,0 und einen pKs2 von 4,5.[2]
Verwendung
Fumarsäure ist als Lebensmittelzusatzstoff E 297 zugelassen und dient als Säuerungsmittel. In der Synthesechemie wird es für die Polyester-Herstellung verwendet; in der Biotechnologie wird Ammoniak stereoselektiv an die Kohlenstoff-Kohlenstoff-Doppelbindung angelagert, es bildet sich enzymkatalysiert L-Asparaginsäure; viele – insbesondere aminogruppenhaltige – pharmazeutisch wirksame Substanzen werden als Salze der Fumarsäure verabreicht; in der Medizin werden Fumarsäureester wie Fumarsäuredimethylester und Fumarsäuremonoethylester zur Behandlung der Schuppenflechte eingesetzt. Studien deuten außerdem auf ihre Eignung zur Behandlung von Patienten mit Multipler Sklerose hin.[4][5] In der Schweineaufzucht wird Fumarsäure als Futterzusatz für Ferkel genutzt um damit den pH-Wert im Darm aufrechtzuerhalten und colibedingten Infektionen vorzubeugen.
Weblinks
Einzelnachweise
- ↑ a b c d e f g Eintrag zu CAS-Nr. 110-17-8 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Juni 2007 (JavaScript erforderlich).
- ↑ a b c A. Reichert: Potentiometrische Titrationen in Theorie und Praxis.
- ↑ a b Eintrag zu CAS-Nr. 110-17-8 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ "Tabletten statt Spritzen: Fumarsäure hilft bei Multipler Sklerose" von dmsg.de - abgerufen am 08. November 2011.
- ↑ Kappos L, Gold R, Miller DH et al. Efficacy and safety of oral fumarate in patients with relapsing-remitting multiple sclerosis: a multicentre, randomised, double-blind, placebo-controlled phase IIb study. Lancet. 2008; 372: S. 1463–1472; PMID 18970976.

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- ATC-D05
- Reizender Stoff
- Alken
- Arzneistoff
- Alkensäure
- Dicarbonsäure
- Säuerungsmittel
- Stoffwechselintermediat
Wikimedia Foundation.
