- Glycerole
-
Strukturformel 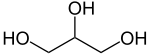
Allgemeines Name Glycerin Andere Namen - Glycerol
- 1,2,3-Propantriol
- Propantriol
Summenformel C3H8O3 CAS-Nummer 56-81-5 ATC-Code Kurzbeschreibung farblose, süßlich schmeckende viskose Flüssigkeit Eigenschaften Molare Masse 92,10 g·mol–1 Aggregatzustand flüssig
Dichte 1,26 g·cm–3 (20 °C)[1]
Schmelzpunkt 18 °C[1]
Siedepunkt 290 °C (unter Zersetzung)[1]
Dampfdruck Löslichkeit mischbar mit Wasser[1], gut löslich in Ethanol, schlecht in unpolaren Lösungsmitteln
Sicherheitshinweise Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln MAK 50 mg·m–3[1]
LD50 4090 mg·kg–1 (Maus, oral) [2]
WGK 1[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Glycerin (nach IUPAC Glycerol, auch Glyzerin) ist der Trivialname und die gebräuchliche Bezeichnung von Propantriol bzw. Propan-1,2,3-triol und stellt einen dreiwertigen Alkohol dar. Der Name Glycerol wurde eingeführt, da er die korrekte Endung -ol für einen Alkohol besitzt (die Endung -in steht für Alkine).
Inhaltsverzeichnis
Physikalische Eigenschaften
Glycerin ist bei Raumtemperatur eine farb- und geruchlose, viskose und hygroskopische Flüssigkeit, die süßlich schmeckt. Sein süßer Geschmack führte auch zu seinem Namen, der von gr. glykeros = süß herrührt. Die Herkunft von Glycerin kann unterschiedlich sein: petrochemisch oder aus natürlichen Fetten.
Glycerin hat eine Viskosität von 1760 mPa·s (20 °C) und einen Brechungsindex
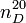 von 1,4735 (lit.). Die Bildungsenthalpie von Glycerin ist: ΔHf0 = −669 kJ/mol
von 1,4735 (lit.). Die Bildungsenthalpie von Glycerin ist: ΔHf0 = −669 kJ/molVerwendung
Glycerin ist eine sehr vielseitig verwendbare Substanz. Unter anderem ist der wasserbindende (hygroskopische) Stoff in Kosmetikartikeln als Feuchtigkeitsspender enthalten. Glycerin kann auch als Frostschutzmittel, Schmierstoff, Weichmacher und Süßungsmittel verwendet werden. Bei der Herstellung von Kunststoffen, Microchips, Farbstoffen sowie Zahnpasta wird die Substanz als Edukt benötigt.
Glycerin wird in der Medizin in Form von Tabletten oder Infusionen als Medikament zur Behandlung des Hirnödems eingesetzt. In Form glycerinhaltiger Zäpfchen dient es als osmotisches Laxans im Enddarm; zusätzlich weicht es den Stuhl als Flüssigkeit selber auf.
Es gibt Forschungen, die auf die Verwendung von Glycerin als "Frostschutzmittel" im menschlichen Körper hinzielen; dies könnte zur Hibernation während schwieriger medizinischer Operationen verwendet werden, um Hirn- und Organschäden zu vermeiden. Inspiration für diese Forschungen ist der kanadische graue Laubfrosch, der diese Methode zur Überwinterung nutzt.
Auch als Lebensmittelzusatzstoff findet Glycerin Anwendung als Feuchthaltemittel, etwa bei Datteln oder Kaugummi. Hier trägt das Triol die Bezeichnung E 422.
Bei der Reaktion mit konzentrierter Salpetersäure und konzentrierter Schwefelsäure entsteht Glyceroltrinitrat, ein gefährlicher, als Nitroglyzerin bekannter Explosivstoff, der zu dem Sprengstoff Dynamit weiterverarbeitet werden kann.
Shisha-Tabak wird oft nachträglich Glycerin beigegeben, um ihn feucht zu halten oder um ihm die ursprüngliche Feuchtigkeit zurückzugeben. Dabei entsteht mehr und dichterer Rauch.
Glycerin bildet unter Hitzeeinwirkung weißen Rauch. Beim Erhitzen unter Sauerstoffmangel zersetzt es sich zu dem in Wasser gut (267 g/l) löslichen sowie giftigen ungesättigten Aldehyd Propenal, das auch Acrylaldehyd oder Acrolein genannt wird.
Aufgrund der zeitweise deutlich gesunkenen Preise werden neue Anwendungsgebiete für Glycerin gesucht. Neben der Verbrennung zur Energieerzeugung ist dabei insbesondere die Nutzung als zusätzliches Nährmedium (Cosubstrat) in Biogasanlagen zur Erzeugung von Biogas eine vielversprechende Alternative. Bei hohen Futtermittelpreisen findet Glycerin auch als Futtermittel für Kühe und Schweine immer mehr Interesse. Weiterhin wird erforscht, Glycerin mit Isobuten zu Glycerin-tert.-Butylether (GTBE; analog zu MTBE) umzusetzen und als Kraftstoffzusatzstoff zu verwenden.[3]
Herstellung
Die Herstellung kann petrochemisch durch Hydrolyse von Epichlorhydrin oder als Nebenprodukt bei der Verseifung von natürlichen Fetten und Ölen zur Gewinnung von Fettsäuren geschehen. Früher wurden aus tierischen Fetten in großen Mengen Seifen (= Alkalisalze der Fettsäuren) produziert. Inzwischen hat die Biodieselherstellung (= katalysierte Umesterung von meist pflanzlichen Ölen mit Methanol) erheblich an Bedeutung gewonnen; auch hierbei wird Glycerin freigesetzt.
Neben 99,5 %igem, auch Pharmagrade genanntem, Glycerin ist noch eine ca. 85 %ige Qualität (ca. 15 % Wasser) erhältlich; letztere ist wegen ihres geringeren Schmelzpunkts (ca. −10 °C) und der niedrigeren Viskosität (ca. 100 mPas) technisch erheblich einfacher zu handhaben.
Hefen können durch Sulfitzusatz die Gärung von Alkoholbildung auf Glycerinbildung umstellen. Als Substrat wurde oftmals Melasse verwendet, da diese viel Sulfit enthält. Diese Form der Gärung wurde 1918 von Neuberg als 2. Neuberg'sche Gärungsform bezeichnet.
Biologische Bedeutung
Glycerin steckt als Grundgerüst in allen Fetten (Triglyceride). In diesem Fall ist der dreiwertige Alkohol Glycerin dreifach mit Fettsäuren verestert. Auch viele andere Andere Lipide - wie Phosphoglyceride - sind Glycerinester, wobei hier jedoch statt der dritten Fettsäure über eine Phosphatgruppe ein anderer Alkohol im Molekül enthalten ist.
Nahezu alle natürlich vorkommenden Glycerinderivate weisen die sn-Konfiguration auf, welche die räumliche Anordnung der Substituenten am mittleren Kohlenstoffatom des Glycerins festlegt.[4]
Einzelnachweise
- ↑ a b c d e f g h Eintrag zu CAS-Nr. 56-81-5 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 29. September 2006 (JavaScript erforderlich)
- ↑ Glycerin bei ChemIDplus
- ↑ Entwicklung von GTBE aus Glycerin; Bericht im Innovationsreport
- ↑ Gregor Cevc: Phospholipids Handbook. CRC Press, 1993, ISBN 9780824790509, S. 2
Weblinks
Wikimedia Foundation.
