- Kiel-Klassifikation
-
Klassifikation nach ICD-10 C82 Follikuläres (noduläres) Non-Hodgkin-Lymphom C83 Diffuses Non-Hodgkin-Lymphom C84 Periphere und kutane T-Zell-Lymphome C85 Sonstige und nicht näher bezeichnete Typen des Non-Hodgkin-Lymphoms ICD-10 online (WHO-Version 2006) Unter dem Sammelbegriff Non-Hodgkin-Lymphome (NHL) werden alle malignen Lymphome zusammengefasst, die nicht die Diagnosekriterien des Morbus Hodgkin erfüllen. Diese Zusammenfassung hat im wesentlichen historische Gründe. Die Erkrankungen, die unter diesem Oberbegriff zusammengefasst werden, sind sehr heterogen. Das gilt sowohl für die zugrundeliegenden genetischen Veränderungen, die immunologischen Charakteristika als auch die klinischen Erscheinungsformen. Dementsprechend sieht auch die Behandlung der NHL sehr unterschiedlich aus. Die NHL werden in eine B- (ca 80 % aller NHL) und eine T-Klasse (20 %) unterteilt, je nachdem, ob das NHL von B-lymphatischen oder T-lymphatischen Zellen ausgeht.
Inhaltsverzeichnis
Ursachen
Grundsätzlich lässt sich sagen, dass einem NHL immer die ungehemmte Teilung von Lymphozyten bei gleichzeitigem Ausbleiben der Apoptose der überzähligen Zellen zu Grunde liegt. Die Folge ist, dass die Masse und Zahl der entsprechenden Lymphozyten immer mehr zunimmt und somit andere Zellen verdrängt werden.
Die Pathogenese der Non-Hodgkin-Lymphome ist bisher nicht vollständig verstanden. Als angeborener Gendefekt tritt das NHL vor allem beim Wiskott-Aldrich-Syndrom auf. Beim Großteil der Erkrankungsfälle sind jedoch erworbene genetische Veränderungen entscheidend für die Entstehung des Lymphoms, vererbt werden kann das NHL in diesen Fällen nicht. Es gibt jedoch einige Risikofaktoren, die eine genetische Prädisposition ergänzen und somit ein Lymphom in seiner Entstehung begünstigen können. Hierzu zählen beispielsweise Strahlenexposition durch ionisierende Röntgen- oder Gammastrahlung oder eine früher erfolgte Zytostatika-Therapie (z. B. im Rahmen der Behandlung einer anderen malignen Erkrankung). Auch eine Autoimmunerkrankung (z. B. Sjögren-Syndrom) oder Infektion mit HIV kann die Entstehung eines NHL begünstigen.
Außerdem gibt es Viren und Bakterien, die die Entstehung eines NHL begünstigen (s.u.).
Genetische Veränderungen
Mittlerweile sind eine Vielzahl von genetischen Veränderungen identifiziert worden, die teilweise von diagnostischer Bedeutung sind, wenn um die genaue Klassifikation des NHL geht. Typisch sind bestimmte Chromosomentranslokationen:
- t(8;14)(q24;q32) – typischerweise bei Burkitt-Lymphom, diffus-großzelligem B-NHL, selten Multiples Myelom
- t(11;14)(q13;q32) – typisch für das Mantelzelllymphom, gelegentlich Multiples Myelom oder chronische lymphatische Leukämie
- t(14;18)(q32;q21) – typisch für das follikuläre Lymphom
Durch diese Chromosomentranslokationen geraten bestimmte Onkogene außer Kontrolle, was einen entscheidenenden Schritt bei der malignen Transformation der betroffenen Zelle darstellt.
Onkogene Viren und Bakterien
Bei einigen NHL-Subtypen ist eine Beteiligung von bestimmten Viren und Bakterien an der Entstehung gesichert:
Viren:
- Epstein-Barr-Virus (EBV): (endemisches) Burkitt-Lymphom, aggressives T-/NK-Zell-Lymphom, lymphomatoide Granulomatose,
- Humanes T-Zell-lymphotropes Virus Typ I (HTLV-I): adultes (endemisches) T-Zell-Lymphom/Leukämie
- Humanes Herpesvirus 8 (HHV-8): Lymphom seröser Körperhöhlen (primary effusion lymphoma)
Bakterien:
- Helicobacter pylori (HP): Eine langjährige Infektion mit HP kann die Entstehung eines niedrig malignen NHL des lymphatischen Gewebes des Magens fördern (MALT-Lymphom).
Quantitativ machen diese Fälle jedoch nur einen relativ kleinen Teil aller NHL aus.
Umweltfaktoren
Eine Fallstudie aus Schweden legt nahe, dass Pestizide ein möglicher Auslöser für die Entwicklung des Non-Hodgkin-Lymphoms sein können.[1] Durch das Bundesministerium für Umwelt, Naturschutz und Reaktorsicherheit wurde eine epidemiologische Fall-Kontroll-Studie zur Ätiologie von Lymphomen in Auftrag gegeben.[2]
Epidemiologie
 Relative Häufigkeit der NHL[3]
Relative Häufigkeit der NHL[3]Die gegenwärtige Inzidenz liegt bei 5–10 Erkrankungsfällen auf 100.000 Einwohner pro Jahr – die Tendenz ist gegenwärtig steigend. Männer sind vom NHL in etwa 1,5 Mal öfter betroffen als Frauen. NHL können in jedem Lebensalter auftreten, insgesamt jedoch häufiger im höheren Lebensalter. AIDS-Patienten haben eine bis zu 1.000fach erhöhte Inzidenz an NHL.
Symptome
- meist nicht schmerzhafte („indolente“) Lymphknotenvergrößerungen („Lymphadenopathie“)
- Leistungsminderung, Müdigkeit
- evtl. sogenannte „B-Symptomatik“ ( Fieber >38 °C, Nachtschweiß, ungewollter Gewichtsverlust > 10 % in 6 Monaten)
- Infektneigung und Infektanfälligkeit
- Blutveränderungen (s. u.)
In den Blutuntersuchungen können sich folgende Veränderungen finden:
- Anämie
- Leukopenie oder auch Leukozytose (durch Lymphomzellen im Blut)
- Thrombopenie
- Entzündungszeichen (Blutsenkungsgeschwindigkeit erhöht, α2-Globuline und Fibrinogen erhöht)
- Eisen erniedrigt, Ferritin erhöht
- bei B-Zell-Lymphomen (Plasmozytom, Morbus Waldenström u. a.) u. U. monoklonale Gammopathie
- häufig Antikörpermangelsyndrom
- charakteristische Veränderungen von bestimmten Serumparametern:
- Lactatdehydrogenase (LDH) erhöht (bei schnell wachsenden NHL oder großer NHL-Tumormasse) oder bei begleitender hämolytischer Anämie
- β2-Mikroglobulin häufig aber nicht immer erhöht (Tumormarker für Lymphomerkrankungen)
Diagnose
Die Diagnose wird histologisch anhand der Biopsie eines betroffenen Lymphknotens gestellt. Neben der histomorphologischen Beurteilung werden spezielle Färbetechniken angewandt, um das gewonnene Biopsiematerial genau klassifizieren zu können. Die derzeit gültige WHO-Klassifikation hat die früher verwendete Kiel- bzw. REAL[4]-Klassifikationen weitestgehend abgelöst.
Für die genaue Stadieneinteilung sind weitere Untersuchungen notwendig:
- Röntgen Thorax
- Sonographie des Bauchraums
- CT von Hals, Thorax und Abdomen
- Knochenmarkpunktion zur Gewinnung der Knochenmarkhistologie und Ausschluss eines Knochenmarkbefalls
Eine genaue Klassifizierung und Stadieneinteilung ist für eine gezielte Therapie unerlässlich.
_-_07.jpg) Sonographie des Halses bei hoch-malignem Non-Hodgkin-Lymphom der Halslymphknoten (Transversalschnitt mit farbkodierter Duplexsonographie.
Sonographie des Halses bei hoch-malignem Non-Hodgkin-Lymphom der Halslymphknoten (Transversalschnitt mit farbkodierter Duplexsonographie.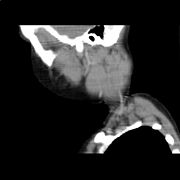 Computertomographie des Halses bei hoch-malignem Non-Hodgkin-Lymphom der Halslymphknoten (rekonstruierter Sagittalschnitt).
Computertomographie des Halses bei hoch-malignem Non-Hodgkin-Lymphom der Halslymphknoten (rekonstruierter Sagittalschnitt).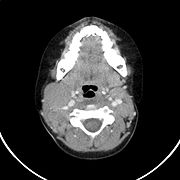 Computertomographie des Halses bei hoch-malignem Non-Hodgkin-Lymphom der Halslymphknoten (Transversalschnitt mit Kontrastmittel).
Computertomographie des Halses bei hoch-malignem Non-Hodgkin-Lymphom der Halslymphknoten (Transversalschnitt mit Kontrastmittel).Stadieneinteilung
Weltweit ist heute die Stadieneinteilung nach Ann Arbor, die 1971 in Ann Arbor, Michigan entwickelt wurde, in Gebrauch.
- Stadium I: Befall einer einzigen Lymphknotenregion ober- oder unterhalb des Zwerchfells
- Stadium II: Befall von zwei oder mehr Lymphknotenregionen ober- oder unterhalb des Zwerchfells
- Stadium III: Befall auf beiden Seiten des Zwerchfells
- Stadium IV: Befall von nicht primär lymphatischen Organen (z. B. Leber, Haut, Zentralnervensystem)
Zusatz A = keine Allgemeinsymptome (Fieber, Nachtschweiß, Gewichtsverlust), B = mit Allgemeinsymptomen, S = mit Milzbefall (die Milz wird in dieser Stadieneinteilung wie ein Lymphknoten behandelt), E = Befall außerhalb von Lymphknoten und Milz.
Therapie
Einige NHL können mittlerweile kurativ, d. h. mit Aussicht auf komplette Heilung behandelt werden. Die Heilungschancen hängen aber von vielen verschiedenen Faktoren ab, z. B. dem Typ des Lymphoms, dem Alter des Patienten, dem Stadium des Lymphoms (es erscheint einleuchtend, dass ein nur wenig ausgebreitetes Lymphom bessere Behandlungschancen bietet als ein schon generalisiertes), den Begleiterkrankungen des Patienten, etc. Als ganz groben Grundsatz kann man festhalten, dass hochmaligne (= schnell wachsende, aggressive) Lymphome sich gut chemotherapeutisch behandeln lassen und auch komplett geheilt werden können, während niedrig maligne (= langsam wachsende) Lymphome sich mit konventioneller Strahlentherapie/Chemotherapie i. d. R. nicht komplett heilen (aber häufig trotzdem gut behandeln) lassen. Der Grund für diese zunächst paradox erscheinende Tatsache liegt darin, dass hochmaligne Lymphome zwar sehr schnell wachsen, aber gerade dadurch sehr empfindlich gegenüber Behandlungsmodalitäten sind, die sich gegen schnell teilende Zellen richten (Chemotherapie, Strahlentherapie). Bei niedrigmalignen Lymphomen sind die Lymphomzellen deutlich weniger empfindlich gegenüber Chemo-/Strahlentherapie und i. d. R. überlebt immer ein gewisser Anteil der Zellen die Behandlung.
Die Therapie richtet sich u. a. nach dem Ann-Arbor-Stadium der Erkrankung. Generell ist zu sagen, dass die Bestrahlung nur in lokalisierten Stadien in kurativer Absicht sinnvoll ist. Bei niedrigmalignen NHL in höheren Stadien (ab Stadium II) hat die Chemotherapie meist nur palliativen Charakter, d. h. eine komplette Heilung ist damit nicht mehr möglich. Die Wahl des Chemotherapieschemas hängt natürlich auch von den Begleiterkrankungen des Patienten ab. Therapieschema der ersten Wahl bei hochmalignen NHL ist meist das CHOP-Schema. Hierbei werden die Medikamente Cyclophosphamid (=C), Doxorubicin (Hydroxidaunorubicin = H), Vincristin (Oncovin = O) sowie Prednisolon (=P) als Kombinationschemotherapie eingesetzt. Zunehmend werden monoklonale Antikörper zusätzlich zur Chemotherapie eingesetzt (bei B-NHL der Anti-CD20-Antikörper Rituximab => R-CHOP oder in Form einer Radioimmuntherapie Ibritumomab-Tiuxetan), da sich gezeigt hat, dass sie die Prognose sowohl bei hoch- als auch bei niedrigmalignen NHL verbessern. Es gibt Untersuchungen, die zeigen, dass bei B-NHL nach Abschluss der Primärbehandlung eine anschließende Erhaltungstherapie mit Rituximab die Langzeitergebnisse verbessern helfen kann.
Insgesamt gilt die Regel, dass die Therapie in Zentren mit viel Erfahrung gehört[5], da sich die Therapieprotokolle z. Z. fast im jährlichen Rhythmus ändern.
Stadium niedrigmaligne Lymphome hochmaligne Lymphome I Bestrahlung IA: Bestrahlung
IB: ChemotherapieII evtl. Chemotherapie Chemotherapie III und IV Chemotherapie Chemotherapie Notwendigkeit einer einheitlichen Klassifikation der Non-Hodgkin-Lymphome
Schon seit längerem war den klinisch tätigen Medizinern und auch den Hämatopathologen klar, dass es sich bei den NHL um eine sehr uneinheitliche Gruppe von Erkrankungen handelt. Es wurden daher Anstrengungen unternommen, die NHL weiter zu klassifizieren. Eine einheitliche Klassifikation war aus verschiedenen Gesichtspunkten notwendig: ohne klar definierte Begriffe und Krankeitsentitäten war es schier unmöglich, die Ergebnisse von Therapiestudien und von grundlagenmedizinischen Forschungen miteinander zu vergleichen. Die Erforschung der Krankheitsursachen und der optimalen Behandlungsmöglichkeiten war dadurch sehr erschwert.
Die ersten wirkliche brauchbaren Klassifikationen waren:
Kiel-Klassifikation
Die Kiel-Klassifikation hat Ihren Namen von der Universität Kiel erhalten, an der sie vom deutschen Hämatopathologen Prof. Karl Lennert 1969 entworfen und 1973/74 publiziert wurde. 1988 wurde die Kiel-Klassifikation überarbeitet. Die Kiel-Klassifikation teilt die NHL aufgrund von mikroskopisch-morphologischen, enzymzytochemischen und immunologischen Eigenschaften ein. Zudem wurden klinische Erfahrungen (eher bösartiger schneller oder eher gutartiger langsamer Verlauf) berücksichtigt. Lennert und seine Mitarbeiter differenzierten die Lymphome in niedrig-maligne und hoch-maligne. Diese Unterteilung basierte auf der Zellgröße. Die niedrig malignen Lymphome bestanden aus zytischen (eher reifen) und einem kleineren Anteil von blastischen (sehr unreifen) Zellen, wohingegen hoch maligne Lymphome überwiegend aus blastischen Zellen bestanden.
Die Kiel-Klassifikation wurde zur verbindlichen Klassifikation für die malignen Lymphome in Deutschland und erfuhr weite Verbreitung in ganz Europa. Im Laufe der Jahre zeigten sich jedoch auch Nachteile:
-
- in der originalen Klassifikation von 1974 waren die „primär extranodalen Lymphome“, d. h. die Lymphome, die primär außerhalb von Lymphknoten entstehen (z. B. die sogenannten MALT-Lymphome), nicht berücksichtigt,
- die Einteilung in „zytische“ niedrig maligne Lymphome und „blastische“ hoch maligne Lymphome korrelierte nicht immer mit dem klinischen Verlauf. So zeigte z. B. das zentrozytische Lymphom (das später sogenannte Mantelzelllymphom) häufig einen ungünstigen klinischen Verlauf, obwohl es durch die Kiel-Klassifikation als „niedrig-maligne“ klassifiziert wurde.
- viele spezielle in den folgenden Jahren erst erkannte bzw. entdeckte Lymphom-Erkrankungen waren in der originalen Kiel-Klassifikation noch nicht enthalten. 1988 erfolgte deswegen eine größere Überarbeitung der Kiel-Klassifikation.
Kiel-Klassifikation nach den Überarbeitungen 1988 und 1992: niedrig-maligne NHL
Niedrig-maligne B-NHL Niedrig-maligne T-NHL Lymphozytisch: B-CLL, B-PLL, Haarzellleukämie Lymphozytisch: T-CLL, T-PLL Lymphoplasmazytoides Lymphom Kleinzellig zerebriforme Lymphome: Mycosis fungoides, Sézary-Syndrom Zentroblastisch-zentrozytisches (cb-cc) Lymphom Angioimmunoblastisches Lymphom (AILD), Lymphogranulomatose X Zentrozytisches Lymphom T-Zonenlymphom pleomorph-kleinzelliges T-NHL Kiel-Klassifikation nach den Überarbeitungen 1988 und 1992: hoch-maligne NHL
Hoch-maligne B-NHL Hoch-maligne T-NHL Zentroblastisches Lymphom Pleomorph mittel- und großzelliges T-NHL Immunoblastisches B-NHL Immunoblastisches T-NHL Burkitt-Lymphom Großzellig anaplastisches B-NHL Großzellig anaplastisches T-NHL Lymphoblastisches B-NHL Lymphoblastisches T-NHL Die sogenannte Working formulation
1992 wurde in den U.S.A. eine Initiative ins Leben gerufen, die das Ziel hatte, die bisherigen unterschiedlichen Klassifikationsschemata zu vereinheitlichen. Die daraus resultierende Working Formulation of Non-Hodgkin’s Lymphoma for Clinical Usage, oder kurz Working Formulation (WF) wurde für die nächsten Jahre in den U.S.A. das verbindliche Klassifikationsschema für die NHL.
WHO-Klassifikation der malignen Lymphome
Die WHO-Klassifikation der NHL durch eine Expertengruppe der Weltgesundheitsorganisation ist die z.Zt. modernste und weitgehend akzeptierte Klassifikation der NHL, so dass man sich möglichst auf sie beziehen sollte. Ältere Klassifikationschemata sind aber immer noch im Gebrauch. Die Klassifikation der NHL befindet sich aber weiter im Fluss. Auch die WHO-Klassifikation wird in der Zukunft noch Überarbeitungen erfahren, da immer neuere und detailliertere Erkenntnisse über die Biologie und Pathophysiologie der NHL gewonnen werden.
Die WHO-Klassifikation klassifiziert (wie auch schon die R.E.A.L.-Klassifikation) die NHL nach zytomorphologischen, immunologischen und genetischen Merkmalen.
Vorläufer-B-Zell-Lymphome
- Vorläufer-B-lymphoblastisches Lymphom/Leukämie
Reife-B-Zell-Lymphome
- B-CLL / kleinzelliges lymphozytisches Lymphom
- Haarzell-Leukämie
- Plasmozytom
- Extranodales MALT-Lymphom
- Follikuläres Lymphom
- Mantelzell-Lymphom
- Diffuses großzelliges B-Zell-Lymphom
- Burkitt Lymphom / Leukämie
Vorläufer-T-Zell-Lymphome
- Vorläufer-T-lymphoblastisches Lymphom/Leukämie
Reife-T-Zell-Lymphome
- Mycosis fungoides/Sézary Syndrom
- Peripheres T-Zell Lymphom
- NK-Zell Leukämie
- Angioimmunoblastisches T-Zell Lymphom
- Anaplastisches großzelliges Lymphom, T-/Null-Zell-Typ
Quellen
- ↑ Lennart Hardell, Mikael Eriksson: A case-control study of non-Hodgkin lymphoma and exposure to pesticides. Cancer (85) 6, 19. Nov. 2000 [1]
- ↑ BMU-2004-639: Epidemiologische Fall-Kontrollstudie zur Ätiologie von Lymphomen. pdf
- ↑ International Non-Hodgkin's Lymphoma Classification Study [2]
- ↑ WHO/Real-Klassifikation
- ↑ Gerd Herold: Innere Medizin. Köln 2007 (Seite 66).
Literatur
- Kiel-Klassifikation
- Lennert K, Feller A. Histopathology of Non-Hodgkin’s Lymphomas, 2nd ed. New York, Springer Verlag 1992
- Lennert K, Mohri N, Stein H, Kaiserling E. The histopathology of malignant lymphoma. Br J Haematol 1975a;31(Suppl):193–203.
- Lennert K, Stein H, Kaiserling E. Cytological and functional criteria for the classification of malignant lymphomata. Br J Cancer 1975b;31 (Suppl 2):29–43. PubMed:52366
- Rappaport-Klassifikation: Rappaport H. Malignant lymphomas: nomenclature and classification. Tumors of the hematopoietic system. Washington, DC: Armed Forces Institute of Pathology, 1966; 6:97–161
- Lukes & Collins-Klassifikation
- Lukes RJ, Collins RD. New approaches to the classification of the lymphomata. Br J Cancer. 1975 Mar;31 Suppl 2:1–28. PubMed:1101914
- Lukes RJ, Collins RD. Immunologic characterization of human malignant lymphomas. Cancer. 1974 Oct;34 (4 Suppl):suppl:1488–503 PubMed:4608683
- Working Formulation: The Non-Hodgkin’s Lymphoma Pathologic Classification Project. National Cancer Institute sponsored study of classification of non-Hodgkin’s lymphomas. Summary and description of a Working Formulation for clinical usage. Cancer 1982;49:2112–2135. PubMed:6896167
- R.E.A.L.-Klassifikation: Harris NL, Jaffe ES, Stein H, Banks PM, Chan JK, Cleary ML, Delsol G, De Wolf-Peeters C, Falini B, Gatter KC, Grogan TM, Isaacson PG, Knowles DM, Mason DY, Müller-Hermelink H-K, Pileri SA, Piris MA, Ralfkiaer E, Warnke RA. A revised European-American classification of lymphoid neoplasms: a proposal from the International Lymphoma Study Group. Blood. 1994 ;84(5):1361–92. PubMed 8068936
- WHO-Klassifikation
- Jaffe E, Harris NL, Stein H, Vardiman JW (eds.): Pathology and Genetics of Tumours of Haemopoietic and Lymphoid Tissues. IARC Press: Lyon 2001
- Stein H.: Die neue WHO-Klassifikation der malignen Lymphome. Der Pathologe. 2000; 21(2):101–105
Weblinks
- Patienteninformationen des Kompetenznetzes „Maligne Lymphome“ und Suche nach Behandlungszentren für hochmaligne und niedrigmaligne Non-Hodgkin-Lymphome
- Patienteninformationen über NHL im Kindesalter pdf-Datei
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.

