- Anisaldehyd
-
Strukturformel 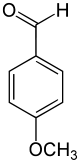
Allgemeines Name Anisaldehyd Andere Namen - 4-Methoxybenzaldehyd
- p-Methoxybenzaldehyd
Summenformel C8H8O2 CAS-Nummer 123-11-5 PubChem 31244 Kurzbeschreibung licht- und luftempfindliche, gelbliche Flüssigkeit mit charakteristischem Geruch[1]
Eigenschaften Molare Masse 136,15 g·mol−1 Aggregatzustand flüssig
Dichte 1,12 g·cm−3[1]
Schmelzpunkt Siedepunkt 248 °C[1]
Löslichkeit schlecht in Wasser (2 g·l−1 bei 20 °C)[1]
Brechungsindex 1,5731[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 
Achtung
H- und P-Sätze H: 302-315-319-335 EUH: keine EUH-Sätze P: 261-305+351+338 [3] EU-Gefahrstoffkennzeichnung [1] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22-36/37/38 S: 26-36 LD50 1510 mg·kg−1 (oral Ratte)[4]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C Anisaldehyd leitet sich strukturell von Benzaldehyd bzw. Anisol ab und gehört zur Stoffgruppe der Methoxybenzaldehyde.
Inhaltsverzeichnis
Vorkommen
In der Natur kommt Anisaldehyd in Anis, Fenchel und anderen ätherischen Ölen vor. Er wird in Pflanzen über den Shikimisäureweg synthetisiert.
Gewinnung und Darstellung
Anisaldehyd kann durch Oxidation (z. B. durch Salpetersäure oder Chromsäure) von Anethol oder 4-Methoxytoluol oder aus Anisol durch eine Vilsmeier-Reaktion gewonnen werden.
Eigenschaften
Anisaldehyd zersetzt sich ab 160 °C.[1]
Durch Umsetzen von Anisaldehyd mit Oxidationsmitteln (z. B. Fehling- oder Silberspiegelprobe) lässt sich Anissäure (p-Methoxybenzoesäure) darstellen.
Verwendung
Anisaldehyd wird als Zwischenprodukt zur Synthese von Arzneistoffen, Duftstoffen und anderer Chemikalien (z. B. Methoxybenzalaceton) verwendet.
Sicherheitshinweise
Die Dämpfe von Anisaldehyd können mit Luft ein explosionsfähiges Gemisch (Flammpunkt 116 °C, Zündtemperatur 220 °C)[1] bilden.
Einzelnachweise
- ↑ a b c d e f g h Eintrag zu CAS-Nr. 123-11-5 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 21. Februar 2009 (JavaScript erforderlich).
- ↑ CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ a b Datenblatt Anisaldehyd bei Sigma-Aldrich, abgerufen am 9. März 2011.
- ↑ ScienceLab: MSDS.
Wikimedia Foundation.
