- Parodontitis
-
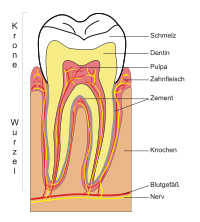
Klassifikation nach ICD-10 K05.2 Akute Parodontitis K05.3 Chronische Parodontitis ICD-10 online (WHO-Version 2011) Die Parodontitis (altgr. παρά ,neben‘ und ὀδούς ,Zahn‘)[1] ist eine bakteriell bedingte Entzündung, die sich in einer weitgehend irreversiblen Zerstörung des Zahnhalteapparates (Parodontium) zeigt.
Inhaltsverzeichnis
Abgrenzung
1921 hatte Oskar Weski zunächst den Begriff „Parodontose“ als Sammelbegriff für alle Erkrankungen (entzündliche und nicht-entzündliche) des Zahnbettes eingeführt.
Seit etwa Mitte des 20. Jahrhunderts wird jedoch zwischen Parodontitis und Parodontose unterschieden. Dies entspricht der allgemein in der Medizin gebräuchlichen Definition, in der die Endung ‚-itis‘ für entzündliche und die Endung ‚-ose‘ für atrophische (Gewebsschwund-) Prozesse steht. Der Begriff Parodontose hat heute nur noch historische Bedeutung.
Parodontose
Auch wenn der Begriff Parodontose (Synonym: Alveolaratrophie) weit verbreitet ist, handelt es sich dabei immer – fachlich korrekt ausgedrückt – um eine entzündliche Parodontitis.
Bei der Parodontose geht der Zahnbettschwund primär vom Knochen aus und Bindegewebe und Zahnfleisch folgen. Es treten keine vertieften Zahnfleischtaschen auf und das Zahnfleisch zeigt keine erhöhte Blutungsneigung. Typisch ist, dass nahezu gleichzeitig das gesamte Gebiss betroffen ist und es erst relativ spät zur Zahnlockerung kommt.[2] In der aktuellen wissenschaftlichen Fachliteratur wird der Begriff Parodontose nur noch unter historischen Gesichtspunkten erwähnt. Die beschriebene Begriffsdefinition, die einen parodontalen Knochenabbau ohne Entzündung beschreibt, ist klinisch nicht existent oder aber eine absolute medizinische Rarität. In der aktuellen Klassifikation der Parodontalerkrankungen taucht der Begriff nicht mehr auf.
Parodontitis
Man unterscheidet apikale (von der Wurzelspitze ausgehende) und marginale (vom Zahnfleischsaum ausgehende) Parodontitis. Die beiden können auch ineinander übergehen (Paro-Endo-Läsionen).
Ursache für die apikale Parodontitis ist ein marktoter Zahn, die Therapie besteht in einer Wurzelkanalbehandlung, einer Wurzelspitzenresektion oder dem Entfernen des Zahnes (Extraktion).
Im Weiteren soll hier nur von der marginalen Parodontitis die Rede sein. Diese kann man nach der aktuellen Klassifikation der Parodontalerkrankungen weiter unterteilen.
Ursachen
Die Parodontitis wird wie Gingivitis durch bakterielle Plaque (Zahnbelag) ausgelöst, einem zäh anhaftenden Biofilm. Hauptunterscheidungsmerkmal ist der bei der Parodontitis vorhandene, röntgenologisch nachweisbare Knochenabbau, während die vertieften Zahnfleischtaschen bei der Gingivitis durch die entzündliche Schwellung der Gingiva zustande kommen. Eine langandauernde Gingivitis (Zahnfleischentzündung) kann auf den Kieferknochen, die Wurzelhaut und das Zement übergreifen. Der Übergang ist jedoch nicht zwangsläufig, gerade bei Kindern und Jugendlichen kann eine Gingivitis über Monate und Jahre bestehen, ohne auf andere Strukturen überzugreifen. Die genauen Mechanismen sind noch nicht vollständig geklärt. Sowohl bei der Gingivitis als auch bei der Parodontitis werden aus dem Biofilm bakterielle Stoffwechsel- und Zerfallsprodukte freigesetzt, die Abwehrreaktionen des Körpers auslösen. Die Hauptrolle bei der Gewebszerstörung selbst spielt das eigene Immunsystem, das versucht, die Bakterien zu beseitigen. Diese Immunantwort besteht aus einer vielfältigen Abfolge von Reaktionen und Aktionen, bei der verschiedene Entzündungsstoffe und –zellen beteiligt sind. Unter anderem werden Enzyme gebildet, die die Bakterien zerstören sollen, jedoch auch zu einer Zerstörung von Eigengewebe führen. Das führt letztlich zum Verlust von Bindegewebe und Knochen. Das Ergebnis der Reaktion auf die Bakterien sind Zahnfleischbluten, Taschenbildung, Zurückgehen des Zahnfleischs und schließlich Lockerung und Verlust der Zähne.
Von den etwa 500 verschiedenen Bakterienspezies, die in der Mundhöhle vorkommen können, sind nur wenige parodontalpathogen (krankheitserregend im Sinne einer Parodontitis). Diese werden auch als Hauptleitkeime bezeichnet und bilden sogenannte Cluster (Haufen), welche in ihrer Vergesellschaftung spezifisch sind. Sie sind obligat oder fakultativ anaerobe, gramnegative, schwarzpigmentierte Bakterienarten wie der so genannte Rote Komplex (Porphyromonas gingivalis, Treponema denticola und Tannerella forsythensis (Bacteroides forsythus) sowie Actinobacillus actinomycetemcomitans Subtyp B (neuerdings Aggregatibacter actinomycetemcomitans).
Risikofaktoren
Obwohl das Immunsystem und die Anwesenheit bestimmter Bakterien die Hauptrolle bei der Entstehung einer Parodontitis spielen, gibt es einige Risikofaktoren, die die parodontale Gesundheit beeinflussen:
- schlechte oder falsche Mundhygiene mit Zahnbelag (Plaque) und Zahnstein
- genetische Prädisposition. In letzter Zeit wurde durch verschiedene Fall-Studien [3], aber auch in transversalen bevölkerungsrepräsentativen Studien[4] der bis dato noch unbekannte große Einfluss genetischer Prädisposition für das Krankheitsbild der Parodontitis erwiesen. Hier zeigt sich vor allem der Einfluss von Genotyp-Varianten im Bereich der Gene IL-1α (Interleukin), IL-1β und IL-1RN (Rezeptorantagonist). Dieser Zusammenhang ist auch für das Myeloperoxidase-Gen bekannt.
- Tabakkonsum. Raucher haben verglichen mit Nichtrauchern ein vier- bis sechsfach erhöhtes Risiko, eine Parodontitis zu entwickeln.
- Diabetes mellitus (insbesondere wenn der Blutzuckerspiegel schlecht eingestellt ist). Dieser Aspekt des Diabetes mellitus ist schon seit längerem bekannt und in verschiedenen Studien[5] belegt worden.
- Lebenspartner mit bestehender Parodontitis. Eine Ansteckung ist auch von Mutter zu Kind möglich.
- Schwangerschaft. Durch Hormonumstellung lockert das Bindegewebe auf, das Zahnfleisch schwillt an und Bakterien können leichter in die Tiefe vordringen.
- offene Zahnkaries
- Mundatmung
- Bruxismus (zumeist stressbedingtes Zähneknirschen)
- allgemeine Abwehrschwäche, insbesondere „immun-supprimierte“ Individuen (während oder nach Chemo-Therapie, Transplantations-Patienten, HIV-Erkrankte, etc.)
- unausgewogene Ernährung. Früher spielte Vitaminmangel eine große Rolle (Skorbut).
- ungünstig lokalisierte Piercings im Mundraum (Lippe, Lippenbändchen, Zunge)
Gefäßerkrankungen
Es existieren zahlreiche Studien, welche einen Zusammenhang zwischen periodontalen Erkrankungen (z.B. Parodontitis, Zahnfleischentzündung) und Gefäßerkrankungen (v.a. Arteriosklerose) nachweisen konnten. Ein Nachweis, ob dieser Zusammenhang kausal oder zufällig ist, existiert allerdings noch nicht.[6]
Diabetes
Es gibt mehrere Studien, die zeigen, dass Diabetiker – vor allem diejenigen mit schlecht eingestellten Blutzuckerwerten – ein höheres Risiko für die Entstehung einer Parodontalerkrankung haben. Ein Mangel an Insulin, also ein erhöhter Blutzucker-Wert kann Ablagerungen an den kleinen Gefäßen (Kapillaren) zur Folge haben und diese in ihrer Funktion beeinträchtigen: die Durchblutung lässt nach. Diese so genannten Mikroangiopathien wirken sich auf die Sauer- und Nährstoffversorgung des gesamten Gewebes aus, also auch auf das Zahnfleisch. Meistens verläuft bei diesen Patienten die Erkrankung in schwererer Ausprägung als bei Nicht-Diabetikern. Besonders gefährdet sind Diabetiker, die älter als 40 sind, denn die Schwere der Parodontitis nimmt mit der Dauer der Diabetes zu. Zudem kann eine Infektion des Zahnhalteapparates, wie alle Infektionen, zu Schwierigkeiten bei der Kontrolle des Blutzuckerspiegels führen und damit die Einstellung der Blutzuckerwerte erschweren.
Schwangerschaft
Seit Anfang der 90er Jahre weiß die zahnmedizinische Forschung um den Zusammenhang zwischen Zahnfleischerkrankungen (Parodontal-Erkrankung) und dem erhöhten Risiko von Frühgeburten bzw. Neugeborenen mit unterdurchschnittlichem Geburtsgewicht. Einige Studien belegen, dass das Risiko einer Frühgeburt oder eines untergewichtigen Neugeborenen bei Frauen mit einer Parodontitis fast achtmal höher als bei Frauen mit gesunden Zähnen und Zahnfleisch ist.
Verlauf
In den meisten Fällen handelt es sich um ein chronisch schubweise verlaufendes Geschehen. Dieses tritt vorwiegend bei Erwachsenen auf, ist nur selten schmerzhaft und führt, von den Betroffenen zumeist unbemerkt, erst nach Jahren zu Zahnlockerungen. Der Zahnfleischsaum bietet dabei für Bakterien einen relativen Schutz vor der Selbstreinigung der Mundhöhle durch Zunge und Speichel. Beim Gesunden garantiert das sogenannte Saumepithel durch seine Anhaftung am Schmelz eine kontinuierliche Oberfläche zwischen Zahnfleisch und Zahn. Wird die Plaque in diesen Nischen nicht sorgfältig entfernt, greifen die Ausscheidungsprodukte der Mikroorganismen (Exotoxine) das Saumepithel an und einige Bakterien sind sogar in der Lage, das Epithel zu durchwandern. Der Körper reagiert auf solche Angriffe mit der Einwanderung von Abwehrzellen aus dem Blut. Dabei bilden die neutrophilen Granulozyten und die Makrophagen einen Schutzwall gegen das weitere Vordringen von Fremdkörpern. Nach und nach werden so die Eindringlinge zerstört und phagozytiert („verdaut“). Dabei werden verschiedene Endotoxine freigesetzt. Sowohl die Exotoxine als auch die Endotoxine und einige Zerfallsprodukte der Körperabwehrzellen stellen einen Reiz dar. Um das umliegende Gewebe vor diesen Reizen zu schützen und einem Vordringen der Entzündung in die Tiefe vorzubeugen, aktiviert der Körper unter anderem Osteoklasten. Deren Aufgabe besteht im zielgerichteten Ab- und Umbau von Knochengewebe.
Bei einer guten Körperabwehr können die Mikroorganismen lange davon abgehalten werden, in die Tiefe vorzudringen. Die Kräfteverhältnisse in diesem Kampf sind jedoch sehr labil. Eine Verschlechterung der Körperabwehr, eine starke Vermehrung von Bakterien oder eine Veränderung der Aggressivität der Mikroorganismen führt dann zum Fortschreiten des Entzündungsgeschehens in die Tiefe. So kommt es im Verlauf zu einem stetigen Knochenverlust, der nur durch eine vollständige Entfernung der Reize gestoppt werden kann. Auf Röntgenbildern erscheint der Knochenverlust vorwiegend horizontal, da die Osteoklasten in Ruhephasen der Entzündung das zerklüftete Knochengewebe ausformen und so an die neuen Gegebenheiten anpassen. Aufgrund des langsamen und langen Krankheitsverlaufs wird diese Form der Entzündung als chronische Parodontitis bezeichnet.
Davon wird die aggressive Parodontitis unterschieden, welche rasch zu umfangreichem Knochenverlust führt und manchmal schon im Kindesalter auftritt. Darum wurde sie in der früheren Nomenklatur als juvenile Parodontitis bezeichnet. In Röntgenbildern erscheint der Knochenverlust bei diesem schnell fortschreitenden Verlauf als scharfkantiger vertikaler Krater entlang der Wurzeloberfläche, da keine Ummodellation stattgefunden hat. Als Ursachen für diese seltenere Form werden besonders aggressive Erreger und/oder eine nicht funktionierende lokale Abwehr der bakteriellen Reize diskutiert.
Da die Entzündungen in den Tiefen der parodontalen Taschen fortschreiten, ist eine Diagnose ohne zahnärztliche Hilfsmittel für Betroffene oft schwierig. Folgende Anzeichen können auf eine Erkrankung des Zahnhalteapparats hindeuten und sollten vom Zahnarzt abgeklärt werden:
- Gingivitiszeichen
- Zahnfleischbluten
- Rötungen, Schwellungen und Berührungsempfindlichkeit des Zahnfleisches
- in aktiven Entzündungsstadien außerdem
- Mundgeruch (Halitosis)
- Eiterbildung am Zahnfleisch
- Bei fortgeschrittenem Verlauf
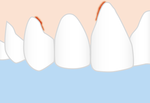
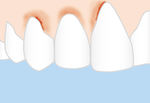
- Zahnfleischrückgang („die Zähne scheinen länger zu werden“)
- Zahnlockerung/-wanderung
Therapie
Die Therapie besteht darin, den Entzündungszustand des Zahnfleischs und des Zahnhalteapparats zu beseitigen und Plaque und Zahnstein sowie entzündungsfördernde Faktoren zu beseitigen. Die Behandlung gliedert sich in verschiedene Phasen mit unterschiedlichen Maßnahmen.
Die erste Phase stellt eine umfassende Diagnostik dar, mit welcher Art, Schwere und Verlauf der Erkrankung bestimmt werden. Klinisch beurteilt man den Gesamtzustand des Gebisses, die Zahnlockerung, die Tiefe der Taschen (Sondierungstiefe), den Zahnfleischrückgang und die Mundhygiene des Patienten. Außerdem wird durch Röntgenaufnahmen der Knochenverlauf festgestellt. In manchen Fällen werden ergänzend mikrobiologische (Nachweis bestimmter parodontalpathogener Bakterien) und genetische (Nachweis einer genetischen Veranlagung) Tests durchgeführt. Auch eine Überweisung zum Allgemeinmediziner zum Ausschluss einer systemischen Erkrankung (Diabetes, HIV, Leukämie etc.) kann nötig sein.
Anschließend werden in der sogenannten Hygienephase alle supragingival (oberhalb des Zahnfleischrands) gelegenen harten und weichen Beläge entfernt (professionelle Zahnreinigung, PZR). Dabei wird dem Patienten auch gezeigt, wie er zu Hause eine optimale Zahnpflege betreiben kann. Dieser Vorgang muss zumeist mindestens einmal wiederholt werden (die gesetzlichen Krankenkassen verlangen drei Sitzungen im Abstand von etwa einer Woche), außerdem müssen in dieser Phase bei Bedarf Füllungen oder Wurzelfüllungen gelegt oder erneuert und nicht erhaltungswürdige Zähne gezogen werden. Dadurch werden weitere Bakterienherde in der Mundhöhle eliminiert. Durch verschiedene Spülflüssigkeiten oder Medikamente kann das Bakterienwachstum ebenfalls kontrolliert und verringert werden. Allein durch diese Hygienemaßnahmen kann bei vielen Betroffenen schon eine merkliche Besserung erreicht werden.
Im Anschluss beginnt bei Bedarf die sogenannte geschlossene Behandlungsphase, bei der die subgingival (unterhalb des Zahnfleischrands) liegenden harten und weichen Beläge entfernt werden (geschlossene Kürettage). Dies geschieht mit Küretten (speziell geformte Handinstrumente), mit schall- und ultraschallbetriebenen Geräten oder unter Anwendung bestimmter Laser. Nach zwei bis drei Wochen Heilungszeit wird das Ergebnis dieser Behandlung kontrolliert, indem erneut die Sondierungstiefen gemessen und wenn nötig die Maßnahmen an einzelnen Stellen wiederholt werden.
Bei sehr tiefen Zahnfleischtaschen (über sechs Millimeter), welche durch die Hygienemaßnahmen und die geschlossene Behandlung nicht ausreichend zurückgegangen sind, kann es notwendig sein, in die offene Behandlungsphase überzugehen. Dabei werden die Bereiche chirurgisch eröffnet, damit die Maßnahmen der geschlossenen Behandlung unter Sicht wiederholt werden können. In diesem Fall ist es zum Teil auch möglich, eröffnete und gesäuberte Knochentaschen mit Knochenersatzmaterialien (Guided Bone Regeneration, GBR) aufzufüllen oder mit Membranen abzudecken (Guided Tissue Regeneration, GTR).
Unter bestimmten Voraussetzungen (aggressive, schnell verlaufende Formen der Parodontitis) ist es sinnvoll, die Behandlung durch die Anwendung von Antibiotika und/oder der Full-Mouth-Disinfection-Therapie zu ergänzen. In einer Schweizer Feldstudie konnten mikrobiologisch fünf parodontale Typen (Vergesellschaftungen von Bakterien) nachgewiesen werden, welche verschieden zu therapieren sind: bei drei Typen genügte eine Kürettage, bei zwei Typen mussten zusätzlich bestimmte Antibiotika verabreicht werden. Diese können in Tablettenform (systemisch) gegeben werden oder sie werden direkt in die Zahnfleischtasche eingebracht (lokal). In beiden Fällen ist es von Vorteil, vorher eine Keimbestimmung durchzuführen, um möglichst zielgerichtet zu behandeln. Es ist jedoch sinnlos, die Infektion mit Antibiotika zu therapieren, ohne die Zähne vorher zu reinigen. Die Bakterien sind in ihrem Biofilm vor der Einwirkung des antibiotischen Medikaments fast vollkommen geschützt. Erst durch die Zerstörung des Biofilms werden die Bakterien für die Antibiotika zugänglich.
Eine weitere lokale medikamentöse Behandlungsmethode (zusätzliche direkte Einbringung in die Zahnfleischtasche) ist die mit einem antiseptischen Chlorhexidinchip. Dieser sorgt für eine nachhaltige Keimfreiheit in der entzündeten Zahnfleischtasche und baut sich biologisch von selbst ab. Da es sich oftmals um eine chronische Form der Parodontitiserkrankung handelt, hat der Chlorhexidinchip zudem den Vorteil, dass die Keime keine Antibiotikaresistenz entwickeln, da es sich bei Chlorhexidin nicht um ein Antibiotikum handelt.
Prognose
Rechtzeitig und richtig behandelt kann einer Parodontitis fast immer Einhalt geboten werden, allerdings ist diese Behandlung zum Teil sehr langwierig und immer stark von der Mitarbeit des Patienten abhängig. Da die Parodontitis ein Ausdruck eines erfolgreichen bakteriellen Angriffs gegen die einst intakte Grenze Zahn-Zahnfleisch ist, muss sich jeder Betroffene im Klaren sein, dass selbst nach erfolgreicher Beseitigung dieser Entzündung die Gefahr des Rückfalls fortbesteht. Darum ist auch nach Beendigung der eigentlichen Therapie eine regelmäßige Nachsorge nötig, um einem erneuten Aufflammen der Entzündung frühestmöglich entgegenzuwirken.
Unbehandelt führt die Parodontitis fast immer zu Zahnverlust und daraus folgend zu ästhetischen und funktionellen Beeinträchtigungen. Außerdem ist Parodontitis ein Risikofaktor für allgemeinmedizinische Erkrankungen. So gilt ein Zusammenhang zwischen parodontalen Erkrankungen und erhöhtem Risiko für das Auftreten von Herz-Kreislauf-Erkrankungen (Herzinfarkt), Diabetes mellitus und Erkrankungen des rheumatischen Formenkreises als wissenschaftlich gesichert. In neueren Untersuchungen konnte außerdem gezeigt werden, dass eine unbehandelte Parodontitis das Risiko von Frühgeburten um das Siebenfache steigert und auch niedriges Geburtsgewicht ursächlich mit einer Parodontitis zusammenhängen kann.
Prophylaxe
Um einer Parodontitis oder ihrem Wiederaufflammen vorzubeugen, ist es am wichtigsten, eine gründliche Parodontitis-Prophylaxe zu betreiben. Neben dem eigentlichen Zähneputzen mit der Zahnbürste sollte auf eine gute Zahnzwischenraumpflege mit Zahnseide oder Interdentalbürsten und eine Entfernung von Belägen auf dem Zungenrücken geachtet werden. Bei regelmäßigen Kontrollen beim Zahnarzt in Verbindung mit einer professionellen Zahnreinigung alle drei bis sechs Monate können außerdem Putznischen gesäubert werden und Hilfestellungen bei der häuslichen Mundhygiene gegeben werden. Bei erhöhtem Risiko, zum Beispiel durch Schwangerschaft oder starken Stress, können die Prophylaxeintervalle verkürzt werden, um frühestmöglich auf Veränderungen des Parodonts reagieren zu können. Daneben ist es wichtig, die oben genannten Risikofaktoren zu verringern (z. B. aufhören zu rauchen, Diabetes optimal einstellen lassen).
Jüngste Forschungen empfehlen auch BLIS als mögliche Prophylaxe.[7]
Die Folgen des Zahnverlusts, vor allem die zum Teil sehr kostenintensiven prothetischen Maßnahmen, welche sich oft an eine parodontologische Behandlung anschließen, sowie die Erkenntnis über die allgemeinmedizinischen Zusammenhänge haben zur Folge, dass der Diagnose, Behandlung und vor allem der Vorbeugung dieser Erkrankung eine immer größere Bedeutung zugesprochen wird. Parodontitis ist eine „Volkskrankheit“, fast jeder ist im Laufe seines Lebens irgendwann mehr oder weniger stark davon betroffen. Bei den Über-40-Jährigen gehen mehr Zähne durch Parodontitis verloren als durch Karies.
Abrechnung bei gesetzlich Versicherten
Die gesetzlichen Krankenkassen in Deutschland haben zum 1. Januar 2004 die Parodontalbehandlung neu organisiert. Damit sollen die Früherkennung von Parodontalerkrankungen gefördert und gleichzeitig der Patient zur verstärkten Eigenleistung animiert werden. Die Idee dahinter war, dass der Patient selbst eine gute Mundhygiene als beste Prophylaxe sicherstellen soll. Die BEMA-Ziffer 04 wurde neu in den Leistungskatalog aufgenommen: 1x alle zwei Kalenderjahre ist die Erstellung eines Parodontalen Screening-Indexes (PSI) zu Lasten der Krankenkasse abrechenbar. Die BEMA-Ziffer 04 ist eine Ausnahmeleistung, hierfür wird die Praxisgebühr nicht fällig. Auf der anderen Seite kann seither die Entfernung des Zahnsteins (BEMA-Ziffer 107) im Rahmen der GKV nur noch einmal im Jahr abgerechnet werden (vorher 3x im Jahr). Stattdessen sollen Patienten bei Bedarf Prophylaxesitzungen beim Zahnarzt privat zahlen. Die Höhe der Kosten dafür ist von Praxis zu Praxis unterschiedlich.
Um für eine Parodontitistherapie die Kostenzusage durch eine Krankenkasse zu erhalten, verlangt diese eine einwandfreie Mundhygiene. Diese soll durch mindestens drei Mundhygienesitzungen beim Zahnarzt sichergestellt werden, die ggf. durch Privatleistungen des Patienten ergänzt werden können. Gefordert wird eine Privatleistung allerdings nicht, da eine Kassenleistung nicht vom Erbringen einer Privatleistung abhängig gemacht werden darf. Außerdem soll während dieser Vorbehandlungsphase das Gebiss in einen Zustand gebracht werden, den der Patient sauber halten kann. Dazu müssen alle nötigen chirurgischen, konservierenden und prothetischen Eingriffe stattfinden, zum Beispiel Extraktion nicht erhaltungsfähiger Zähne, Füllungen und Wurzelfüllungen.
Erst im Anschluss kann die eigentliche Parodontitisbehandlung beginnen, welche die Krankenkassen im eingeschränkten Umfang der Richtlinien bezahlt. Die Kosten für eventuelle Zusatzleistungen wie Laserbehandlungen oder die Bestimmung der Bakterienarten oder des genetischen Risikos muss der gesetzlich versicherte Patient selbst tragen.
Die Lage in Deutschland
Fast 12 Millionen Deutsche leiden an Parodontitis. Mehr als die Hälfte der 35- bis 44-Jährigen litt 2007 in Deutschland an Parodontitis, etwa 20 Prozent sogar an einer schweren Form. Dies ergab die Vierte Deutsche Mundgesundheitsstudie (DSM IV), erstellt vom Institut der Deutschen Zahnärzte im Auftrag der Kassenärztlichen Bundesvereinigung (KV) und der Bundeszahnärztekammer. Ein Grund für den Anstieg parodontaler Erkrankungen ist die verbesserte Mundgesundheit: Aufgrund der guten Kariesprophylaxe und zahnärztlicher Versorgung behalten ältere Menschen ihre eigenen Zähne immer länger. Die Zähne sind mit zunehmendem Alter aber einem hohen Parodontitis-Risiko ausgesetzt. Zum Beispiel leiden mehr als 40 Prozent der 65- bis 74-Jährigen an einer schweren Form der Parodontitis.[8]
Tiere
Auch Tiere, beispielsweise Hunde und Katzen, können von Parodontitis betroffen sein. Der Verlauf ähnelt dem beim Menschen. Auch hier stellen regelmäßige Kontrollen und die Zahnsteinentfernung die häufigsten Behandlungsmethoden dar.
Siehe auch
Literatur
- American Academy of Periodontology; Annette Bergfeld (Übersetzung, Bearb.): Parodontalerkrankungen und Gesundheit. Phillip Verlag, München 2000, ISBN 3934341020.
- Deutsche Gesellschaft für Parodontologie e.V. (Herausgeber): Risikokompendium Parodontitis. Quintessenz-Verl., Berlin u.a. 2002, ISBN 3-87652-433-4.
- C. Dörfer: Parodont und Allgemeingesundheit. In: zm – Zahnärztliche Mitteilungen, ISSN 0341-8995, zm 92, Nummer 9, Seiten 38 bis 43 (2002)
- Patienteninformationen der Bundeszahnärztekammer und der Deutschen Gesellschaft für Zahn-, Mund- und Kieferheilkunde zur Parodontalbehandlung, Regenerativen Therapie (GTR), Mikrobiologischen Diagnostik und Parodontitistherapie und zur Professionellen Zahnreinigung (PZR).
Einzelnachweise
- ↑ GEMOLL: Griechisch-deutsches Schul- und Handwörterbuch
- ↑ Walter Hoffmann-Axthelm: Lexikon der Zahnmedizin, Quintessenz-Verlag, Berlin
- ↑ Association of interleukin-1 polymorphisms with pe...[J Periodontol. 2005] - PubMed Result
- ↑ Smoking and polymorphisms of the interleukin-1 gen...[J Periodontol. 2002] - PubMed Result
- ↑ Diabetes-a risk factor for periodontitis in adult...[J Periodontol. 1994] - PubMed Result
- ↑ Periodontal infections and cardiovascular disease:...[J Am Dent Assoc. 2006] - PubMed Result
- ↑ LCL biokey: Literaturservice – aktuelle Literatur zu BLIS K12: Wirkung und Sicherheit (zum Herunterladen)
- ↑ Parodontitis-Erkrankungen nehmen zu Stand 2007

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- Krankheitsbild in der Zahnmedizin
- Bakterielle Infektionskrankheit des Menschen
Wikimedia Foundation.