- Atomkern
-
Der Atomkern ist der, im Vergleich zur Atomhülle, winzig kleine Kern des Atoms.
Kenntnisse über die Eigenschaften von Atomkernen sind beispielsweise zum Verstehen der Radioaktivität, der Kernspaltung (Kernkraftwerk, Kernreaktor, Kernwaffe) und der Kernfusion (Kernfusionsreaktor, Wasserstoffbombe) notwendig.
Von dem lateinischen Wort nucleus (Nuss- oder Pinienkern) leitet sich der Begriff „nuklear“ ab. Er bezeichnet Dinge oder Wirkungen, die mit Eigenschaften oder mit Reaktionen von Atomkernen zusammenhängen, beispielsweise Nuklearmedizin. Verschiedene Atomsorten werden nach dem Aufbau ihrer Atomkerne als Nuklide bezeichnet.
Inhaltsverzeichnis
Aufbau des Atomkerns
Bestandteile
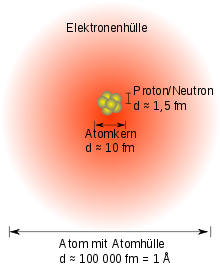
Der Atomkern besteht aus Protonen und Neutronen, die zusammen auch Nukleonen genannt werden. Er befindet sich, anschaulich gesprochen, im Zentrum des Atoms; sein Durchmesser beträgt etwa 1/10.000 bis 1/100.000 des Durchmessers der Elektronenhülle, konzentriert aber in sich mehr als 99,9 % der Masse des gesamten Atoms. Die Gesamtzahl der Nukleonen im Kern heißt deshalb auch Massenzahl (für Genaueres zur Masse des Kerns siehe Kernmasse oder Massendefekt).
Die Dichte des Kerns, also das Verhältnis von Kernmasse zu Kernvolumen, ist für alle Nuklide annähernd gleich und beträgt rund 2·1017 kg/m³.[1] In Neutronensternen werden noch bis zu 10 mal höhere Dichten vermutet.
Mit steigender Massenzahl der Atome nimmt die Dichte der Elemente nicht gleichmäßig zu, weil der Atomradius von der Atomhülle bestimmt wird und deshalb stark mit dem chemischen Charakter der Atome schwankt. Trotzdem gehören natürlich so genannte schwere Atomkerne auch zu umgangssprachlich/technisch schweren Elementen. Beispielsweise hat Lithium (Massenzahlen 6 und 7) eine Dichte von 0,53 g/cm³, Gold (Massenzahl 197) dagegen von 19,3 g/cm³.
Neutronen besitzen keine elektrische Ladung; Protonen sind positiv geladen. Infolgedessen ist der Atomkern elektrisch positiv geladen und kann durch die Coulombkraft negativ geladene Elektronen an sich binden. Da die elektrische Ladung des Elektrons bis auf das Vorzeichen gleich der Ladung des Protons ist, muss ein nach außen hin elektrisch neutrales Atom ebenso viele Elektronen in der so genannten Elektronenhülle besitzen wie Protonen im Kern. Werden durch chemische oder physikalische Effekte Elektronen entfernt oder hinzugefügt, ist das Atom nach außen hin elektrisch geladen und wird Ion genannt. Im Atomkern ändert sich dadurch nichts.
Eine Atomsorte (Nuklid) ist durch bestimmte Zahlen von Protonen und Neutronen im Atomkern bestimmt. Die Zahl der Protonen heißt Ordnungszahl oder Kernladungszahl. Sie bestimmt, zu welchem Element das Nuklid gehört. Nuklide gleicher Ordnungszahl werden als Isotope bezeichnet. Die Zahl der Neutronen hat nur geringen Einfluss auf die chemischen Eigenschaften des Atoms, ist aber entscheidend für die Stabilität oder Instabilität (Radioaktivität) des Kerns. Nuklide mit gleich vielen Protonen und Neutronen, aber unterschiedlichem inneren Anregungszustand (siehe unten) werden Isomere genannt. Bezeichnet werden Nuklide mit dem chemischen Elementsymbol und der Massenzahl, wie z. B. das häufigste Kohlenstoffisotop 12C oder das häufigste Eisenisotop 56Fe (bei Isomeren noch mit einem Zusatz wie „m“ für „metastabil“). Noch vollständiger ist die Schreibweise mit Massenzahl und Ordnungszahl:
 . Derzeit sind über 1000 Nuklide bekannt, davon sind ungefähr 250 stabil.
. Derzeit sind über 1000 Nuklide bekannt, davon sind ungefähr 250 stabil.Kernkraft und Coulombkraft
Die positiv geladenen Protonen im Kern stoßen sich gegenseitig aufgrund der Coulombkraft ab. Da der Kern jedoch trotzdem nicht auseinander fliegt, muss im Kern eine weitere Kraft existieren, mit der sich die Nukleonen gegenseitig anziehen und die stärker ist als die Coulombkraft. Diese Kraft wird als Kernkraft bezeichnet (nicht zu verwechseln mit dem umgangssprachlichen Ausdruck „Kernkraft“ für Kernenergie); sie ist eine Restwechselwirkung der Starken Wechselwirkung. Die Kernkraft ist bis heute nur näherungsweise beschrieben. Ihre Aufklärung ist unter anderem Gegenstand der Kernphysik. Gesichert ist allerdings die sehr kurze Reichweite der Kernkraft, die von der Größenordnung des Nukleon-Durchmessers (etwa 1 fm = 10 -15 m) ist. Sie bewirkt, dass es keine beliebig großen Kerne gibt, denn ein Proton an der „Oberfläche“ eines großen Kerns spürt Anziehung nur von seinen nächsten Nachbar-Nukleonen, Coulomb-Abstoßung hingegen von allen anderen Protonen des Kerns. Sind genügend viele andere Protonen vorhanden, überwiegt daher schließlich die Abstoßung.
Bindungsenergie
Die Bindungsenergie ist anschaulich die Arbeit, die aufgewandt werden müsste, um den Kern in seine einzelnen Nukleonen zu zerlegen. Sie entspricht dem sogenannten Massendefekt.
Die Bindungsenergie pro Nukleon – also Bindungsenergie geteilt durch Massenzahl – ist in verschiedenen Kernen verschieden.
 Darstellung der Kernspaltungs-Kettenreaktion auf einer Gedenkmünze
Darstellung der Kernspaltungs-Kettenreaktion auf einer Gedenkmünze
Auf Unterschieden der Bindungsenergie pro Nukleon beruht der Energiegewinn oder -verlust bei Kernreaktionen, also insbesondere die Möglichkeit, Energie im technischen Maßstab aus Kernreaktionen zu gewinnen.
Energieniveaus
Kerne haben wie Atome diskrete Energieniveaus. (Anders als beim Atom setzt sich die Folge dieser Niveaus aber auch oberhalb der Bindungsenergie eines Nukleons noch fort, was sich beispielsweise in den Resonanzen der Anregungsfunktion von Kernreaktionen zeigt.) Ein ungestörter Kern befindet sich normalerweise in seinem tiefsten Energieniveau, dem Grundzustand. Die höheren Niveaus (angeregte Zustände) sind nicht stabil, sondern der Kern geht früher oder später von dort in den Grundzustand über, wobei die Energiedifferenz als Photon (Gammastrahlung) abgegeben wird. Besonders langlebige (metastabile) angeregte Zustände werden als Isomere bezeichnet.
Radioaktivität
Der Begriff Radioaktivität bezeichnet die Eigenschaft instabiler Atomkerne, sich spontan unter Energieabgabe umzuwandeln. Dabei werden im Wesentlichen drei Zerfallsarten unterschieden:
- Zerfälle unter Aussendung von Nukleonen (z. B. Alpha-Zerfall),
- Beta-Zerfälle und
- Übergänge zwischen Zuständen ein- und desselben Kerns (unter Emission von Gammastrahlung).
Wegen des oben genannten Reichweitenunterschieds der Kräfte verringert sich die Bindungsenergie pro Nukleon zu hohen Massenzahlen hin. Daher tritt bei manchen Nukliden mit Massenzahlen oberhalb etwa 140 Alpha-Zerfall auf, oberhalb etwa 230 auch Spontane Spaltung. Beide Zerfallsarten führen zu Nukliden mit geringeren Massenzahlen.
Beim Betazerfall wird aus dem Kern eines Radionuklids ein Elektron oder Positron abgegeben. Dieses entsteht, indem sich im Kern eines der Neutronen in ein Proton, ein Antineutrino und ein Elektron bzw. eines der Protonen in ein Neutron, ein Neutrino und ein Positron umwandelt.
Die Abgabe von Gammastrahlung setzt voraus, dass der Kern in einem angeregten Zustand ist (vgl. Abschnitt Energieniveaus) und tritt daher hauptsächlich unmittelbar nach einem Alpha- oder Betazerfall auf, sofern dieser nicht direkt zum Grundzustand des Tochterkerns führt. Deshalb wird die Gamma-Emission analog den anderen Prozessen der Radioaktivität manchmal als Gamma„zerfall“ bezeichnet.
Kernmodelle
Anders als in der Atomphysik mit dem quantenmechanischen Atommodell, wo lediglich die elektromagnetische Wechselwirkung eine Rolle spielt, existiert in der Kernphysik kein Modell zur umfassenden Beschreibung aller Vorgänge im Atomkern, sondern es werden verschiedene Modelle für unterschiedliche Fragestellungen benutzt. Ähnlich dem Schalenmodell der Atomphysik gibt es auch in der Kernphysik ein Schalenmodell, das es erlaubt, die Energiezustände eines einzelnen Nukleons trotz fehlendem Zentralpotential in einem mittleren Potential zu berechnen. Die meisten angeregten Zustände eines Atomkerns können jedoch nur durch die kollektive Anregung mehrerer Nukleonen erklärt werden. Für die Beschreibung solcher Zustände kann man das kollektive Modell heranziehen. Die Eigenschaften von großen Atomkernen werden durch ein vibrierendes Tröpfchenmodell beschrieben.
- Das Tröpfchenmodell (Niels Bohr, 1936) beschreibt den Atomkern als Tröpfchen einer geladenen Flüssigkeit. Mit diesem klassischen Modell kann etwa die Kernspaltung gut erklärt werden (Bohr und John Archibald Wheeler, 1939).
- Das Schalenmodell (Eugene Paul Wigner, Maria Goeppert-Mayer, J. Hans D. Jensen, 1949) führt den Aufbau der Atomkerne auf quantenmechanische Gesetzmäßigkeiten (unter Anderem das Pauli-Prinzip) zurück. Die Wechselwirkung zwischen den Nukleonen wird dabei mit berücksichtigt. Das Schalenmodell kann die verschiedene Stabilität der Kerne gut erklären, insbesondere die hohe Stabilität bei bestimmten, sogenannten magischen Protonen- und Neutronenanzahlen.
Neben diesen beiden gängigen Modellen gibt es weitere (das folgende orientiert sich stark an Siegfried Flügge, 1957):
- das Fermigas-Modell (auch uniformes Modell). In diesem Modell werden die Nukleonen trotz der starken Wechselwirkungen als frei beweglich postuliert. Der Kern hat in diesem Modell unendliche Ausdehnung, womit die Wellenfunktionen der einzelnen Nukleonen flache Wellen sind;
- das Alphateilchen-Modell. Alphateilchen sind stabile Untereinheiten innerhalb des Kerns;
- das vereinte Modell (mit dem kollektiven Modell als Spielart).
- das Potentialtopf-Modell (potential well model).
Modelle des Atomkerns fallen in zwei Kategorien:
- starke Wechselwirkungsmodelle: Der Atomkern wird als Ansammlung von eng gepaarten Nukleonen verstanden (Tröpfchenmodell, Alphateilchen-Modell und partiell auch das optische Modell, compound well model);
- Unabhängige-Teilchen-Modelle: Die Nukleonen bewegen sich relativ frei im Kern (Fermigas-Modell, optisches Modell, Schalenmodell, Potentialtopf-Modell).
Zwischen den einzelnen Modellen lassen sich folgende Beziehungen aufstellen:
- Das Schalenmodell ist eine Verfeinerung des Fermigas-Modells;
- Das Fermigas-Modell und das Tröpfchenmodell basieren auf diametral entgegengesetzten Annahmen, erklären jedoch beide nukleare Eigenschaften wie die Bindungsenergien;
- Das optische Modell ist ein Hybrid zwischen Potentialtopf- und Zwischenkern-Modell;
- Schalenmodell und vereintes Modell sind äquivalent.
Jedes der genannten Modelle ist nur für einen bestimmten nuklearen Phänomenbereich anwendbar. Es gibt keine konsistente Theorie, die alle nuklearen Phänomene umfasst.
Geschichte
Der Nachweis von Atomkernen gelang dem Nobelpreisträger Ernest Rutherford am 20. Dezember 1910. Bei Versuchen hatte er beobachtet, dass Alphateilchen (das sind Helium-Atomkerne, dies war damals aber noch nicht bekannt) beim Durchqueren dünner Metallfolien zwar nur selten, aber dann sehr stark von ihrer Bahn abwichen. Dies stand im Widerspruch zu dem erwarteten Ergebnis: Nach dem damals angenommenen Thomsonschen Atommodell („Rosinenkuchen-Modell“, englisch „plum pudding model“) hätte das Atom aus Elektronen bestanden, die in einer diffusen positiv geladenen Wolke schwebten. Rutherford hatte dementsprechend erwartet, dass die Alphateilchen häufig, aber dafür nur wenig von ihrer Bahn abweichen würden. Zweck des Versuchs war es eigentlich, die Eigenschaften dieser Wolke näher zu untersuchen. Rutherford interpretierte das unerwartete Ergebnis so, dass die Atome der Folie größtenteils aus leerem Raum bestanden, der die Alphateilchen ungehindert passieren ließ , während kleine, aber sehr massive Partikel darin existierten, die die Alphateilchen bei einem der seltenen Zusammenstöße sehr stark aus ihrer Bahn warfen. Einige Berechnungen zeigten Rutherford, dass fast die gesamte Masse der Atome in diesen „Kernen“ konzentriert sein musste.[2]
Siehe auch
Literatur
- Theo Mayer-Kuckuk, Kernphysik, Verlag: B.G. Teubner Stuttgart, 1994, 6. durchgesehene Auflage, ISBN 3-519-03223-6
- Bogdan Povh, K. Rith, C. Scholz, F. Zetsche, Teilchen und Kerne, Springer-Verlag Heidelberg, 1994, 2. neu bearbeitete und erweiterte Auflage, ISBN 3-540-58172-3
- Siegfried Flügge (Hrsg.), Handbuch der Physik, Band XXXIX: Bau der Atomkerne, Göttingen: Springer-Verlag, 1957.
Videos
- Was ist ein Atomkern? aus der Fernseh-Sendereihe alpha-Centauri
- Einfache Erklärung von "Anderthalb" (langsame Verbindung)
- Einfache Erklärung von "Anderthalb" (schnelle Verbindung)
Weblinks
 Wiktionary: Atomkern – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Wiktionary: Atomkern – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen- animierte Seite zu Kernmodellen (Potentialtopf~, Tröpfchen~) (LEIFI)
- umfangreiche Nuklidliste
- Paul, Weise (TU München), online Skript Teilchen und Kerne
Einzelnachweise
- ↑ D. Meschede: Gerthsen Physik, 22. Auflage, 2004; S. 630
- ↑ Deutsche Welle-Kalenderblatt zum 20. Dezember, abgefragt am 19. Dezember 2008
Wikimedia Foundation.