- Pyridyl
-
Strukturformel 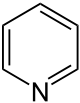
Allgemeines Name Pyridin Andere Namen - Azabenzol
- Azin
Summenformel C5H5N CAS-Nummer 110-86-1 Kurzbeschreibung farblose Flüssigkeit mit unangenehmem Geruch Eigenschaften Molare Masse 79,10 g·mol−1 Aggregatzustand flüssig
Dichte 0,982 g/cm3[1]
Schmelzpunkt Siedepunkt 115 °C[2]
Dampfdruck Löslichkeit vollständig mischbar mit Wasser, gut löslich in Ethanol, Ether, Aceton, Ölen und Fetten, Chloroform, Petrolether und Ligroin
Dipolmoment 2,2 D (20 °C) Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [3] 

Leicht-
entzündlichGesundheits-
schädlich(F) (Xn) R- und S-Sätze R: 11-20/21/22 S: (2)-26-28 MAK 5 ml/m3; 16 mg/m3
LD50 WGK 2 (wassergefährdend)[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Pyridin auch bekannt als Azin oder Azabenzol, ist ein Heteroaromat, also eine heterocyclische Verbindung mit aromatischen Eigenschaften (siehe Aromate). Man kann es sich vom Benzol abgeleitet denken, in dessen Ring eine C-H Gruppe durch ein Stickstoffatom ersetzt ist (daher der Name Azabenzol).
Inhaltsverzeichnis
Historisches
Es wurde zuerst im Knochenöl, welches sich durch starkes Erhitzen von trockenen Knochen bildet, entdeckt. „Pyr“ ist abgeleitet vom griechischen Wort für Feuer.
Natürliches Vorkommen
Pyridin kommt neben vielen anderen aromatischen Verbindungen im Steinkohlenteeröl vor. Salze von Pyridinderviaten sind in der belebten Natur häufig zu finden, wie zum Beispiel im Nicotinamidadenindinukleotid (NAD). Viele Pyridin-Derivate sind wichtige Naturstoffe, wie beispielsweise Nikotin, Nicotinamid, ein Vitamin, dessen Mangel Pellagra verursacht, oder Vitamin B6, auch Pyridoxin genannt.
Gewinnung und Herstellung
Pyridin und alkylsubstituierte Pyridine wie beispielsweise Picoline werden durch Destillation oder Schwefelsäure-Extraktion aus Steinkohlenteer, in dem es zu 0,1 % vorkommt, gewonnen. Sie können auch aus Acetaldehyd und Ammoniak über eine für viele Pyridinderivate anwendbare Hantzsch-Synthese dargestellt werden.
Physikalische und chemische Eigenschaften
Pyridin liegt bei Raumtemperatur als farblose, gesundheitsschädliche, übelriechende Flüssigkeit vor. Es ist mit Alkohol und Wasser mischbar, reagiert schwach basisch und bildet mit Chlorwasserstoffsäure (Salzsäure) ein kristallines Hydrochlorid, welches erst bei 145 °C schmilzt. Durch den elektronegativen Stickstoff ist der Ring relativ elektronenarm. Dies hemmt die sonst für aromatische Systeme typische elektrophile Substitution und begünstigt die Metallierung durch starke Basen.
Verwendung
Pyridin wird als Base in vielen organisch-chemischen Synthesen eingesetzt, oft auch gleichzeitig als Lösungsmittel. Es dient auch als Synthesebaustein zur Herstellung einer Vielzahl von Stoffen wie Arzneimitteln und Herbiziden. Im Gemisch mit Picolinen wurde Pyridin manchmal zum Denaturieren von Ethanol zu Brennspiritus eingesetzt, ist heute aber oft durch ungiftigere Stoffe ersetzt.
Nomenklatur
Kommt Pyridin als Substituent vor, wird wie bei anderen Heterocyclen die Endung -yl angehängt, also Pyridinyl, oder die gebräuchlichere Kurzform Pyridyl verwendet. Die Zählung der Ringpositionen beginnt mit "1" am Stickstoffatom und verläuft in Richtung der Anknüpfungsposition.
Gefährdungspotential
Pyridin verursacht Reizungen an Haut und Schleimhäuten. Nach Verschlucken sind Übelkeit und Kopfschmerzen, in hohen Dosen auch Herz-Kreislaufstörungen, Kollaps und Bewusstlosigkeit möglich. Es besteht die Gefahr der Hautresorption und von irreversiblen Gesundheitsschäden. Bei längerer Exposition werden Leber und Nieren geschädigt. Durch den unangenehmen Geruch bei gleichzeitig niedriger Geruchsschwelle besteht jedoch eine gute Warnwirkung. Pyridin ist wassergefährdend.
Methyl-Derivate
Picoline sind mono-Methyl-Pyridine,
Lutidine sind di-Methyl-Pyridine,
Collidine sind tri-Methyl-Pyridine.Siehe auch
- Terpyridin
- Bipyridin
Literatur
- Eicher/ Hauptmann, Heterocyclic Chemistry, 2. Aufl. 2003, WILEY-VCH, Weinheim, S. 269-309. (Struktur, physikalische Eigenschaften, spektroskopische Eigenschaften; chemische Eigenschaften, Synthesen; wichtige Derivate, Naturstoffe, Medikamente; Nutzen als Reagenz, Baustein, Auxiliar in der org. Synthese)
Einzelnachweise
- ↑ a b c d Sicherheitsdatenblatt der Merck KGaA, Darmstadt
- ↑ a b c Eintrag zu CAS-Nr. 110-86-1 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 21. Oktober 2007 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 110-86-1 im European chemical Substances Information System ESIS
Weblink
Wikimedia Foundation.

