- 1-Pentanol
-
Strukturformel 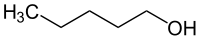
Allgemeines Name 1-Pentanol Andere Namen - Pentan-1-ol
- Amylalkohol
- Butylcarbinol
- Pentylalkohol
Summenformel C5H12O CAS-Nummer 71-41-0 PubChem 6276 Kurzbeschreibung farblose Flüssigkeit[1]
Eigenschaften Molare Masse 88,15 g·mol−1 Aggregatzustand flüssig
Dichte 0,81 g·cm−3[1]
Schmelzpunkt Siedepunkt 138 °C[1]
Dampfdruck Löslichkeit schlecht in Wasser (22 g·l−1 bei 20 °C)[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 

Achtung
H- und P-Sätze H: 226-332-335-315 EUH: keine EUH-Sätze P: 302+352 [1] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 10-20-37-66 S: (2)-46 MAK 73 mg·m−3[1]
LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. 1-Pentanol (veraltet: Amylalkohol) ist eine organische chemische Verbindung aus Kohlenstoff, Wasserstoff und Sauerstoff, die eine Hydroxygruppe trägt. Sie gehört damit zu den Alkoholen. 1-Pentanol ist Bestandteil der Fuselöle.
Inhaltsverzeichnis
Gewinnung und Darstellung
Früher wurden die Amylakohole durch Destillation von Fuselölen gewonnen. Aktuell werden sie durch Hydrolyse von Halogenpentanen synthetisiert:[5]
Eigenschaften
1-Pentanol ist eine farblose Flüssigkeit mit charakteristischem Geruch, die sich nur wenig in Wasser löst.[5] 1-Pentanol löst Lithiumchlorid, was für den qualitativen Nachweis von Lithium von Bedeutung ist.
Thermodynamische Eigenschaften
Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,68277, B = 1492,549 und C = −91.621 im Temperaturbereich von 307 bis 411 K.[6]
Zusammenstellung der wichtigsten thermodynamischen Eigenschaften Eigenschaft Typ Wert [Einheit] Bemerkungen Standardbildungsenthalpie ΔfH0liquid
ΔfH0gas−351,62 kJ·mol−1[7]
−298 kJ·mol−1 [8]Standardentropie S0l
S0g258,9 J·mol−1·K−1[9]
401,3 J·mol−1·K−1[10]als Flüssigkeit
als GasVerbrennungsenthalpie ΔcH0liquid −3330,91 kJ·mol−1[7] Wärmekapazität cp 123,1 J·mol−1·K−1 (25 °C)[11]
167,91 J·mol−1·K−1 (130,35 °C)[12]als Flüssigkeit
als GasSchmelzenthalpie ΔfH0 10,502 kJ·mol−1 [9] beim Schmelzpunkt Schmelzentropie ΔfS0 53,70 kJ·mol−1 [9] beim Schmelzpunkt Verdampfungsenthalpie ΔVH0 44,36 kJ·mol−1 [13] beim Normaldrucksiedepunkt Die Temperaturabhängigkeit der Verdampfungsenthalpie lässt sich entsprechend der Gleichung ΔVH0=Aexp(−αTr)(1−Tr)β (ΔVH0 in kJ/mol, Tr =(T/Tc) reduzierte Temperatur) mit A = 67,55 kJ/mol, α = −0,8195, β = 0,8272 und Tc = 588,2 K im Temperaturbereich zwischen 298 und 421 K beschreiben. [13]
Sicherheitstechnische Kenngrößen
1-Pentanol gilt als entzündliche Flüssigkeit. Oberhalb der Flammpunktes können sich entzündliche Dampf-Luft-Gemische bilden. Die Verbindung hat einen Flammpunkt bei 43 °C.[14] Der Explosionsbereich liegt zwischen 1,3 Vol% (47 g/m3) als untere Explosionsgrenze (UEG) und 10,5 Vol% (385 g/m3) als obere Explosionsgrenze (OEG).[14] Der maximale Explosionsdruck liegt bei 8,4 bar.[14] Die Zündtemperatur beträgt 320 °C.[14] Der Stoff fällt somit in die Temperaturklasse T2.
Verwendung
1-Pentanol wird als Lösungsmittel und zur Herstellung von Pharmazeutika, Kosmetika, Farb- u. Geschmackstoffen verwendet. Er ist weiterhin in Desinfektionsmitteln enthalten.
Toxizität
Alle Pentanole besitzen eine wesentlich höhere Toxizität als die meisten niederen Alkohole wie etwa Ethanol. Orale Dosen von 1-Pentanol ab etwa 0,5 g pro kg Körpergewicht (~30 ml) werden für den Menschen als letal angesehen.[1] Neben einer oralen Aufnahme ist auch eine Schädigung über die Atemwege sowie eine Reizung von Augen und Haut möglich.[5] Im Tierversuch erzeugte 1-Pentanol bei Ratten[3] und Mäusen[15] Nierenfunktionsstörungen, Atembeschwerden bis zu Lungenödemen und depressives Verhalten bis zur Schläfrigkeit.
Einzelnachweise
- ↑ a b c d e f g h i j Eintrag zu CAS-Nr. 71-41-0 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. August 2007 (JavaScript erforderlich)
- ↑ Nicht explizit in RL 67/548/EWG, Anh. I gelistet, fällt aber dort mit der angegebenen Kennzeichnung unter den Sammelbegriff „Pentanolisomere“; Eintrag in der GESTIS-Stoffdatenbank des IFA, abgerufen am 30. März 2009 (JavaScript erforderlich)
- ↑ a b c National Technical Information Service. Vol. OTS0534716
- ↑ Gigiena i Sanitariya. (English translation in HYSAAV. Vol. 35(9), Pg. 88, 1970.)
- ↑ a b c Wissenschaft-Online-Lexika: Eintrag zu Amylalkohole im Lexikon der Chemie. Abgerufen am 10. Februar 2009
- ↑ Kemme, H.R.; Kreps, S.I.: Vapor Pressure of Primary n-Alkyl Chlorides and Alcohols in J. Chem. Eng. Data 14 (1969) 98-102.
- ↑ a b Mosselman, C.; Dekker, H.: Enthalpies of formation of n-alkan-1-ols in J. Chem. Soc. Faraday Trans. 1, 1975, 417-424.
- ↑ NIST Chemistry WebBook http://webbook.nist.gov/chemistry/
- ↑ a b c Counsell, J.F.; Lees, E.B.; Martin, J.F.: Thermodynamic properties of organic oxygen compounds. Part XIX. Low temperature heat capacity and entropy of propan-1-ol, 2-methyl-propan-1-ol and pentan-1-ol 1968, J.
- ↑ Counsell J.F.: Thermodynamic properties of organic oxygen compounds. Part XIX. Low-temperature heat capacity and entropy of propan-1-ol, 2-methylpropan-1-ol, and pentan-1-ol in J. Chem. Soc. A, 1968, 1819-1823.
- ↑ Benson, G.C.; D'Arcy, P.J.: Excess isobaric heat capacities of some binary mixtures: (a C5-alkanol + n-heptane) at 298.15 K in J. Chem. Thermodynam. 18 (1986) 493-498.
- ↑ Stromsoe E.: Heat capacity of alcohol vapors at atmospheric pressure in J. Chem. Eng. Data 15 (1970) 286-290.
- ↑ a b Majer, V.; Svoboda, V., Enthalpies of Vaporization of Organic Compounds: A Critical Review and Data Compilation, Blackwell Scientific Publications, Oxford, 1985, 300
- ↑ a b c d E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen - Band 1: Brennbare Flüssigkeiten und Gase, Wirtschaftsverlag NW – Verlag für neue Wissenschaft GmbH, Bremerhaven 2003
- ↑ American Industrial Hygiene Association Journal. Vol. 34, Pg. 493, 1973.
Wikimedia Foundation.
