- Batterie (Elektrotechnik)
-
Mit dem Begriff der elektrischen Batterie wurde ursprünglich eine Zusammenschaltung mehrerer gleichartiger galvanischer Zellen bzw. Elemente[1] bezeichnet, als welche zunächst, z. B. in der voltaschen Säule oder Zambonisäule, nur nicht wiederaufladbare (sogenannte „Primärzellen“ bzw. „Primärelemente“) zur Verfügung standen. Mit der Entwicklung wirtschaftlich einsetzbarer wiederaufladbarer „Sekundärzellen“, „Sekundärelemente“ bzw. „Akkumulatoren“, z. B. des Bleiakkus um 1850 bis 1886, wurde die Benutzung des Begriffs „Batterie“ auch auf die Zusammenschaltung mehrerer solcher Zellen erweitert, z. B. in den späteren Starterbatterien von Kraftfahrzeugen oder Traktionsbatterien von U-Booten usw.
In letzter Zeit schließlich hat sich die Verwendung des Begriffs „Batterie“ auch auf einzelne Primär- oder Sekundärzellen ausgedehnt, wobei für letztere der Eindeutigkeit wegen stets besser die Bezeichnung „Akkuzelle“ oder einfach nur „Akku“ verwendet werden sollte. Dem geschilderten Wandel des Sprachgebrauchs hat sich auch die DIN-Norm 40729 Akkumulatoren; Galvanische Sekundärelemente; Grundbegriffe angeschlossen, die den Begriff der „Batterie“ zwar eingangs allein im ursprünglichen Sinn als Reihenschaltung mehrerer galvanischer Elemente definiert, dann aber doch den entstandenen Neologismus „Batterie“ als allgemeiner Bezeichnung auch einzelner galvanischer Zellen mitverwendet.[2]
Unter Hinweis auf diese Begriffshistorie wird hier ausschließlich die Vielfalt „elektrischer Zellen“ beschrieben, die umgangssprachlich bzw. „handelsüblich“, seit einiger Zeit aber auch vom DIN als „Batterien“ bezeichnet werden, wobei die Besprechung von „Primärzellen“ im Vordergrund steht – für eine nähere Besprechung von „Sekundärzellen“ siehe Hauptartikel Akkumulator.
Inhaltsverzeichnis
Geschichte
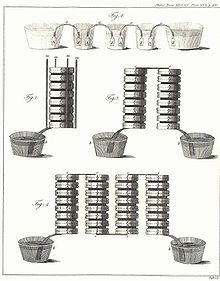
Im Jahr 1780 bemerkte der italienische Arzt Luigi Galvani, dass ein Froschbein, das in Kontakt mit zwei verschiedenen Metallen kam, zuckte und hielt das für eine elektrische Wirkung. Das erste funktionierende galvanische Element und damit die erste Batterie wurde in Form der Voltaschen Säule im Jahr 1800 von Alessandro Volta vorgestellt. 1901 entwickelte Paul Schmidt in Berlin die Trockenbatterie.
In der Antike vorhandene Gefäße wie die „Bagdad-Batterie“ erzeugen durch das Zusammenspiel aus Kupfer, Eisen und Essig eine elektrische Spannung von circa 0,8 V. Ob dieses Gefäß zum damaligen Zeitpunkt vor etwa 2.000 Jahren als Batterie im heutigen Sinn verwendet wurde, ist umstritten.
Grundlagen
Eine elektrische Zelle ist ein elektrochemischer Energiespeicher und ein Energiewandler. Bei der Entladung wird gespeicherte chemische Energie durch die elektrochemische Redoxreaktion in elektrische Energie umgewandelt. Diese kann von einem vom Stromnetz unabhängigen elektrischen Verbraucher genutzt werden. Alternativ kann sie auch in einem vom Stromnetz abhängigen Verbraucher eingesetzt werden, um kurzzeitige Ausfälle im Stromversorgungsnetz zu überbrücken und so eine unterbrechungsfreie Stromversorgung sicherstellen.
Primärzellen können nur einmal entladen und nicht wieder aufgeladen werden. In diesen Zellen sind die Reaktionen bei der Entladung teilweise umkehrbar, das führt jedoch nicht zur Wiederherstellung eines dem Neuzustand ähnlichen Energieinhalts. Dagegen sind die wiederaufladbaren Sekundärbatterien (Akkumulatoren) weitgehend in den Ladezustand ähnlich dem Neuzustand zu bringen, so dass eine mehrfache Umwandlung von chemischer in elektrische Energie und zurück möglich ist.
Die Elektrodenmaterialien legen die Nennspannung der Zelle fest, die Menge der Materialien die enthaltene Energie.
Wichtige Begriffe in Bezug auf die elektrischen Eigenschaften einer Batterie sind:
- Kapazität
- Die in einer Batterie gespeicherte elektrische Ladung wird umgangssprachlich als Kapazität bezeichnet, das ist nicht zu verwechseln mit der elektrischen Kapazität. Die Kapazität einer Batterie wird in der Regel in Amperestunden (Einheitenzeichen: Ah), seltener in Amperesekunden (As) oder Coulomb (C; 1 As entspricht 1 C) angegeben.
- Leistung
- Die Leistung einer Batterie ist die Menge an elektrischer Energie, die pro Zeiteinheit entnommen werden kann. Sie wird in der Regel in Watt (W) angegeben und ist das Produkt aus Entladestrom und Entladespannung.
- Energieinhalt
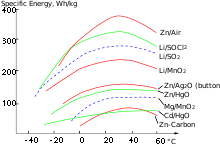
- Die in einer Batterie gespeicherte Energie elektrische Arbeit wird meist nicht angegeben, die Energie pro Masse oder pro Volumen ist jedoch eine typische Kenngröße von Batteriesystemen. Eine Einschätzung je nach Typ geben Diagramme vergleichender Energieangaben (siehe Diagramm).
- Selbstentladung
- Alle Batterien unterliegen bei Lagerung der Selbstentladung. Die Geschwindigkeit der Selbstentladung hängt unter anderem vom Batterietyp und der Temperatur ab. Je niedriger die Lagertemperatur, desto geringer ist die Selbstentladung.
Einsatzbereiche
Je nach dem Einsatzgebiet gibt es folgende Begriffe und Zuordnungen:
- Gerätebatterien dienen zur Stromversorgung kleiner, meist tragbarer Geräte, beispielsweise in Taschenlampen oder Mobiltelefonen. Besonders kleine Ausführungen für Hörgeräte oder Quarzuhren werden als Knopfzellen bezeichnet.
- Starterbatterien für Kraftfahrzeuge, Traktionsbatterien für Elektrofahrzeuge und stationäre Batterien bei ortsfesten Anwendungen wie beispielsweise Unterbrechungsfreie Stromversorgung sind immer Akkumulatoren.
Typvariationen
Aufgrund der vielfältigen Einsatzbereiche mit sehr unterschiedlichen Anforderungen bezüglich Spannung, Leistung und Kapazität gibt es heute Batterien in vielen Typen. Diese werden unterschieden beispielsweise
- nach chemischer Qualität in der zugrunde liegenden chemischen Redoxreaktion,
- Zusammenschaltung von Zellen
- nach Zellengrößen.
Handelsübliche Batterien und Zellen unterscheiden sich sowohl als auch in den elektrischen Werten oder der geometrischen bzw. konstruktiven Bauform. Von den nachfolgend aufgeführten Bezeichnungen können mehrere zusammen einen Batterietyp beschreiben, z. B. „Alkali-Mangan-Batterie – LR 6/AM-3 – AA – Mignon“. Oft wird aber nur ein bestimmtes Merkmal gefordert, z. B. die Größe „AA“ für eine speziell darauf abgestimmte Taschenlampe.
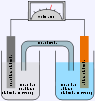
Im experimentellen Bereich und zur Veranschaulichung des Funktionsprinzips werden recht exotische Batterien, wie zum Beispiel Zitronenbatterien, eingesetzt.
Bestimmte Batterietypen haben eine breite Anwendung über die originäre Verwendung hinaus erfahren, wobei diese Originalprodukte heute (Stand 2009) bereits nicht mehr im Markt verfügbar sind.
Primärzellen
Als Primärzellen werden Batterien bezeichnet, die nach der Entladung nicht wieder neu aufgeladen werden können. Die verschiedenen Typen werden nach den eingesetzten Materialien bezeichnet (ausgenommen wiederaufladbare alkalische Zellen - diese werden trotzdem zu den Primärzellen gezählt):
- Alkali-Mangan-Batterie; 1,5 V Nennspannung pro Zelle
- Zink-Kohle-Batterie; 1,5 V pro Zelle
- Nickel-Oxyhydroxid-Batterie; 1,7 V pro Zelle
- Lithiumbatterien; je nach Kathodenmaterial 1,8 V (FeS2) bis 3,7 V (SOCl2)
- Lithium-Eisensulfid-Batterie; 1,5 V pro Zelle
- Zink-Luft-Batterie; 1,5 V pro Zelle
- Zinkchlorid-Batterie; 1,5 V pro Zelle
- Quecksilberoxid-Zink-Batterie; 1,35 V pro Zelle
- Silberoxid-Zink-Batterie; 1,55 V pro Zelle
- Natrium-Nickelchlorid-Batterie (Zebra-Batterie); 2,58 V pro Zelle
Historisch wurde zwischen Trockenbatterien mit festem oder gelartigem Elektrolyt und Nassbatterien, wie dem Daniell-Element mit flüssigem Elektrolyt, unterschieden. Nassbatterien spielen heute keine Rolle mehr.
Baugrößen
Als Gerätebatterien werden häufig Batterien bezeichnet, die sehr verbreitet für die Energieversorgung von Elektrokleingeräten wie Uhren, Radios, Spielzeug, Taschenlampen u.Ä. und auch in fest installierten Geräten wie Rauchmeldern verwendet werden.
Gerätebatterien müssen kompakt, lageunabhängig einsetzbar, leicht und trotzdem mechanisch robust sein. Sie dürfen bei normaler Lagerung und Verwendung im Gerät weder auslaufen noch ausgasen. Sie sind in einer Vielzahl von Ausführungen auf der Basis von Zink-Kohle- oder Alkali-Mangan-Batterie im Handel erhältlich. Ihre Bezeichnung folgt den von der IEC festgelegten Leistungsklassen[3] und den von der ANSI genormten Baugrößen.
Zink-Kohle-Batterien werden immer seltener angeboten und kaum noch hergestellt. Die am häufigsten verwendeten Batteriegrößen (sog. „Big-5“):
IEC
Alkali-Mangan
(Zink-Kohle)ANSI Bezeichnung Größe Nennspannung Ladung in mAh
Zink-KohleLadung in mAh
Alkali-ManganLR03 / AM-4
(R03 / UM-4)AAA Micro Ø 10,3 mm × H 45 mm 1,5 V 370…540 900…1.450 LR06 / AM-3
(R6 / UM-3)AA Mignon Ø 14,3 mm × H 51 mm 1,5 V 700…1.100 2.200…3.500 LR14 / AM-2
(R14 / UM-2)C Baby Ø 27 mm × H 50 mm 1,5 V 1.800…3.800 ≈ 8.000 LR20 / AM-1
(R20 / UM-1)D Mono Ø 35 mm × H 62 mm 1,5 V 4.000…8.000 8.500…20.700 6LR61 / AM-6
(6F22)1604D
PP3E-Block
9-V-BlockL 48,5 mm × B 26,2 mm × H 17 mm 9,0 V (beinhaltet 6 Zellen à 1,5 V)
6LR61 = 6× Rundzelle LR61
6F22 = 6× Flachzelle 22190…330 500…600 Hier nicht aufgeführt ist die ebenfalls genormte Größe SUB-C.
Neben diesen „Standardtypen“ gibt es noch eine große Formenvielfalt bei produktspezifischen Batterien, beispielsweise für Fotoapparate und bei Knopfzellen.
Batterien, die seltener eingesetzt werden und teilweise auch nur in Fachgeschäften erhältlich sind:
IEC
Alkali-Mangan
(Zink-Kohle)ANSI Bezeichnung Größe Nennspannung Ladung in mAh
Zink-KohleLadung in mAh
Alkali-ManganLR23 A R23 Ø 17 mm × H 50 mm 1,5 V LR61 AAAA Mini Ø 8,3 mm × H 42,5 mm 1,5 V 300 500…600 F Ø 33 mm × H 91 mm 1,5 V LR1 / AM-5
(R1 / UM-5)N Lady Ø 12 mm × H 30 mm 1,5 V ≈ 400 ≈ 800 2LR10
(2R10)Duplex Stabbatterie Ø 21,8 mm × H 74,6 mm 3,0 V
(beinhaltet 2 Zellen à 1,5 V)1.000…1.500 3LR12
(3R12 / 1203)Flachbatterie L 67 mm × B 62 mm × H 22 mm 4,5 V
(beinhaltet 3 Zellen à 1,5 V)≈ 1.800 ≈ 5.900 4LR61 J Flat Pack L 49 mm x B 36 mm × H 8,5 mm 6,0 V
(beinhaltet 4 Zellen à 1,5 V)500…600 (6F90) PP7 L 62,2 mm × B 46 mm × H 46 mm 9,0 V
(beinhaltet 6 Zellen à 1,5 V)ca. 2.000 (6F100) PP9 Blockbatterie L 80 mm × B 64,5 mm × H 51 mm 9,0 V
(beinhaltet 6 Zellen à 1,5 V)4.300 (4R25) 908D Laternenbatterie L 112 mm × B 66,7 mm × H 66,7 mm 6,0 V
(beinhaltet 4 Zellen à 1,5 V)8.500…9.500 8LR23
(MN21)1181A A23 Batterie Ø 10,3 mm × H 28,9 mm 12,0 V
(beinhaltet 8 Zellen à 1,5 V)≈ 33 Adapter und Kontaktierung
Nicht jeder Batterietyp ist in allen Ländern erhältlich. Deshalb gibt es zum Beispiel Flachbatterie-Adapter, die drei AA-Zellen zu je 1,5 V aufnehmen. Diese lassen sich in allen Geräten verwenden, in die auch eine Flachbatterie hineinpasst. Nützlich sind diese Adapter auch, weil es bis dato keine wiederaufladbaren Flachbatterien gibt.
Die Kontaktierung kleiner Batterien erfolgt mit Federkontakten, zuverlässigere Ausführungen für Lithiumbatterien sind vergoldet. Fest eingebaute Akkumulatoren sind mit Steckkontakten, Polbolzen oder Lötfahnen versehen.
Batteriepacks bestehen aus mehreren Zellen, die untereinander mit Blechbändern kontaktiert sind.
Microsoft offerierte 2010 eine „InstaLoad“ genannte, rein mechanische Lösung eines Batteriefaches, die das Einlegen von Batterie-Einzelzellen in beliebiger Orientierung erlaubt.
Entsorgung
Batterien und Akkumulatoren gehören nicht in den haushaltsüblichen Restmüllbehälter oder in die Umwelt, da sie umweltschädliche und zudem erneut nutzbare wertvolle Rohstoffe enthalten, die das Batterierecycling für entsprechende Unternehmen wirtschaftlich attraktiv machen.
In Deutschland regelt die Batterieverordnung die Rücknahme und Entsorgung von Batterien. Sie legt unter anderem fest, dass in Deutschland keine Batterien oder Zellen mit einem Quecksilbergehalt von mehr als 0,0005 Gewichtsprozent in den Verkehr gebracht werden dürfen. Bei Knopfzellen darf der Quecksilbergehalt nicht über 2,0 Gewichtsprozent liegen. Alkali-Mangan-Batterien enthalten seit Beginn der 1990er Jahre kein Quecksilber mehr. Davor wurde es zum Amalgamieren des Elektrodenmaterials Zink verwendet.
Kleine Batterien können in Deutschland in Einzelhandelsgeschäfte zurückgebracht werden, wenn diese auch Batterien verkaufen. Zu diesem Zweck müssen dort Sammelbehälter aufgestellt sein. Für Autobatterien existiert in Deutschland ein Pfandsystem.
Siehe auch
Literatur
- Lucien F. Trueb, Paul Rüetschi: Batterien und Akkumulatoren – Mobile Energiequellen für heute und morgen. Springer, Berlin 1998, ISBN 3-540-62997-1
- David Linden, Thomas B. Reddy (Hrsg.): Handbook of Batteries. 3. Auflage. McGraw-Hill, New York 2002, ISBN 0-07-135978-8 (englisch)
- Clive D.S. Tuck (Hrsg.): Modern Battery Technology. Ellis Horwood, New York 1991, ISBN 0-13-590266-5 (englisch)
- Philipp Brückmann: Autonome Stromversorgung - Auslegung und Praxis von Stromversorgungsanlagen mit Batteriespeicher. Ökobuch, Staufen 2007, ISBN 978-3-936896-28-2
- Werner Döring, Einführung in die Theoretische Physik, Band II, Berlin, Göschen 1965, speziell das Kapitel über Batterien
Einzelnachweise
- ↑ Grimsehl: Lehrbuch der Physik, Bd. II; Leipzig 1954, S. 38
- ↑ Dirk Flottmann, Detlev Forst, Helmut Roßwag: Chemie für Ingenieure: Grundlagen und Praxisbeispiele. Springer, 2003, ISBN 354006513X, S. 225
- ↑ IEC 60086 – allumfassende Norm der IEC für Primärbatterien
Weblinks
 Wiktionary: Batterie – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Wiktionary: Batterie – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen Commons: Batterien – Sammlung von Bildern, Videos und Audiodateien
Commons: Batterien – Sammlung von Bildern, Videos und Audiodateien- Geschichte der elektrischen Energiespeicherung
- Battery Chemistry FAQ (Englisch)
- Stiftung Gemeinsames Rücknahmesystem Batterien
- Technische Daten und Vergleichslisten für Knopfzellen und Batterien (PDF; 195 kB)
- Batteriegesetz vom 30. Juni 2009 (PDF)
- Allgemeine Hinweise für Akkus und Batterien (Entsorgung) (PDF)
- Kapazitätsmessung von Marken-Mignon-Batterien mit verschiedenen Stromstärken
Primärzellen: Alkali-Mangan-Batterie | Lithiumbatterie | Lithium-Eisensulfid-Batterie | Lithium-Mangandioxid-Batterie | Lithium-Thionylchlorid-Batterie | Lithium-Schwefeldioxid-Batterie | Lithium-Kohlenstoffmonofluorid-Batterie | Nickel-Oxyhydroxid-Batterie | Quecksilberoxid-Zink-Batterie | Silberoxid-Zink-Batterie | Zink-Braunstein-Zelle | Zinkchlorid-Batterie | Zink-Luft-Batterie
Sekundärzellen: Bleiakkumulator | Natrium-Schwefel-Akkumulator | Nickel-Cadmium-Akkumulator | Nickel-Eisen-Akkumulator | Nickel-Lithium-Akkumulator | Nickel-Metallhydrid-Akkumulator | Nickel-Wasserstoff-Akkumulator | Nickel-Zink-Akkumulator | Lithium-Eisen-Phosphat-Akkumulator | Lithium-Ionen-Akkumulator | Lithium-Mangan-Akkumulator | Lithium-Polymer-Akkumulator | Lithium-Schwefel-Akkumulator | Silber-Zink-Akkumulator | STAIR-Zelle | Vanadium-Redox-Akkumulator | Zink-Brom-Akkumulator | Zebra-Batterie | Zellulose-Polypyrrol-Zelle | Zinn-Schwefel-Lithium-Akkumulator
Historische Zellen: Daniell-Element | Gravity-Daniell-Element | Leclanché-Element | Voltasche Säule | Clark-Normalelement | Weston-Normalelement | Zambonisäule
Ausführungen: Akkumulator | Batterie | Brennstoffzelle | Knopfzelle | Konzentrationselement | Redox-Flow-Zelle | Thermalbatterie | Bestandteile: Halbzelle (Donator- und Akzeptorhalbzelle)
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Batterie — Das Wort Batterie steht für verschiedene Begriffe, denen im allgemeinen eine regelmäßige geometrische Formation von mehreren, meist gleichen Objekten zugrunde liegt: Batterie (Elektrotechnik) – Zusammenschaltung mehrerer galvanischer Primärzellen … Deutsch Wikipedia
Elektrotechnik — ist diejenige Technikwissenschaft, die sich ingenieurwissenschaftlich mit der Forschung und der technischen Entwicklung sowie der Produktionstechnik von Geräten oder Verfahren befasst, die zumindest anteilig auf elektrischer Energie beruhen.… … Deutsch Wikipedia
Batterie — Ansammlung; Konzentration * * * Bat|te|rie [batə ri:], die; , Batterien [batə ri:ən]: 1. kleinste militärische Einheit bei der Artillerie. 2. a) Zusammenschaltung mehrerer gleichartiger technischer Geräte (z. B. Stromquellen). b) Stromquelle, die … Universal-Lexikon
Nickel-Metallhydrid-Batterie — von VARTA Ein Nickel Metallhydrid Akkumulator (NiMH) ist ein Akkumulator, der mechanisch baugleich zu handelsüblichen Batterien hergestellt wird. Diese Teile werden üblicherweise in das Batteriefach des mit Strom zu versorgenden Gerätes eingelegt … Deutsch Wikipedia
Akkumulator (Elektrotechnik) — 12 V „Autobatterie“ aus sechs Sekundärzellen Ni MH Akkumulator im Standardformat „AA“ … Deutsch Wikipedia
Liste Persönlichkeiten der Elektrotechnik — Liste von Persönlichkeiten, die Beiträge im Bereich der Elektrotechnik geleistet haben: Inhaltsverzeichnis A B C D E F G H I J K L M N O P Q R S T U V W X Y Z … Deutsch Wikipedia
Kondensator (Elektrotechnik) — Prinzipdarstellung eines Kondensators mit Dielektrikum Ein Kondensator (von lateinisch condensare ‚verdichten‘) ist ein passives elektrisches Bauelement mit der Fähigkeit, elektrische Ladung und damit zusammenhängend Energie zu speichern.… … Deutsch Wikipedia
VDE Verband der Elektrotechnik Elektronik Informationstechnik — Verband der Elektrotechnik, Elektronik und Informationstechnik e.V. (VDE) Zweck: Technisch wissenschaftlicher Verband Vorsitz: Dr. Ing. Joachim Schneider Gründungsdatum: 21. Januar 1893 Mitgliederzahl: ca … Deutsch Wikipedia
VDE Verband der Elektrotechnik Elektronik Informationstechnik e.V. — Verband der Elektrotechnik, Elektronik und Informationstechnik e.V. (VDE) Zweck: Technisch wissenschaftlicher Verband Vorsitz: Dr. Ing. Joachim Schneider Gründungsdatum: 21. Januar 1893 Mitgliederzahl: ca … Deutsch Wikipedia
Verband der Elektrotechnik Elektronik Informationstechnik — Verband der Elektrotechnik, Elektronik und Informationstechnik e.V. (VDE) Zweck: Technisch wissenschaftlicher Verband Vorsitz: Dr. Ing. Joachim Schneider Gründungsdatum: 21. Januar 1893 Mitgliederzahl: ca … Deutsch Wikipedia