- Bromcyan
-
Strukturformel 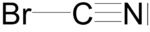
Allgemeines Name Bromcyan Andere Namen - Cyanogenbromid
- Cyanobromid
- Bromcyanid
Summenformel BrCN CAS-Nummer 506-68-3 Kurzbeschreibung farblose, flüchtige Nadeln[1]
Eigenschaften Molare Masse 105,9 g·mol−1 Aggregatzustand fest
Dichte Schmelzpunkt Siedepunkt 61,4 °C [2]
Dampfdruck Löslichkeit löslich in Wasser, Ethanol und Diethylether [3]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [4] 


Gefahr
H- und P-Sätze H: 300-310-314-330-410 EUH: keine EUH-Sätze P: 260-264-273-280-284-302+350 [4] EU-Gefahrstoffkennzeichnung [2] 

Sehr giftig Umwelt-
gefährlich(T+) (N) R- und S-Sätze R: 26/27/28-34-50 S: 9-15-26-28-36/37/39-45-61 LD50 LC50 (human, inhalativ): 92 ppm in 10 min [5]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Bromcyan ist ein Derivat der Blausäure (HCN), bei dem das Wasserstoffatom durch Brom ersetzt ist. Umgangssprachlich wird es auch Bromcyanid oder Campilit genannt.
Inhaltsverzeichnis
Darstellung und Gewinnung
Die Darstellung von Bromcyan gelingt durch die Umsetzung von Brom mit Natriumcyanid in wäßriger Lösung bei Temperaturen unterhalb von 20 °C.[6][7] Eine weitere Synthese geht vom Kaliumthiocyanat oder Ammoniumthiocyanat aus.[8]
Eigenschaften
Bromcyan ist noch um ein vielfaches giftiger als Kaliumcyanid (KCN). Seine außerordentliche Giftwirkung beruht auf den beiden Komponenten Brom und Cyanid, die sowohl durch enzym-inhibitorische Eigenschaften als Stoffwechselgift, als auch toxisch auf Nervenzellen wirken.[2]
Bromcyan liegt in Form von leicht flüchtigen Nadeln vor. Mit einer molaren Bildungswärme von 185,6 kJ/mol für Bromcyandampf bzw. 140,4 kJ/mol für den Feststoff handelt es sich um eine instabile endotherme Verbindung,[9] Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in kPa, T in K) mit A = 3,53667, B = 727,385 und C = −130.052 im Temperaturbereich von 273 K bis 313 K.[9]
In Natronlauge erfolgt die Hydrolyse zu Natriumcyanat und Natriumbromid. Die Reaktion verläuft mit einer Reaktionswärme von −235 kJ·mol-1 stark exotherm.[9]
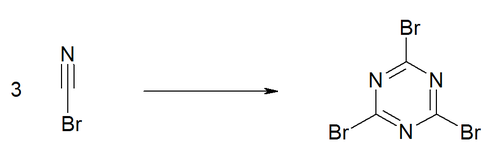
Bei höheren Temperaturen und in Gegenwart von Aluminiumbromid erfolgt eine Trimerisierung zum Cyanurbromid.[10]
Struktur
Das BrCN-Molekül besitzt eine lineare Struktur. Die Bindungslängen der Br-C-Bindung bzw. der C-N-Bindung sind typisch für eine C-Br-Einfachbindung bzw. C-N-Dreifachbindung. Die Bindungslängen betragen für die C–Br–Bindung 1,789 Angstroem, für die C–N–Bindung 1,160 Angstroem.[11] Das Bromcyanmolekül ist polar. Das Dipolmoment beträgt 2,94 D.[12]
Verwendung
Bromcyan wird vorwiegend in der Goldlaugerei verwendet. In der Biochemie wird es für die Sequenzierung von Proteinen eingesetzt. Bromcyan spaltet selektiv C-terminal nach der Aminosäure Methionin. Dadurch wird das Protein in kürzere Fragmente zerlegt, welche mit anderen Analysetechniken z. B. dem Edman-Abbau analysiert werden.
Sicherheitshinweise
Gasförmiges Bromcyan wird über die Haut kaum, über Atemwege und Verdauungstrakt gut resorbiert. Es kann beim Kontakt mit Wasser und Magensäure oder beim Erhitzen zu Cyanwasserstoff, Bromwasserstoff, Dicyan und Cyanurbromid hydrolysiert oder zersetzt werden. Auf Augen, Haut und Schleimhäute wirkt Bromcyan sehr stark reizend bis ätzend. Im Gegensatz zu Blausäure wird es bei Anwesenheit in der Luft ab 1 ppm als reizend wahrgenommen; bei etwa 9 ppm liegt die „Erträglichkeitsgrenze“.[2]
Einzelnachweise
- ↑ Römpp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b c d e f g Eintrag zu Bromcyanid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. September 2007 (JavaScript erforderlich).
- ↑ enius.de.
- ↑ a b Datenblatt Bromcyan bei Sigma-Aldrich, abgerufen am 14. März 2011.
- ↑ Bromcyan bei ChemIDplus.
- ↑ K.H. Slotta: Bromcyan und wasser-freie Blausäure in Chem. Ber. 67 (1934) 1028-1030. doi:10.1002/cber.19340670622.
- ↑ Hartmann, W.W., Dreger, E.E.: Organic Syntheses, Coll. Vol. 2, p.150 (1943); Vol. 11, p.30 (1931).pdf-Datei.
- ↑ W. König: J. Prakt. Chem. (Leipzig) 84 (1911) 558–560.
- ↑ a b c Lord, G.; Woolf, A.A., The cyanogen halides. Part III. Their heats of formation and free energies in J. Chem. Soc., 1954, 2546-2551.
- ↑ F. Oberhauser,Das Verhalten des Bromcyans gegenüber Metallsalzen in Chem. Ber. 60 (1927) 1434-1439 doi:10.1002/cber.19270600628.
- ↑ A. G. Smith, H. Ring, W. V. Smith, W. Gordy: Interatomic Distances and Nuclear Quadrupole Couplings in ClCN, BrCN, and ICN in Phys. Rev. 74 (1948) 370–372. doi:10.1103/PhysRev.74.370.
- ↑ J.K. Tyler, J. Sheridan: Structural studies of linear molecules by microwave spectroscopy in Trans. Faraday Soc. 59 (1963) 2661–2670. doi:10.1039/TF9635902661.
Kategorien:- Giftiger Stoff
- Umweltgefährlicher Stoff
- Bromverbindung
- Nitril
- Pseudohalogen
Wikimedia Foundation.