- Diphenylphosphan
-
Strukturformel 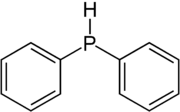
Allgemeines Name Diphenylphosphan Andere Namen Diphenylphosphin
Summenformel C12H11P CAS-Nummer 829-85-6 PubChem 70017 Kurzbeschreibung farblose Flüssigkeit[1]
Eigenschaften Molare Masse 186,19 g·mol−1 Aggregatzustand flüssig
Dichte Schmelzpunkt Siedepunkt 280 °C[1]
Dampfdruck Brechungsindex 1,626[3]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 

Gefahr
H- und P-Sätze H: 250-315-319-335 EUH: keine EUH-Sätze P: 222-231-261-305+351+338-422 [1] EU-Gefahrstoffkennzeichnung [1] 

Leicht-
entzündlichReizend (F) (Xi) R- und S-Sätze R: 17-36/37/38 S: 26-36 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C Diphenylphosphin ist eine chemische Verbindung aus der Gruppe der Phosphane.
Inhaltsverzeichnis
Herstellung
Diphenylphosphan kann durch die Hydrierung von Chlordiphenylphosphan mit Lithiumaluminiumhydrid erhalten werden.
Auch die Reaktion von Triphenylphosphan mit elementarem Lithium liefert Diphenylphosphan.[4]

- Reaktion von Triphenylphosphan mit Lithium zu Dipenylphosphan. Durch wässrige Aufarbeitung werden aus den lithiierten Verbindungen die Produkte freigesetzt. Ph = Phenyl
Eigenschaften
Diphenylphosphin ist eine farblose Flüssigkeit die bei −14,5 °C schmilzt und bei 280 °C siedet. Diphenylphosphin reagiert als sehr schwache Säure nur mit starken Basen zum Diphenylphosphid-Anion, das durch Mesomerie stabilisiert ist.
Verwendung
Das Anion von Diphenylphosphin (Ph2P–) kann durch die Umsetzung mit basischen Salzen von beispielsweise Kalium- oder Lithium erhalten werden. Das Anion kann als Nukleophil in Substitutionsreaktionen eingesetzt werden. Dieses wird beispielsweise zur Synthese von Phosphanliganden wie dppm[5] oder dppp[6] verwendet.
Einzelnachweise
- ↑ a b c d e f g Datenblatt Diphenylphosphine bei Sigma-Aldrich, abgerufen am 28. März 2011.
- ↑ E. Wiberg, M. van Ghemen, G. Müller-Schiedmayer: Neues aus der Chemie der Polyphosphane, in: Angew. Chem., 1963, 75, S. 814–823.
- ↑ H. R. Hudson, A. R. Qureshi, D. Ragoonanan: Factors in the formation of isomerically and optically pure alkyl halides. Part IX. Reactions of (1-substituted n-alkyl) diphenylphosphinites with hydrogen halides and with halogens, in: J. Chem. Soc., Perkin Trans. 1, 1972, S. 1595–1597.
- ↑ D. Wittenberg, H. Gilman: Lithium Cleavages of Triphenyl Derivatives of Some Group Vb Elements in Tetrahydrofuran, in: J. Org. Chem., 1958, 23, S. 1063–1065.
- ↑ E. N. Tsvetkov, N. A. Bondarenko, I. G. Malakhova, M. I. Kabachnik, in: Synthesis, 1986, 3, S. 198–208.
- ↑ M. T. Honaker, B. J. Sandefur, J. L. Hargett, A. L. McDaniel, R. N. Salvatore, in: Tetrahedron Lett., 2003, 44, 46, S. 8373–8378.
Kategorien:- Feuergefährlicher Stoff
- Reizender Stoff
- Phenylphosphan
Wikimedia Foundation.
