- Aerobe Atmung
-
Übergeordnet Zellatmung Untergeordnet Atmungskette
Aerobe Atmung mit Elektronendonor:
Nitrit
Arsenit
Ammonium
Kohlenstoffmonoxid
Eisenionen
Wasserstoff
Schwefel/SulfatGene Ontology AmiGO QuickGO Als aerobe Atmung (Zellatmung, innere Atmung) werden Stoffwechselprozesse in Zellen von Lebewesen bezeichnet, bei denen die durch verschiedene oxidative Stoffwechselvorgänge anfallenden und an speziellen Überträgern gebundenen Wasserstoffatome oxidiert werden. Hierbei dient molekularer, elementarer Sauerstoff (O2) als Oxidationsmittel, welches dabei zu Wasser reduziert wird. Der Zweck der aeroben Atmung ist die Erzeugung von Energie in Form von Adenosintriphosphat (ATP). Die Bezeichnung aerobe Atmung wird insbesondere für die biochemischen Vorgänge der Atmungskette in der inneren Membran der Mitochondrien verwendet, an deren Ende ATP synthetisiert wird.
Andere Formen der Atmung – im Sinne des Gasaustausches von Lebewesen – werden unter dem Begriff der äußeren Atmung zusammengefasst.
Inhaltsverzeichnis
Übersicht
- Der Einheitlichkeit halber werden für Säuren als Zwischenstufen – wie in der Biochemie üblich – die Namen ihrer Anionen verwandt („Pyruvat“ statt „Brenztraubensäure“).
Im Folgenden wird die Nutzung der Energie aus der Oxidation von D-Glucose (Traubenzucker) durch Zellen dargestellt. Zellen können Energie auch durch Oxidation anderer Stoffe gewinnen, die Oxidation von Glucose ist jedoch die am häufigsten genutzte Energiequelle.
Zellen nehmen zu ihrer Energieversorgung Glucose auf. Sie wird von Eukaryoten im Cytoplasma und in den Mitochondrien vollständig zu Kohlenstoffdioxid und Wasser oxidiert. Die Summengleichung lautet:

- Aus einem Molekül Glucose und sechs Molekülen Sauerstoff werden sechs Moleküle Kohlenstoffdioxid und sechs Moleküle Wasser.
Die Änderung der Freien Enthalpie unter Standardbedingungen beträgt jedoch bei pH = 7 für diese Reaktion ΔG0' = −2880 kJ je Mol Glucose[1]. Weichen die tatsächlichen Bedingungen von diesen Standardbedingungen ab, so ist auch der Betrag der Änderung der Freien Enthalpie ein anderer, er kann erheblich vom Standardwert abweichen. In lebenden Systemen sind Standardbedingungen in der Regel nicht gegeben und ändern sich oft auch während der Stoffumsetzung. Der Betrag der Änderung der Freien Enthalpie unter Standardbedingungen bietet also bei Lebewesen lediglich einen Anhaltspunkt für die bei einer chemischen Stoffumsetzung frei werdende Energie.
Bei dieser chemischen Stoffumsetzung werden in einer Reihe von komplizierten Reaktionsschritten – darunter viele Redoxreaktionen – Wasserstoffatome von den Abbauprodukten der Glucose-Moleküle abgetrennt und mit Hilfe von Wasserstoffüberträgern (Nicotinamid-Adenin-Dinucleotid, NAD) zu den Mitochondrien transportiert. Dort reagieren die Wasserstoffatome in der Atmungskette mit Sauerstoff zu Wasser (gelegentlich, nicht ganz zutreffend, als „biologische Knallgasreaktion“ bezeichnet); die Glucose-Moleküle werden letztlich vollständig oxidiert. Am Ende des Abbauprozesses gewinnt die Zelle mit Hilfe der bei der biologischen Wasserstoff-Oxidation frei werdenden Energie die energiereiche Verbindung Adenosintriphosphat (ATP). Sie dient als Energieüberträger und kurzfristiger Energiespeicher und ist für viele Stoffwechselvorgänge als universelle Energiequelle erforderlich.
Die zusammenfassende Reaktionsgleichung der Zellatmung entspricht von rechts nach links gelesen der Reaktionsgleichung für die oxygene Photosynthese.
Ablauf des Prozesses
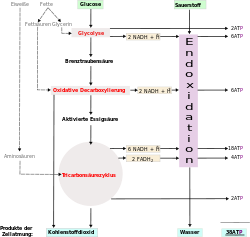
Die Zellatmung ist ein Prozess, bei dem energiereiche in energiearme Stoffe umgesetzt werden. Im Fall der Zellatmung wird meistens das Glucosemolekül C6H12O6 in einer längeren Reihe von Schritten zu C1-Körpern (CO2) und Wasser (H2O) oxidiert. Dieser Abbau kann in vier Abschnitte unterteilt werden:
- die Glykolyse,
- die oxidative Decarboxylierung,
- den Citratzyklus und
- die Endoxidation in der Atmungskette.
Die Gesamtbilanz der Zellatmung kann folgendermaßen formuliert werden:

- Aus einem Molekül Glucose und sechs Molekülen Sauerstoff werden sechs Moleküle Kohlenstoffdioxid und sechs Moleküle Wasser.
Glykolyse
→ Hauptartikel: Glykolyse
Die Glykolyse (= Zuckerzerlegung) läuft im Cytoplasma ab. Bei diesem Vorgang wird D-Glucose gespalten. Dies geschieht durch zweifache Phosphorylierung, so dass Glucose-6-phosphat Fructose-6-phosphat und dann Fructose-1,6-bisphosphat entsteht. Für diese Prozesse werden 2 Moleküle ATP zu 2 Molekülen ADP dephosphoryliert. Durch die Phosphorylierung der Glucose ist sie nun im aktivierten Zustand. Dieser C6-Körper wird dann in zwei C3-Körper gespalten, in ein Molekül Dihydroxyacetonphosphat (DHAP) und ein Molekül Glycerinaldehyd-3-phosphat (GAP). Nur das Glycerinaldehyd-3-phosphat wird weiter abgebaut, deswegen wird das DHAP in dieses isomerisiert.
Ein weiteres Molekül anorganischen Phosphates wird angelagert und GAP wird oxidiert, wodurch Glycerinsäure-1,3-biphosphat (1,3bPG) entsteht. Die Elektronen werden auf den Wasserstoffüberträger NAD+ (Nicotinamidadenindinukleotid) übertragen. Im weiteren Schritt wird ein Phosphatrest (Pi) auf ADP übertragen, so dass ATP und Glycerinsäure-3-phosphat (3-PG) entstehen. 3-PG wird zu Glycerinsäure-2-phosphat (2-PG) isomerisiert. Durch Abspaltung von Wasser entsteht daraus Phosphoenolpyruvat (PEP). In diesem letzten Schritt der Glykolyse wird auch der letzte Phosphatrest auf ADP übertragen, so dass Pyruvat und ATP entstehen. Auf dem Weg von GAP zum Pyruvat werden also je Molekül GAP zwei Moleküle ATP durch Phosphorylierung von ADP gebildet.
Nettobilanz der Glykolyse:
Oxidative Decarboxylierung
→ Hauptartikel: Oxidative Decarboxylierung
Die oxidative Decarboxylierung ist ein kurzer Schritt, der allerdings unabdingbar für den darauf folgenden Schritt ist. Sie läuft bei Eukaryoten in der Mitochondrienmatrix ab. Aus dem Pyruvat wird durch einen mehrstufigen Reaktionsmechanismus ein CO2 abgespalten (Decarboxylierung) und 2 H-Atome auf NAD+ übertragen (Redoxreaktion) sowie das dadurch entstehende Acetat an das Coenzym A (CoA) gebunden, so dass Acetyl-CoA entsteht.
Bilanz der Oxidativen Decarboxylierung:
Citratzyklus
→ Hauptartikel: Citratzyklus
Der Citratzyklus, auch als Citronensäurezyklus oder Tricarbonsäurezyklus bezeichnet, ist nach dem ersten Zwischenprodukt benannt, dem Citrat, dem Anion der Citronensäure.
Im letzten Schritt des Citratzyklus entsteht Oxalacetat. Dieses kondensiert mit Acetyl-CoA zu Citrat – durch Aufnahme von Wasser und Abspaltung von Coenzym A. Dabei wird also das Coenzym A wieder regeneriert. Dann wird CO2 abgespalten und Wasserstoff vom Wasserstoffüberträger NAD übernommen (Bildung von NADH), so dass α-Ketoglutarat gebildet wird. Im nächsten Schritt wird mit Hilfe von Coenzym A erneut CO2 abgespalten und Wasserstoff auf NAD übertragen. Die nächsten Schritte dienen nur noch der Regenerierung von Oxalacetat, damit der Zyklus wieder von vorn beginnen kann. Dies geschieht über die Moleküle Succinyl-CoA, Succinat, Fumarat, L-Malat.
Bilanz des Citratzyklus (läuft je Molekül Glucose zweimal ab, da aus 1 Mol Glucose 2 Mol Pyruvat und somit auch 2 Mol Acetyl-Coenzym A gebildet werden):
Endoxidation in der Atmungskette
Durch den bisherigen Prozess sind 4 ATP entstanden. Den größten Teil der ATP-Ausbeute liefert jedoch die Atmungskette durch Oxidation der an die Wasserstoffüberträger NAD und FAD gebundenen Wasserstoffatome mit Sauerstoff (O2). Insgesamt stehen 10 NADH (2 aus der Glykolyse, 2 aus der oxidativen Decarboxylierung und 6 (2 mal 3) aus dem Citratzyklus) und 2 FADH2 (Flavinadenindinukleotid) zur Verfügung, also 24 Reduktionsäquivalente.
Ein NADH gibt 2 Elektronen (e−) ab, wodurch der am NAD gebundene Wasserstoff als Proton (H+) frei wird und das verbleibende NAD-Molekül positiv geladen wird: NAD+. Weil die so abgegebenen 2 Elektronen auf einem recht hohen Energieniveau liegen (sehr niedriges Redoxpotential des Redoxpaares NADH/NAD+), können mit ihrer Hilfe 10 Protonen aus der Matrix in den Intermembranraum transportiert werden. Dies geschieht folgendermaßen: Die 2 Elektronen des NADH reduzieren den ersten Komplex (Komplex I) von mehreren Enzym-Komplexen der Atmungskette, die sich zwischen Matrix und Intermembranraum des Mitochondriums befinden. Jedes Elektron wird nun über Redoxreaktionen von einem Enzym-Komplex zum nächsten weitergegeben. Aufgrund der Weitergabe von Elektronen von Komplex zu Komplex wird dieser Vorgang auch als Elektronentransportkette bezeichnet. Durch den Komplex I, den Komplex III und den Komplex IV werden H+-Ionen (Protonen) aus der Matrix in den Intermembranraum transportiert. Im Intermembranraum entsteht auf diese Weise eine hohe Wasserstoffionen-Konzentration, wodurch ein pH-Wert unter 7 entsteht, und sich ein osmotisches Potential bildet. Die Redoxreaktionen und die Entstehung des osmotischen Potentials zusammen werden Chemiosmose genannt: Die Redoxreaktionen sind chemische Umsetzungen, der Unterschied der H+-Konzentrationen von Matrix und Intermembranraum stellt ein osmotisches Potential dar.
Die Protonen fließen schließlich durch die membrangebundene ATP-Synthase vom Intermembranraum in den Matrixraum zurück. Dieses Enzym katalysiert die Synthese von ATP aus einem Phosphatrest und ADP. Die in der protonenmotorischen Kraft steckende Durchflussenergie wird dazu genutzt, dass entstandenes ATP von der ATP-Synthase freigesetzt wird. Der Transport eines Moleküls ADP aus dem Cytoplasma in die Matrix bzw. umgekehrt der Transport eines Moleküls ATP in das Cytoplasma wird durch eine ATP/ADP-Translokase katalysiert. Für diesen Transport wird jedoch auch der Protonengradient angezapft, so dass für die Verfügbarkeit von ATP bzw. ADP ein Proton verbraucht wird. Damit müssen mindestens 4 Protonen für die Erzeugung eines Moleküls ATP berechnet werden.
Durch die Oxidation von einem NADH entstehen somit 2,5 ATP. Ausnahme sind die zwei NADH aus der Glykolyse. Diese befinden sich noch im Cytoplasma und müssen erst in die Mitochondrien transportiert werden. Erfolgt dies mit Hilfe des Glycerin-3-Phosphat-Shuttles, gewinnt man aus diesen nur je 1,5 ATP. Da 8 + 2 NADH oxidiert werden, entstehen insgesamt 8 × 2,5 + 2 × 1,5 = 23 ATP.[2] Wird jedoch cytosolisches NADH durch den Malat-Aspartat-Shuttle in die Matrix gebracht, können aus diesen Reduktionsäquivalenten analog je 2,5 mol ATP erzeugt werden. Damit können maximal 10 × 2,5 = 25 ATP erzeugt werden.[3]
Mit dem FADH2 verläuft der Vorgang im Prinzip genauso, nur gibt FADH2 auf einem höheren Redoxpotential und damit niedrigeren Energieniveau Elektronen ab. Dessen Elektronen können also erst auf einer energetisch niedriger stehenden Stufe in die Atmungskette eingeschleust werden. Deshalb können mit Hilfe der Elektronen des FADH2 nur 4 Protonen aus der Matrix in den Intermembranraum gepumpt werden. Mit einem FADH2 werden infolgedessen nur 1,5 ATP gebildet. Da zwei FADH2 oxidiert werden, entstehen dabei 3 ATP.[2]
Die Protonen und die Elektronen des NADH und des FADH2 (insgesamt 24) werden zusammen mit 6 Molekülen O2, die durch die Membran in die Mitochondrienmatrix transportiert werden, zu 12 H2O oxidiert. Die Elektronen- bzw. Wasserstoffüberträger NAD+ und FAD können durch Aufnahme von je 2 e– und 2 H+ wieder zu NADH bzw. FADH2 reduziert werden.
Bilanz der Atmungskette:
Energiebilanz
Schritt Coenzym-Ausbeute ATP-Ausbeute ATP-Quelle Glykolyse Vorbereitungsstufe −2 für die Zerlegung der Glucose in 2 Moleküle Glycerinaldehyd-3-phosphat verbrauchte Energie Glykolyse Ertragsstufe 4 Substratkettenphosphorylierung 2 NADH 3 Oxidative Phosphorylierung Oxidative Decarboxylierung 2 NADH 5 Oxidative Phosphorylierung Citratzyklus 2 Substratkettenphosphorylierung (in Form von GTP) 6 NADH 15 Oxidative Phosphorylierung 2 FADH2 3 Oxidative Phosphorylierung Gesamtausbeute 30 ATP[3][2]–32 ATP[3] pro Molekül Glucose (Glycerin-3-phosphat-Shuttle bzw. Malat-Aspartat-Shuttle) Da Prokaryoten keine Zellkompartimente besitzen, müssen sie nicht Energie für intrazelluläre Transportvorgänge ausgeben. Daher können sie maximal 38 Moleküle ATP aus einem Molekül Glucose erzeugen.[3]
Einzelnachweise
- ↑ R. Wehner, W. Gehring: Zoologie. 24. Auflage. Georg Thieme Verlag, Stuttgart, New York 2007, ISBN 978-3-13-367424-9.
- ↑ a b c d e Berg, Stryer, Tymoczko: Biochemie. Spektrum Akademischer Verlag, 2007, ISBN 978-3-8274-1800-5
- ↑ a b c d Reginald Garrett und Charles M. Grisham: Biochemistry. (International Student Edition). Thomsom Learning Inc.; 3. Auflage 2005; ISBN 0-534-41020-0; S. 669f.
Literatur
- Reginald Garrett und Charles M. Grisham: Biochemistry. 3. Auflage (International Student Edition). Thomsom Learning Inc., 2005, ISBN 0-534-41020-0, S. 640–674
- Geoffrey Zubay: Biochemie. 4. Auflage. Mcgraw-Hill Professional, 1999, ISBN 3-89028-701-8
- Donald Voet und Judith G. Voet: Biochemie. Wiley-VCH, 1994, ISBN 3-527-29249-7, S. 420ff.
- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Biochemie. 6 Auflage. Spektrum Akademischer Verlag, Heidelberg 2007; ISBN 978-3-8274-1800-5
- H. Robert Horton, Laurence A. Moran, K. Gray Scrimgeour, Marc D. Perry, J. David Rawn und Carsten Biele (Übersetzer): Biochemie. 4., aktualisierte Auflage. Pearson Studium, 2008, ISBN 978-3-8273-7312-0
- David L. Nelson, Michael M. Cox, Albert L. Lehninger (Begr.): Lehninger Biochemie. 4., vollst. überarb. u. erw. Auflage. Springer, Berlin 2009, ISBN 978-3-540-68637-8
Kategorien:- Biologischer Prozess
- Zellbiologie
- Stoffwechsel
Wikimedia Foundation.