- E. coli
-
Escherichia coli Systematik Abteilung: Proteobacteria Klasse: Gamma Proteobacteria Ordnung: Enterobacteriales Familie: Enterobacteriaceae Gattung: Escherichia Art: Escherichia coli Wissenschaftlicher Name Escherichia coli (Migula 1895) Castellani & Chalmers 1919 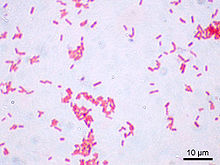 E. coli in der Gramfärbung.
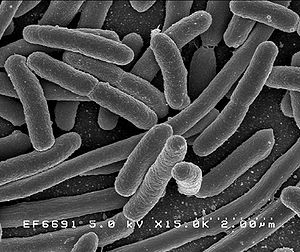
E. coli in der Gramfärbung.Escherichia coli (abgekürzt E. coli) ist ein säurebildendes (Laktose-positiv), gramnegatives, stäbchenförmiges, Oxidase-negatives und peritrich begeißeltes Bakterium, das im menschlichen und tierischen Darm vorkommt. Es gehört zur Familie der Enterobacteriaceae (griech. „enteron“: Darm). Benannt wurde es 1919 nach seinem Entdecker Theodor Escherich. Es gehört zu den am besten untersuchten Organismen der Welt.
Inhaltsverzeichnis
Merkmale
E. coli gehört zu den fakultativ anaeroben Mikroorganismen und besitzt die Fähigkeit, Energie sowohl durch Atmung als auch durch „Gemischte Säuregärung“ zu gewinnen. Es dient als Indikator für fäkale Verunreinigungen, zum Beispiel von Wasser. Es veranlasst ein dauerndes Training des Mukosa-Immunsystems und fördert die Produktion von sekretorischem Immunglobulin A. Weiterhin produziert es Vitamin K.
Die verschiedenen Serotypen von Escherichia coli erschweren die Immunantwort. Man unterscheidet drei Gruppen von Serotypen: „O“ für die Lipopolysaccharide, „H“ (von „mit Hauch wachsende Bakterien“) für die Flagellen und eventuell „K“ für die Kapsel. Es gibt circa 180 „O“-Serogruppen und circa 50 „H“-Typen bei E. coli.
Ernährung
Diese Bakterien ernähren sich bevorzugt von Zucker und bestimmten Aminosäuren.
Bewegung
Diese Organismen können sich gezielt in Richtung einer Anhäufung von Nährstoffen bewegen. Andererseits ist es ihnen auch möglich, Säuren und hohen Salzkonzentrationen auszuweichen, die sie eventuell schädigen könnten. Zunächst schwimmen sie dabei in irgendeine Richtung und messen zugleich eine mögliche Veränderung der Nährstoffkonzentration. Im Falle einer Erhöhung derselben bewegen sich die Bakterien anhaltend in der eingeschlagenen Richtung. Bei einer Verringerung wird diese Bewegungsrichtung früher geändert. Deshalb gleicht ihre Bewegungsspur insgesamt einer Zickzacklinie.
Die Registrierung der Nährstoffe erfolgt durch etwa 15 000 Rezeptormoleküle, welche sich an den Enden des ungefähr zwei Mikrometer großen Organismus befinden. Sollten diese Rezeptoren Nährstoffe feststellen, schicken sie Signale zu sogenannten Motorproteinen, welche 20 Mikrometer lange fadenförmige Geißeln (auch Flagellen genannt) drehen und damit das Bakterium voranbringen. Drehen sich diese Fäden gegen den Uhrzeigersinn, so wickeln sie sich zu Spiralen auf und wirken als Propeller. Wenn sie sich jedoch in entgegengesetzter Richtung drehen, dann taumelt das Bakterium und ändert dadurch seine Richtung.
Chemotaxis
Das Bakterium ist in der Lage, das Signal der Rezeptoren um den Faktor 100 intern zu verstärken. 2005 haben Forscher herausgefunden, wie die Signalübertragung zur Steuerung der Bewegungsrichtung funktioniert. Das Schwimmverhalten von E. coli wird durch das Antwortregulatorprotein CheY gesteuert. Ist eine Phosphatgruppe an das CheY-Protein gebunden, entspricht diese Tatsache dem Signal „Die gegenwärtige Richtung ist schlecht.“ Fehlt dort das Phosphat, wird damit das Gegenteil signalisiert. Abhängig von der Anzahl der phosphorylierten CheY-Proteine drehen die Motorproteine in die eine oder in andere Richtung. Ist viel phosphoryliertes CheY am Motor gebunden, dann dreht er sich im Uhrzeigersinn, was die Zelle taumeln lässt. Ist wenig phosphoryliertes CheY am Motor gebunden, dann dreht er sich im Gegenuhrzeigersinn, was zu einer vorwärtsgerichteten Schwimmbewegung führt.
Die Aufnahme der Umweltreize erfolgt durch so genannte methylierbare Chemotaxisproteine (methyl accepting chemotaxis proteins; MCPs), welche über Transmembranhelices in der Membran verankert sind. Die MCPs besitzen eine periplasmatische Bindestelle für Chemikalien sowie eine intrazelluläre Signaldomäne und intrazelluläre Methylierungsstellen. Durch Bindung von Chemikalien entsteht in den MCPs ein Signal, das sich über die Membran hinweg fortpflanzt und von der Signaldomäne der MCPs weitergeleitet wird. Die Weiterverarbeitung des Signals erfolgt durch ein Zweikomponentensystem bestehend aus einer Histidinkinase CheA und einem Antwortregulatorprotein CheY. Auf dieser Ebene erfolgt die Integration von Reizen verschiedensten Ursprungs (pH-Wert, Sauerstoff- oder Nährstoffkonzentration u. a.) in ein einziges, eindeutiges Signal. Zwei Moleküle CheA binden über zwei Adaptermoleküle CheW an ein MCP-Dimer. Wird ein Schreckstoff an ein MCP gebunden, so wird die Sensorkinase CheA aktiviert. Sie wird zu CheA-P autophosphoryliert und phosphoryliert ihrerseits CheY zu CheY-P. CheY-P diffundiert dann zum Flagellarmotor und löst dort Rotation des Flagellarmotors im Uhrzeigersinn aus, was die Zelle taumeln lässt. Um die Akkumulation von CheY-P zu verhindern beschleunigt CheZ den Zerfall von CheY-P. Wird ein Lockstoff an ein MCP gebunden, wird die CheA Aktivität unterdrückt, die Zahl an CheY-P Moleküle sinkt und die Häufigkeit des Taumelns.
Dieser Mechanismus erklärt aber noch nicht, warum die Zelle immer nur auf Stoffgradientenänderungen von Lock- bzw. Schreckstoffen anspricht. Es muss daher eine Adaptation stattfinden. Die Adaptation erfolgt durch Methylierung bzw. Demethylierung der MCP-Methylierungsstellen. Die Methyltransferase CheR überträgt durch das Methylierungsreagenz S-Adenosylmethionin Methylgruppen auf Glutamatreste. Aktiviertes CheA phosphoryliert nicht nur sich selbst und CheY, sondern auch die Methylesterase CheB zu CheB-P. CheB-P demethyliert die Methylbindungsstellen. Bei einer gleichbleibenden Lockstoffkonzentration ändert sich im zeitlichen Mittel der Methylierungsgrad der MCPs nicht und die MCPs geben kein Signal ab. Steigt die Lockstoffkonzentration, wird CheA deaktiviert, die Methylesterase damit nicht aktiviert und die Methyltransferase überträgt zusätzliche Methylgruppen auf die MCPs, welche die CheA-Aktivität wieder normalisieren. Sinkt die Lockstoffkonzentration, sind die MCPs sozusagen übermethyliert, die MCPs aktivieren somit CheA, die aktive Methylesterase CheB-P wird gebildet und die Methylgruppen an den Glutamatresten werden in Form von Methanol abgespalten.[1]
Pathogenität von Escherichia coli
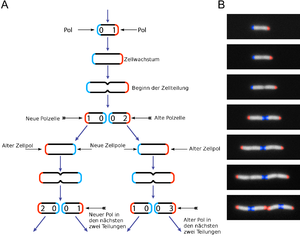
E. coli ist Teil der Darmflora. E. coli teilt sich sehr schnell (unter optimalen Bedingungen alle 20 Minuten), so dass andere Keime, die dem Körper schaden könnten, sich nicht ausbreiten können. Außerhalb des Darms jedoch kann E. coli Infektionen hervorrufen, da es sich „am falschen Fleck“ befindet (fakultativ pathogen), etwa Harnwegsinfekte, eine Bauchfellentzündung (beispielsweise präoperativ nach Perforation eines Sigmadivertikels, seltener allein postoperativ) oder Hirnhautentzündung bei Neugeborenen (Infektion während der Geburt). Zum Anheften an bestimmte Zellen der Harnwege besitzen die Bakterien so genannte P-Fimbrien oder PAP (pyelonephritis assoziierte Pili). Weiterhin kommen Fimbrien und Hämolysine vor. Das Kapselantigen K1 von bestimmten Kapsel tragenden E. coli ist an der Neugeborenenmeningitis beteiligt (siehe unten).
Einige Stämme von E. coli sind für den Menschen darmpathogen (krankheitsauslösend im Sinn einer Darmerkrankung), da sie Mechanismen besitzen, die dem Körper Schaden zufügen können. Hier unterscheidet man einige Subtypen (Pathovare), die unterschiedliche Pathogenitätsfaktoren besitzen:
- EHEC enterohämorrhagische E. coli
- EPEC enteropathogene E. coli
- ETEC enterotoxische E. coli
- EIEC enteroinvasive E. coli
- EAEC enteroaggregative E. coli
- DAEC diffus adhärente E. coli,
wobei die vier Erstgenannten die wichtigsten sind.
Die oben in der Einleitung genannten Erkrankungen werden teilweise auch den folgenden Pathovarnamen zugeordnet:
- UPEC uropathogene E. coli
- SEPEC Sepsis auslösende E. coli
- MENEC Meningitis auslösende E. coli
Ein neuartiger Stamm soll nach Ergebnissen der Cornell University in Ithaca, NY (USA) eng mit der chronisch entzündlichen Darmerkrankung Morbus Crohn verknüpft sein.[2]
Pathogenese
Darminfektionen wurden vornehmlich unter dem Namen EHEC-Colitis (enterohämorrhagische Colitis) bekannt. EHEC-Infektionen zählen zu den häufigsten Lebensmittelvergiftungen. Infektionsquellen sind Rinder, Rohmilch, infizierte Menschen oder Trinkwasser. 20–100 Keime des EHEC sind für eine Infektion ausreichend, und es kann zu einem definitiven Nierenschaden kommen (vgl. Hämolytisch-urämisches Syndrom). Möglich sind weiterhin neurologische Ausfälle, chronische Pankreatitis, Glucose-Unverträglichkeit (Intoleranz), Diabetes mellitus, Dickdarmstriktur. Dieser Keim enthält ein Toxin mit dem Namen Verotoxin, da es toxisch auf Verozellen wirkt, einer Zelllinie aus Affennierenzellen.
Der Stamm ETEC ist ein häufiger Erreger der Reisediarrhoe (Montezumas Rache). Grund für diese Erkrankung ist ein hitzelabiles Enterotoxin vom A/B Typ (LT I und LT II). Dieses 73 kDa große Protein besitzt zwei Domänen, von denen eine an ein G-Gangliosid der Zielzelle bindet (Bindene Domäne). Die andere Domäne ist die Aktive Komponente, die ähnlich dem Choleratoxin die Adenylatcyclase und die Guanylatcyclase aktiviert. Die genetische Information erhält das Bakterium von einem lysogenen Phagen durch Transduktion. Weiterhin enthält der ETEC Stamm noch ein hitzestabiles Toxin (ST), deren Funktion allerdings noch nicht vollständig enthüllt ist.
Bei Säuglingen löst der Stamm EPEC Durchfall aus und führt zu Gedeihstörungen.
Auch EIEC zerstören die Darmschleimhautzelle, indem sie in sie eindringen und das Krankheitsbild einer Bakterienruhr imitieren.
Therapie
Sie sollte immer gezielt nach Antibiogramm erfolgen. Gyrasehemmer, Aminopenicilline und – meist besser wirksam – Cephalosporine sind die Mittel der Wahl. Für Cotrimoxazol wurde bei EHEC eine Steigerung der Toxinbildung beschrieben, so dass hier auf diese Substanz verzichtet werden sollte. Bei der Dauer der Therapie spielen die Schwere der Infektion sowie anatomische Anomalien eine Rolle.
Im Fall der häufigen Reisedurchfälle ist in erster Linie der Wasser- und Elektrolytverlust zu ersetzen, eine antibiotische Therapie ist selten notwendig. Grundsätzlich gilt jedoch, dass die Durchfälle zur Ausscheidung der Erreger entscheidend beitragen und daher bei unkomplizierter Reisediarrhoe (wie oben erwähnt: „Montezumas Rache“) nicht künstlich unterbunden werden sollten. Zum Ausgleich des Wasser- und Salzverlustes sind in Apotheken Pulvermischungen erhältlich, die in (sauberem!) Wasser aufgelöst werden können und i.d.R. völlig ausreichend sind. Diese Mischungen werden auch als orale Rehydratationslösungen (englisch: Oral Rehydratation Solution, ORS) bezeichnet und enthalten vor allem Natriumsalze und Zucker (Glucose), daneben Kaliumsalze und zum Teil Bicarbonat oder Citrat.
Prophylaxe
Seit Ende 2004 gibt es in Deutschland einen zugelassenen Impfstoff (Dukoral). Dieser imitiert die Beta-Untereinheit des hitzelabilen ETEC-LT (siehe oben) und gleichzeitig die ähnliche Beta-Untereinheit des Colera-Toxins. Auf diesem Wege bildet der Körper eine Immunantwort gegen beide Toxine aus (Kreuzreaktivität).
Escherichia coli in der Tiermedizin
Escherichia coli ist für eine Vielzahl von Erkrankungen bei Tieren verantwortlich. Spezifische Krankheitsbilder sind:
- Coliruhr der Saug- und Absatzferkel
- Coliseptikämie der Kälber und Lämmer
- Coliseptikämie des Geflügels
- Colimastitis der Kühe
Escherichia coli ist der Keim, der am häufigsten im Zusammenhang mit krankhaften Prozessen im Rachenraum von Hunden und Katzen in Erscheinung tritt. [3]
Escherichia coli in der Forschung
Aus E. coli gelang Jonathan Beckwith 1969 als erstem die Isolierung eines einzelnen Gens. Das relativ kleine Genom dieses Prokaryoten (ca. 4,65 ·106 Basenpaare, entspricht etwa 5000 Genen) wurde als eines der ersten vollständig sequenziert.
E. coli ist die in der Molekularbiologie am meisten verwendete Bakterienart. Ihr Genom ist entschlüsselt worden und viele ihrer Einzelstämme wurden isoliert. Seit 1988 führte Richard Lenski ein Langzeitexperiment über die Evolution von E. coli durch.
Im Zuge der GeneSat-1 Mission wurden am 16. Dezember 2006 E. coli mittels eines CubeSat in den Orbit befördert, um genetische Änderungen aufgrund von Strahlungen im All und der Schwerelosigkeit zu untersuchen.[4]
Um E. coli in biotechnologischen Anwendungen leichter handhaben zu können, züchtete ein Team um Frederick Blattner (University of Wisconsin) einen Stamm, dessen Genom gegenüber natürlich vorkommenden Varianten um ca. 15 Prozent verkleinert wurde, und der dennoch lebens- und fortpflanzungsfähig ist. Hierfür wurden zwei unterschiedliche E. coli-Stämme verglichen, und diejenigen Gene entfernt, die kein Homolog im jeweils anderen Stamm haben und somit entbehrlich scheinen.[5]
Neuere Forschungen von Professor James Liao[6][7] und seinem Team von der Universität von Kalifornien, Los Angeles (UCLA) zeigen, daß sich genetisch veränderte E.coli nutzen lassen, um Biotreibstoffe in Form von Isobutanol und anderen längerkettigen Alkoholen, wie etwa 1-Butanol, 2-Phenylethanol oder verzweigten Pentanolen aus Glucose herzustellen.[8][9]
Escherichia coli XL1-Red
E. coli XL1-Red ist ein Stamm, der in der Molekularbiologie und Gentechnik zur ungerichteten Mutagenese genutzt wird. Durch Defekte im DNA-Reparaturmechanismus zeigt der Stamm eine 5000-fache Mutationsrate gegenüber dem Wildtyp. Die Defekte im DNA-Reparaturmechanismus gehen auf drei Mutationen der genomischen DNA zurück. Das Gen MutS codiert für ein Protein, welches bei der Error Prone Reparatur eine Rolle spielt. Durch die Mutation erfolgt keine Fehlbasenreparatur nach der DNA-Replikation. MutD löst einen Defekt der 3'-5'-Exonukleaseaktivität der DNA-Polymerase III aus. MutT ist für die Unfähigkeit zur Hydrolyse des Basenanalogons 8-oxoGTP verantwortlich. Da die Mutationen nur auf den defekten DNA-Reparaturmechanismus zurückzuführen sind, werden zur Mutationsauslösung weder Mutagene noch Karzinogene benötigt.
Die Generierung von Gen-Mutationen ist ein klassisches Mittel in der biomedizinischen Forschung, um generelle oder Teil-Funktionen des entsprechenden Gens zu erforschen.
E.coli in der industriellen Anwendung
E.coli ist ein weit verbreiteter Organismus in bio- bzw. gentechnologischen Verfahren, wo er z.B. als Wirt für Klonierungsvektoren, wie z.B. das Plasmid pBR322 eingesetzt wird. Ferner stammt aus dem Genom von E.coli das Restriktionsenzym EcoRI, das in der Gentechnik weite Verwendung findet.
In der Biotechnologie wird mittels genetisch veränderten E.coli in industrieller Biosynthese grosstechnisch Insulin produziert und das derart hergestellte Insulinpräparat in der Behandlung von Diabetes eingesetzt. Hierfür ist E. coli besonders geeignet, da es zur Darmflora des Menschen gehört und so gut wie keine Allergien verursacht. Auch in der industriellen Herstellung von Aminosäuren, Interferon oder dem menschlichen Wachstumshormon werden gentechnisch veränderte E.coli Bakterien verwandt.[10]
Siehe auch
- Symbiont
- Richard Lenski und das E. coli Langzeitprojekt in Experimenteller Evolution.
Literatur
- Weinke: Prävention von Reisediarrhoen, Flug- und Reisemedizin. April 2004, S. 12–13
- Clemens et al.: Field trial of oral cholera vaccines in Bangladesh: results from three-year follow up, Lancet 1990; 335, S. 270–273
- Alfred-Nissle-Gesellschaft e. V. (Hrsg.): Darmflora in Symbiose und Pathogenität, 4. Interdisziplinäres Symposium, Berlin 10.–11. November 2000. Alfred-Nissle-Gesellschaft e. V. Hagen 2001 (kostenlos bei Alfred-Nissle-Gesellschaft e. V., Brüningstr. 16, 58089 Hagen, E-Mail: office@a-nissle-ges.de)
- Gruss et. al. (Hrsg.): Industrielle Mikrobiologie - Ausgewählte Verfahren und Perspektiven für die Zukunft, 3. Auflage, Spektrum Verlag Heidelberg 1987, ISBN 3-922508-25-1
Weblinks
- EcoliWiki englischsprachiges Wiki der Texas A&M University
- Das Enterotoxin von Escherichia coli – Aufbau und Wirkung (von Dr. Bernhard Peter)
- http://www.uni-protokolle.de/nachrichten/id/42080/
Genomik (englisch)
- EcoCyc: Enzyklopädie von E. coli -Genen und Stoffwechsel
- coliBASE: eine vergleichende Genomdatenbank für E. coli
- EchoBASE: eine integrierte post-genomische Datenbank für E. coli
- Der E. coli Index: Ressourcen für E. coli als Modellorganismus* E. coli CFT073 Genomseite
- E. coli K12-MG1655 Genomseite
- E. coli O157:H7 EDL933 Genomseite
- E. coli O157:H7 VT2-Sakai Genomseite
- E. coli UTI89 Genomseite
Einzelnachweise
- ↑ http://www.nature.com/nature/journal/v438/n7067/abs/nature04228.html Nature, Bd. 438, S.504
- ↑ Yahoo! Groups
- ↑ Bakteriologische und mykologische Untersuchungen von Rachenabstrichen bei Hund und Katze
- ↑ http://www.crestnrp.org/genesat1/ GeneSat-1
- ↑ Scaled-down genome may power up E. coli's ability in lab, industry. Biology News Net, 28. April 2006 (englisch)
- ↑ Personnel of the California NanoSystems Institute (englisch)
- ↑ Metabolic Engineering and Systems Biology Laboratory (englisch)
- ↑ UCLA Engineering researchers develop new method for the production of more efficient biofuels UCLA Engineering: News Center, 01.02.08 (englisch)
- ↑ Bakterien produzieren Butanol Heise Online Technology Review, 30.01.08
- ↑ T.A. Brown: Gentechnologie für Einsteiger, 3. Auflage, Spektrum Verlag Heidelberg 2002, ISBN 3-8274-1302-8
Wikimedia Foundation.