- Iodessigsäure
-
Strukturformel 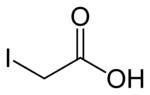
Allgemeines Name Iodessigsäure Andere Namen - Iodethansäure
- Monoiodessigsäure
Summenformel C2H3IO2 CAS-Nummer 64-69-7 PubChem 5240 Kurzbeschreibung weißer, stechend riechender Feststoff[1]
Eigenschaften Molare Masse 185,96 g·mol−1 Aggregatzustand fest
Schmelzpunkt Siedepunkt 208 °C[1]
pKs-Wert 3,18[2]
Löslichkeit gut in Wasser (600 g·l−1 bei 20 °C)[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [3] 

Gefahr
H- und P-Sätze H: 301-314 EUH: keine EUH-Sätze P: 260-301+310-303+361+353-305+351+338-405-501 [4] EU-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [3] 

Giftig Ätzend (T) (C) R- und S-Sätze R: 25-35 S: (1/2)-22-36/37/39-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Iodessigsäure (auch: Monoiodessigsäure) ist ein Derivat der Essigsäure, bei welcher ein Wasserstoffatom der Methylgruppe durch ein Iodatom ersetzt ist. Ihre Salze werden als (Mono-)Iodacetate bezeichnet.
Inhaltsverzeichnis
Gewinnung und Darstellung
Die Darstellung erfolgt durch Umsetzung von Chloressigsäure mit Kaliumiodid[5] (nukleophile Substitution):
Eigenschaften
Iodessigsäure bildet farblose Kristalle mit stechendem Geruch, die zwischen 80 und 82 °C schmelzen und sich sehr leicht in Wasser, Ethanol, Diethylether und anderen organischen Lösungsmitteln lösen. Die wässrige Lösung reagiert stark sauer, deutlich stärker sauer als Essigsäure. Der Grund dafür ist die Stabilisierung des Anions durch das recht elektronegative Iodatom: Es wirkt elektronenziehend und verteilt (delokalisiert) die negative Ladung des Anions über das gesamte Molekül. Das Anion bildet sich daher leichter als das entsprechende Anion der Essigsäure. In wässriger Lösung dissoziiert die Iodessigsäure unter Bildung von Oxonium- und Iodacetat-Ionen.
Iodessigsäure ist, wie viele andere Alkyliodide auch, instabil gegenüber Sonnenlicht und zersetzt sich dabei recht leicht. Iodessigsäure ist daher in braunen Flaschen bei Temperaturen unterhalb von 15 °C zu lagern.
Verwendung
Iodessigsäure ist Ausgangsstoff für verschiedene Synthesen, beispielsweise für Pflanzenschutzmittel oder Arzneimittel. So wird das Mukolytikum (ein Sekretlöser bei Erkältungskrankheiten) Carbocystein („Carbocistein“), aus L-Cystein und Iodessigsäure hergestellt.
Direkte Anwendung findet Iodessigsäure in der Biochemie. Iodessigsäure alkyliert irreversibel die SH-Gruppe von Proteinen, beispielsweise die Glycerinaldehydphosphat-Dehydrogenase. Sie kann dazu verwendet werden, Enzyme mit –SH an der aktiven Stelle irreversibel zu deaktivieren. Diese Eigenschaft der irreversiblen Enzymblockade bedingt auch die Giftigkeit der Iodessigsäure.
Prinzipiell ist Iodessigsäure, wie auch Bromessigsäure, als Konservierungsmittel geeignet. Wegen der hohen Toxizität und Instabilität wird sie allerdings kaum eingesetzt.
Gefahren
Iodessigsäure und ihre Lösungen wirken stark ätzend und sind giftig.
Einzelnachweise
- ↑ a b c d Datenblatt Iodessigsäure bei Merck, abgerufen am 19. Februar 2010.
- ↑ CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ a b Eintrag zu CAS-Nr. 64-69-7 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ Eintrag zu CAS-Nr. 64-69-7 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 5. April 2011 (JavaScript erforderlich).
- ↑ Thieme Chemistry (Hrsg.): RÖMPP Online – Version 3.11. Georg Thieme Verlag KG, Stuttgart 2011

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- Giftiger Stoff
- Ätzender Stoff
- Organoiodverbindung
- Carbonsäure
Wikimedia Foundation.


