- Citratkreislauf
-
Der Citratzyklus (auch Zitratzyklus, Zitronensäurezyklus, Tricarbonsäurezyklus oder Krebs-Zyklus) ist ein zentraler Kreislauf biochemischer Reaktionen im Stoffwechsel (Metabolismus) aerober Zellen von Lebewesen, der hauptsächlich dem oxidativen Abbau organischer Stoffe dient und Zwischenprodukte für Biosynthesen liefert.
Das beim Abbau von Fetten, Zuckern und Aminosäuren als Zwischenprodukt entstehende Acetyl-CoA wird darin unter Freisetzung von Kohlenstoffdioxid (CO2) und Wasser (H2O) zur direkten und indirekten Erzeugung von biochemisch für den Organismus verfügbarer Energie genutzt. Der Citratzyklus läuft bei Eukaryoten in der Matrix der Mitochondrien, bei Prokaryoten im Zytoplasma ab.
Namensgeber ist das dabei entstehende Zwischenprodukt Citrat, das Anion der Citronensäure. Die Reaktionsfolge wird nach ihrem Entdecker Hans A. Krebs (1900–1981) auch als Krebs-Zyklus bezeichnet. Krebs erhielt 1953 den Nobelpreis für Medizin für die Klärung metabolischer Abbauwege.
Inhaltsverzeichnis
Entdeckung
1937 postulierte der Biochemiker Hans Adolf Krebs als erster den Citronensäure-Zyklus als Weg der Pyruvatoxidation. Er untersuchte den Einfluss verschiedener organischer Säuren auf den Sauerstoffverbrauch bei der Pyruvatoxidation mit Suspensionen von zerkleinertem Taubenbrustmuskel. Dieser Flugmuskel ist für die Untersuchung besonders gut geeignet, da er eine hohe oxidative Aktivität aufgrund einer sehr hohen Atmungsgeschwindigkeit aufweist. Krebs bestätigte die Beobachtung von unter anderem Albert Szent-Györgyi, dass C4-Dicarbonsäuren aus tierischen Geweben (Succinat, Malat, Fumarat und Oxalacetat) den Sauerstoffverbrauch von Muskeln stimulieren. Krebs bestätigte diese Beobachtung und fand, dass auch die Pyruvatoxidation einen solchen Effekt hervorruft. Diese wird durch C6-Tricarbonsäuren Citrat, cis-Aconitat und Isocitrat, sowie durch die C5-Verbindung α-Ketoglutarat stimuliert. Andere organische Säuren zeigten nicht den genannten Effekt. Dieser war jedoch äußerst beachtlich, denn sehr geringe Mengen führten bereits zu einer Oxidation einer vielfachen Menge an Pyruvat.
Die zweite wichtige Beobachtung von Krebs war, dass Malonat – eng verwandt mit Succinat und kompetitiver Inhibitor der Succinat-Dehydrogenase – die aerobe Verwertung von Pyruvat in Muskelsuspensionen hemmt und zwar unabhängig davon, welche der aktiven organischen Säuren zugesetzt wird. Dies zeigt, dass Succinat und Succinat-Dehydrogenase wesentliche Bestandteile der an der Pyruvatoxidation beteiligten Reaktion sein müssen.
Aus diesen grundlegenden Beobachtungen und weiteren Hinweisen schloss Krebs, dass die unten aufgeführten aktiven Tri- und Dicarbonsäuren in einer chemisch logischen Reihenfolge angeordnet sein könnten. Da die Inkubation von Pyruvat und Oxalacetat mit zerkleinertem Muskelgewebe eine Anreicherung von Citrat im Medium hervorrief, folgerte Krebs, dass diese Sequenz nicht linear, sondern zyklisch arbeitet – ihr Ende ist mit ihrem Anfang verknüpft. Er irrte sich nur bei der letzten fehlenden Reaktion. Es gilt nämlich nicht: Pyruvat + Oxalacetat → Citrat + CO2. Somit schlug Krebs vor, dass der von ihm als Zitronensäure-Zyklus bezeichnete Weg den Hauptweg der Kohlenhydratoxidation im Muskel darstellt.
Rolle im Stoffwechsel
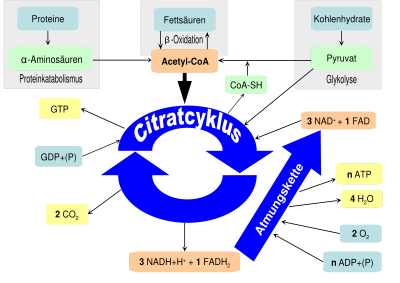
Im oberen Teil der Abbildung 2 sind die drei Klassen von Nährstoffen eingetragen, die im Stoffwechsel abgebaut werden: Proteine, Fette und Kohlenhydrate.
Durch Abbau der Proteine im Proteinkatabolismus entstehen α-Aminosäuren. In der Glykolyse werden Kohlenhydrate zu Pyruvat (Brenztraubensäure) abgebaut. Weitere Reaktionen lassen sowohl aus den Aminosäuren als auch aus dem Pyruvat Acetyl-CoA entstehen. Aus Fettsäuren werden durch β-Oxidation direkt Acetyl-CoA-Moleküle gebildet.
Acetyl-CoA kann daher als zentrales Abbauprodukt aller drei Nährstoffklassen bezeichnet werden. In den Mitochondrien tritt sein Essigsäure-Rest in den Citratzyklus ein und wird dort zwecks Gewinnung von Energie (ATP, GTP) und von Reduktionsäquivalenten (NADH, FADH2) und unter Kohlenstoffdioxid-Abgabe weiter abgebaut. Die im Citratzyklus gewonnenen, an Coenzyme (NAD+ und FAD) gebundenen Elektronen werden der Atmungskette zugeführt und auf den terminalen Elektronenakzeptor Sauerstoff übertragen. Die Energie dieses Redoxpotentials wird schließlich genutzt, um ATP zu generieren.
Ablauf
Der Citratzyklus läuft bei Eukaryoten in den Mitochondrien, bei Prokaryoten im Zytoplasma oder gegebenenfalls in Mitochondrienäquivalenten ab. Er ist ein amphiboler Stoffwechselprozess, d. h. er kann sowohl anabolen als auch katabolen Stoffwechselwegen dienen. Der Citratzyklus ist Teil oxidativer Abbauprozesse und geht bei aeroben Organismen der eigentlichen Atmungskette voraus. Anaerobe Organismen verwenden zunächst die gleichen Abbauwege für energiereiche organische Stoffe, z. B. die Glykolyse, dann aber nicht die Oxidation von Wasserstoff in der Atmungskette, sondern andere, nicht von Sauerstoff abhängige Fermentationsprozesse, um Energie zu gewinnen (siehe auch Gärung).
Bei erhöhter Leistungsabforderung wird auch beim Menschen ein wachsender Prozentsatz des in der Glykolyse gewonnenen Pyruvats nicht mehr zu Acetyl-CoA umgesetzt, sondern unter ATP-Gewinnung zu Lactat verstoffwechselt. Das Zellgift Lactat muss aber ab einem bestimmten Quantum, das leistungshemmend wirkt, abgebaut werden. Dabei gibt die Muskulatur Laktat an das Blut ab, welches zur Leber transportiert wird. Anschließend wird Laktat in der Leber zu Glucose durch den Prozess der Gluconeogenese umgesetzt. Glucose kann wieder durch das Blut von den Muskelzellen aufgenommen werden. Dieser Kreislauf wird auch als der sogenannte Cori-Zyklus bezeichnet. Die Fähigkeit, eine hohe Leistung trotz hohen Lactatspiegels aufrechtzuerhalten, wird in der physiologisch begründeten Trainingslehre als Lactattoleranz bezeichnet.
Der Citratzyklus kann als der dritte von vier Schritten im Kohlenhydrat-Katabolismus betrachtet werden. Er findet nach der Glykolyse und der oxidativen Decarboxylierung von Pyruvat, jedoch vor der Endoxidation in der Atmungskette, statt.
Für den Citratzyklus lässt sich folgende Bilanz aufstellen:
- Acetyl-CoA + 3 Nicotinamidadenindinukleotid (NAD+) + Flavinadenindinukleotid (FAD) + Guanosindiphosphat (GDP) + Phosphat + 2 Wasser (H2O) → 2 Kohlenstoffdioxid (CO2) + 3 (NADH + H+) + FADH2 + Guanosintriphosphat (GTP) + Coenzym A (CoA-SH)
Acetyl-CoA, das ist Essigsäure gebunden an Coenzym A, also Essigsäure in ihrer „aktivierten“ Form, wird durch den Citratzyklus zu Kohlenstoffdioxid (CO2), den Reduktionsäquivalenten NADH und FADH2 sowie den Energieüberträgern Adenosintriphosphat, ATP, sowie Guanosintriphosphat, GTP, verstoffwechselt. In der Atmungskette werden die an den Reduktionsäquivalenten gebundenen Elektronen im letzten Schritt auf einen terminalen Elektronenakzeptor, in den Mitochondrien auf Sauerstoff, übertragen. Die Potentialdifferenz, die bei der Wanderung der Elektronen durch die Atmungskette von Proteinkomplex zu Proteinkomplex und schließlich auf Sauerstoff entsteht, wird nutzbar gemacht. Dabei werden nämlich Protonen vom Inneren des Mitochrondriums (Matrix) in den Intermembranraum transportiert, es bildet sich dabei ein elektrochemischer Protonengradient. Durch die Vermittlung des elektrochemische Protonengradienten über der inneren Mitochrondrienmembran wird schließlich über die ATP-Synthase ATP synthetisiert.
Teilreaktionen
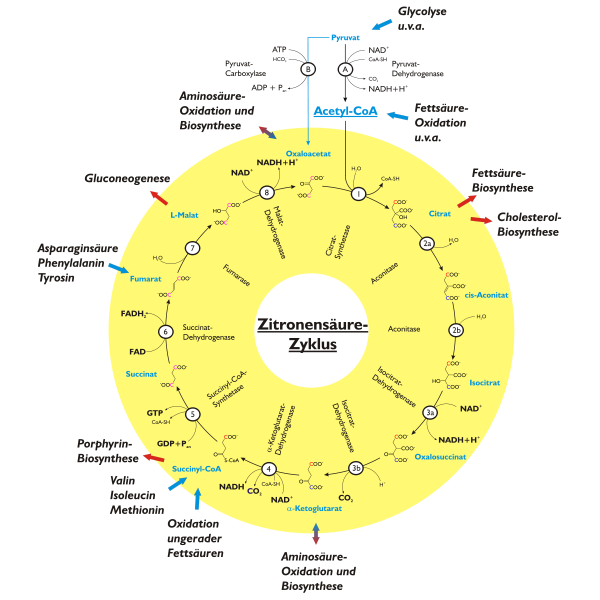 Abb. 1. Der Reaktionsablauf des Citratzyklus; blaue Pfeile symbolisieren anaplerotische, rote Pfeile cataplerotische Stoffwechselwege, die eng mit dem Citratzyklus verbunden sind.
Abb. 1. Der Reaktionsablauf des Citratzyklus; blaue Pfeile symbolisieren anaplerotische, rote Pfeile cataplerotische Stoffwechselwege, die eng mit dem Citratzyklus verbunden sind.Der Reaktionsablauf ist in Abb. 1 skizziert. Ausgangspunkt des Citratzyklus ist eine durch die Citrat-Synthase katalysierte Kondensation 1 von Oxalacetat mit Acetyl-CoA zum Citrat. Citrat wird bei Bedarf aus dem Zyklus abgezogen und der Cholesterolbiosynthese bzw. der Fettsäuresynthese zugeführt. Diese im Cytosol stattfindenden Prozesse benötigen Acetyl-CoA, welches – im Gegensatz zum Citrat – nicht vermag, die Mitochondrienmembran zu passieren, jedoch aus Citrat synthetisiert werden kann.
Die sich daran anschließende Isomerisierung 2a-b des Citrats durch die Aconitase liefert Isocitrat. Die Bedeutung dieses Schrittes liegt in der Umwandlung eines schwer zu oxidierenden tertiären Alkohols (Citrat) in einen leicht zu oxidierenden sekundären Alkohol.
Isocitrat wird durch die Isocitrat-Dehydrogenase in den Schritten 3a-b oxidiert und decarboxyliert. Neben dem ersten Reduktionsäquivalent NADH entsteht hierbei α-Ketoglutarat (anderer Name: 2-Oxoglutarat), ein auch für den Aminosäuren-Metabolismus wichtiges Zwischenprodukt (cataplerotischer Stoffwechselpfad: reduktive (Trans-)Aminierung zum Glutamat ⇒ Aminosäurebiosynthese; anaplerotischer Stoffwechselpfad: Desaminierung des Glutamats ⇒ Aminosäureoxidation).
Experimente mit isotopenmarkierten Substraten zeigen, dass das bei der Decarboxylierung im Schritt 3b freigesetzte CO2 dem Oxalacetat entstammt, im Gegensatz zur folgenden Reaktion 4, die über eine oxidative Decarboxylierung neben NADH ein zweites Molekül CO2 liefert, dessen Kohlenstoff der Carbonylgruppe des Acetyl-CoAs zuordenbar ist. Das nun entstehende Succinyl-CoA ist ein weiteres Schlüsselprodukt des Citratzyklus (cataplerotischer Stoffwechselpfad: Porphyrin-Biosynthese; anaplerotische Stoffwechselpfade: Abbau der Aminosäuren Valin, Isoleucin und Methionin, Oxidation ungeradzahliger Fettsäuren, siehe auch Fettsäureoxidation).
Die vermittels der Succinyl-CoA-Synthetase katalysierte Hydrolyse 5 des energiereichen Thioesters Succinyl-CoA zum Succinat liefert das einzige Energieäquivalent des Citratzyklus in Form von GTP.
Succinat ist im Schritt 6 das Substrat der Succinat-Dehydrogenase, welche durch Oxidation ein drittes Reduktionsäquivalent in Form des FADH2 liefert sowie Fumarat, welches auch durch einen anaplerotischen Stoffwechselpfad über den Abbau der Aminosäuren Asparaginsäure, Phenylalanin und Tyrosin in den Citratzyklus eingespeist wird.
Die Fumarase katalysiert die stereospezifische Addition von Wasser an die Doppelbindung des Fumarats im Schritt 7, so dass L-Malat entsteht, welches auch als Ausgangsstoff zur Gluconeogenese dient.
Wie schon das Isocitrat ist auch das Malat bedingt durch die sekundäre OH-Gruppe oxidabel, so dass im Schritt 8 durch die Malat-Dehydrogenase unter Gewinnung von NADH das Substrat des ersten Schrittes, Oxalacetat, resynthetisiert wird und der Kreislauf somit geschlossen wird. An das Oxalacetat sind wiederum weitere Stoffwechselpfade angebunden (cataplerotisch: reduktive (Trans-)Aminierung zum Aspartat ⇒ Aminosäure-Biosynthese; anaplerotisch: Desaminierung des Aspartats ⇒ Aminosäureoxidation).
Teilschritte des Citrat-Zyklus Substrat Reaktionspartner/
CoenzymeEnzym Reaktionstyp Inhibitoren Aktivatoren Produkte/
Coenzyme1 Oxalacetat Acetyl-CoA, Wasser Citrat-Synthase Kondensation Citrat, NADH, Succinyl-CoA, ATP Citrat 2a Citrat - Aconitase Dehydratisierung cis-Aconitat, Wasser 2b cis-Aconitat Wasser Hydratisierung Isocitrat 3a Isocitrat NAD+ Isocitrat-Dehydrogenase Oxidation NADH, ATP Ca2+, ADP Oxalsuccinat, NADH 3b Oxalsuccinat H+ Decarboxylierung α-Ketoglutarat, CO2 4 α-Ketoglutarat NAD+, CoA-SH α-Ketoglutarat-Dehydrogenase Oxidative Decarboxylierung NADH, Succinyl-CoA Ca2+ Succinyl-CoA, NADH, CO2 5 Succinyl-CoA GDP, Phosphat Succinyl-CoA-Synthetase Phosphat-Transfer Succinat, GTP, CoA-SH 6 Succinat FAD Succinat-Dehydrogenase Oxidation Malonat Mg2+ Fumarat, FADH2 7 Fumarat Wasser Fumarase Hydratisierung L-Malat 8 L-Malat NAD+ Malat-Dehydrogenase Oxidation Oxalacetat, NADH Nicht zum Citratzyklus gehörig: A Pyruvat NAD+, CoA-SH Pyruvat-Dehydrogenase Oxidative Decarboxylierung NADH, Acetyl-CoA Ca2+ Acetyl-CoA B Pyruvat ATP, H+, CO2 Pyruvat-Carboxylase Carboxylierung Acetyl-CoA Oxalacetat, ADP, Phosphat Regulation
Der Citratzyklus als zentraler Drehpunkt des aeroben Metabolismus unterliegt starken regulatorischen Einflüssen. Neben der Produktinhibition („negative Rückkopplung“, kompetitive Hemmung) und Inhibition durch andere Zwischenverbindungen spielen als Effektoren insbesondere NAD+/NADH, ADP/ATP und Ca2+ eine große Rolle. Regulatorischer Kontrolle unterliegen dabei insbesondere die Teilschritte großer Exergonie: die Citrat-Synthese 1 (ΔGo = −38 kJ/mol), die Ketoglutarat-Bildung 3 (ΔGo = −7 kJ/mol) und die Bildung des Succinyl-CoA 4 (ΔGo = −37 kJ/mol).
Die oben genannten exergonen Teilschritte werden durch hohe NADH-Pegel inhibiert: gerät z. B. infolge Sauerstoffmangels die Atmungskette ins Stocken, wird also weniger NADH verbraucht und steigt damit dessen Konzentration, so kann auch der Citratzyklus zum Erliegen kommen.
Wird andererseits wenig Energie benötigt (z. B. Muskel im Ruhezustand), so steigt die ATP-Konzentration bei sinkender ADP-Konzentration. Während ADP ein allosterischer Aktivator der Isocitrat-Dehydrogenase ist, inhibiert ATP deren Wirkung: Der Zyklus wird gebremst.
Weitere Effektoren des Citratzyklus sind der Tabelle zu entnehmen.
Trivia
Harold Baum hat ein Lehrbuch[1] herausgebracht, in dem biochemische Prozesse durch bekannte Lieder vertont wurden. Dies soll es Studenten erleichtern, sich besser an komplizierte Sachverhalte bei Stoffwechselwegen zu erinnern. Auch die Prozesse im Citratzyklus wurden im Lied „Waltz Round The Cycle“ vertont.
Quellen
- ↑ Harold Baum: Biochemists' Song Book. Taylor & Francis Ltd, 2. Auflage 1998; ISBN 0-7484-0416-3
Weblinks
- Was ist das Ziel des Zitratzyklus ?
- Prof. DP. Silva: The chemical logic behind the citric acid cycle (engl.)
Siehe auch
Wikimedia Foundation.