- Extrinsic Factor
-
Strukturformel 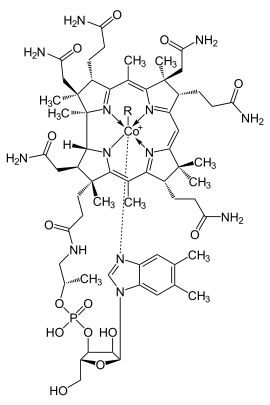
Coenzym B12 (=AdoCbl): R = 5'-Desoxyadenosyl
Cyanocobalamin (=Vitamin B12): R = –C≡N
Hydroxycobalamin (=Vitamin B12a): R = -OH
Methylcobalamin (=MeCbl oder MeB12): R = –CH3Allgemeines Trivialname 5'-Desoxyadenosylcobalamin Andere Namen - Coenzym B12
- Adenosylcobalamin
- AdoCbl
- Cobamamid (INN)
Summenformel C72H100CoN18O17P CAS-Nummer 13870-90-1 ATC-Code B03BA04
Kurzbeschreibung roter, kristalliner Feststoff (Cyanocobalamin) Vorkommen tierische Produkte, Lupinen, Brottrunk Physiologie Funktion Zellteilung, Blutbildung, Funktion des Nervensystems Täglicher Bedarf 0,003 mg[1] Folgen bei Mangel Perniziöse Anämie, neurologische Erkrankungen (z. B. funikuläre Myelose), Glossitis, Diarrhöen Überdosis nicht bekannt Eigenschaften Molare Masse 1579,58 g·mol−1 Aggregatzustand fest Schmelzpunkt zersetzt sich ab 392 °C (Cyanocobalamin) Löslichkeit wenig löslich in Wasser: 12 g·l−1, unlöslich in Ether, Aceton und Chloroform (Cyanocobalamin) Sicherheitshinweise Gefahrstoffkennzeichnung [2] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: 22-24/25 LD50 5000 mg/kg (Meerschweinchen, peroral) [3] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Cobalamine bilden eine (das Spurenelement Cobalt enthaltende) biochemische Stoffgruppe, deren wichtigster Vertreter das Coenzym B12 ist. Coenzym B12 ist ein wasserlösliches Vitamin der B-Gruppe und die unmittelbar aktive Form des Vitamins B12. Aus historischen Gründen steht die Bezeichnung Vitamin B12 jedoch für ein anderes, nicht unmittelbar aktives vitaminisches Cobalamin, das Cyanocobalamin. Coenzym B12 trägt weitere Namen wie Antiperniziosa-Faktor, Extrinsic-Faktor, AdoCbl oder nach chemischer Nomenklatur 5'-Desoxyadenosylcobalamin. Es handelt sich bei all diesen Bezeichnungen immer um dieselbe chemische Verbindung, das Coenzym B12. Vor allem in der Ernährungsliteratur wird der Begriff "Vitamin B12" auch für Coenzym B12, andere Cobalamine oder die ganze Cobalamin-Stoffgruppe gebraucht, was im Widerspruch zu der bioanorganischen Sichtweise steht, die den Begriff nur für die biologisch nicht aktive Substanz Cyanocobalamin verwendet.[4][5][6].
Cyanocobalamin ist ein weiteres bekanntes Cobalamin, das in der Medizin anstelle von Vitamin B12 verwendet wird, da es stabiler ist und sich im menschlichen Körper in dieses Vitamin umwandelt. Die physikalischen Eigenschaften von Cyanocobalamin werden in diesem Artikel beispielhaft für Vitamin B12 behandelt.
Inhaltsverzeichnis
Geschichte
Vitamin B12 wurde in den 1920er-Jahren entdeckt, als man erkannte, dass Hunde (und später auch Menschen) mit perniziöser Anämie mit Extrakten aus tierischer Leber erfolgreich behandelt werden konnten. Auf der Suche nach der essenziellen Komponente im Leberextrakt stießen die Forscher nach jahrelangen Verbesserungen der analytischen Methoden auf die nicht unmittelbar aktive Form des Vitamins, Cyanocobalamin. Vitamin B12 wurde 1926 zum ersten Mal beschrieben, doch erst 1948 rein dargestellt. Die erste Reindarstellung erfolgte unabhängig voneinander durch Folkers bzw. Smith und Mitarbeiter. Da die Substanz nur von Mikroorganismen synthetisiert werden kann und das Spurenelement Kobalt dem Körper zwingend von außen zugeführt werden muss, wurde das Molekül Vitamin B12 getauft. Die aktive Form des Vitamins, Coenzym B12, ist noch wesentlich schwieriger zu isolieren und zu charakterisieren. Sie wurde deshalb erst später entdeckt. Die Strukturaufklärung erfolgte mittels Röntgenbeugung an Einkristallen, eine damals erst in den Anfängen befindliche Methode. Die Biochemikerin Dorothy Crowfoot Hodgkin wurde u. a. für die Strukturaufklärung von Vitamin B12 1964 mit dem Nobelpreis gewürdigt. Die Totalsynthese gelang Albert Eschenmoser und Robert B. Woodward. Noch heute gilt Vitamin B12 als eines der größten Moleküle, das je totalsynthetisiert wurde [7][8].
Beschreibung
Cobalamine sind organometallische Verbindungen mit einem ein-, zwei- oder dreifach positiv geladenen Cobalt-Ion. Es sind die einzigen bekannten natürlich vorkommenden cobalthaltigen Naturstoffe.
Alle Cobalamine haben dieselbe Grundstruktur, einen Cobaltkomplex, in dem das Cobaltkation von fünf Stickstoffatomen und einem sechsten, austauschbaren Liganden umgeben ist. Vier der Stickstoffatome liegen in einer Ebene und gehören zu einem Corrin-Ringsystem. Das Cobalt ist darin sehr fest gebunden und kann praktisch nur durch Zerstörung des Ringsystems herausgelöst werden.
Der austauschbare Ligand wird in der chemischen Strukturformel mit R (für „Rest“) abgekürzt und ist namensgebend für das Cobalamin: Ist R beispielsweise eine Hydroxygruppe, so handelt es sich bei der Verbindung um Hydroxycobalamin. Ist R eine Cyanogruppe, so handelt es sich um Cyanocobalamin, und bei einem 5'-Desoxyadenosylliganden spricht man von 5'-Desoxyadenosylcobalamin, kurz Coenzym B12. Meist ist der sechste Ligand R nur schwach an das Cobaltkation gebunden und kann deshalb leicht ausgetauscht werden. So kann der menschliche Körper bestimmte Cobalamine, zum Beispiel Cyanocobalamin, in Coenzym B12 umwandeln, indem die Cyanogruppe durch eine 5'-Desoxyadenosylgruppe ersetzt wird.
Cyanocobalamin ist eine geruchlose, tief dunkelrote, kristalline, hygroskopische Substanz. Sie löst sich mäßig in Wasser und niederen Alkoholen, gar nicht in organischen Lösungsmitteln wie Aceton, Chloroform oder Ether.
Vitamin B12 ist zwar relativ hitzestabil, jedoch lichtempfindlich. In den Zellen kommt Cobalamin in den Mitochondrien typischerweise als 5'-Desoxyadenosylcobalamin (Coenzym B12) vor, im Cytosol hingegen überwiegt Methylcobalamin. Therapeutisch wird jedoch zumeist Cyanocobalamin oder Hydroxycobalamin eingesetzt, die dann entsprechend umgebaut werden. Die Abbildung zeigt die allgemeine Strukturformel der Cobalamine mit R als austauschbaren Liganden.
Aufgabe/Funktion
Coenzym B12 nimmt im Menschen als Coenzym an nur zwei enzymatischen Reaktionen teil:
- N5-Methyl-Tetrahydrofolat-Homocystein-S-Methyltransferase = Methionin Synthase (EC 2.1.1.13) und
- Methylmalonyl-CoA-Mutase (EC 5.4.99.2).
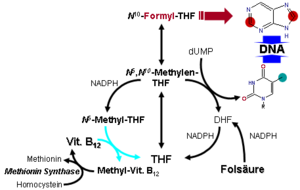
Die Reaktion der Methionin-Synthase[9] dient u. a. der Regeneration des Methylgruppenüberträgers S-Adenosylmethionin (SAM) bzw. der Bildung von Methionin. Dabei wird Homocystein zum Methionin remethyliert. Gelingt dies nicht, bildet sich vermehrt Homocystein, ein Zwischenprodukt beim Abbau der Aminosäure Methionin (erhöhte Homocysteinspiegel werden mit der Bildung von Arteriosklerose in Zusammenhang gebracht). Als Methylgruppendonator fungiert dabei N5-Methyl-Tetrahydrofolat (N5-Methyl-THF). Fehlt Coenzym B12, so reichert sich N5-Methyl-THF an und es kommt zu einem sekundären Mangel an THF, welches für die Synthese der Purinbasen Adenin und Guanin und der Pyrimidinbase Thymidin erforderlich ist. Durch einen Mangel an diesen Nukleobasen ist die Synthese insbesondere von DNA aber auch RNA gestört. Dies äußert sich vorrangig in Organen mit hoher Zellteilungsaktivität wie dem Knochenmark. Es kommt zu einer mehr oder minder ausgeprägten Panzytopenie im Blut, wobei der Mangel an Erythrozyten – die Anämie – am offensichtlichsten ist. Die verbleibenden Erythrozyten werden mit Hämoglobin „vollgestopft“, so dass sie einen höheren Hämoglobingehalt als normale Erythrozyten haben. Auch sind diese Zellen etwas größer. Daher spricht man von einer hyperchromen, makrozytären Anämie. Durch die Gabe von Folsäure kann dieser Block umgangen werden, jedoch löst dieser Ansatz nicht den zugrundeliegenden Vitamin B12-Mangel, so dass die Behandlung der perniziösen (wörtl. „gefährlich“) oder megaloblastären Anämie bei Vitamin B12-Mangel mit Folsäure einen Kunstfehler darstellt.
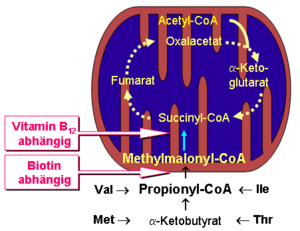
Der Grund hierfür ist die zusätzliche Funktion des Vitamin B12 in der Methylmalonyl-CoA-Mutase. Diese dient der Einschleusung des terminalen Propionyl-CoAs ungeradzahliger Fettsäuren, sowie Teilen des Kohlenstoffgerüstes der Aminosäuren Valin, Isoleucin, Threonin und Methionin in den mitochondrialen Citratzyklus. Das im Rahmen des Abbaus dieser Verbindungen aus Propionyl-CoA (in einem Biotin-abhängigen Schritt) gebildete Methylmalonyl-CoA wird durch die Vitamin-B12-abhängige Methylmalonyl-CoA-Mutase zu Succinyl-CoA, einem Zwischenprodukt des Citratcyclus, umgesetzt.
Ist dieser Schritt gehemmt, kommt es zu einem Anstieg von Methylmalonsäure im Plasma und vor allem im Urin. Dieser Stoffwechselweg spielt offenbar eine besondere Rolle im ZNS, da sich ein Vitamin-B12-Mangel bisweilen sogar vor der typischen Anämie mit Symptomen wie z. B. der funikulären Myelose, einer Störung der Pyramidenbahn und der Hinterstränge, aber auch scheinbaren „Altersdemenzen“ und anderem bemerkbar macht. Daher sollte insbesondere bei älteren Patienten mit neurologischer Symptomatik ein Vitamin-B12-Mangel als mögliche (Mit-)Ursache ausgeschlossen und ggf. behandelt werden. Erste neurologische Symptome äußern sich als so genannte Polyneuropathie in Form von Kribbelparästhesien oder anderen Missempfindungen (z. B. leichtes Brennen) in verschiedenen Körperregionen, die anfangs nur vorübergehend sind.
Vereinfachend zusammengefasst ist Vitamin B12 also wichtig für die Zellteilung und Blutbildung, sowie die Funktion des Nervensystems.
Vorkommen
Vitamin B12 wird ausschließlich von Mikroorganismen hergestellt,[10] die entweder im Verdauungstrakt, oder auf der Oberfläche von (ungewaschener) Nahrung vorkommen. Tiere und Pflanzen sind dazu nicht in der Lage. Lebewesen, die Vitamin B12 benötigen, decken ihren Bedarf durch Fressen „unsauberer“ Nahrung, auf der solche Mikroorganismen vorkommen, oder durch Pflanzen, die durch Düngung mit Ausscheidungen das Vitamin aufgenommen haben. Man nimmt aber an, dass gerade Pflanzenfresser den Hauptteil ihres Bedarfes über eine Symbiose mit diesen Mikroorganismen in ihrem Darm decken. Auch beim Menschen kommen diese Mikroorganismen im Darm vor und produzieren dort Vitamin B12.
Allerdings kann der Mensch damit seinen B12-Bedarf nur unzureichend decken. Dies liegt daran, dass beim Menschen B12 vor allem im Dickdarm produziert wird, die Absorption jedoch nur im Ileum (kurz davor) erfolgen kann. Dadurch wird das im Dickdarm gebildete B12 ausgeschieden.[11]
Außerdem entsteht Vitamin B12 auch durch Milchsäuregärung in Gemüse. Bekannte milchsaure Gemüseprodukte sind Sauerkraut, saure Bohnen (auch Salzbohnen genannt), Salzgurken oder Oliven. Ein weiterer pflanzlicher Vitamin B12 - Lieferant sind Algen (z.B. Spirulina, Chlorella und AFA). Durch diese Lebensmittel ist es auch Vegetariern und Veganern möglich sich ausreichend mit Vitamin B12 zu versorgen ohne tierische Produkte zu konsumieren.[12][13][14]
Sanddorn kann unter Umständen auch Vitamin B12 enthalten. Dieses entsteht durch eine Symbiose mit Bakterien auf der Außenschale der Beere. Damit dieses Vitamin auch in einem Sanddornprodukt vorhanden ist, muss es Fruchtfleisch des Sanddorns enthalten. Unabhängige Erkenntnisse hierzu existieren jedoch bislang nicht. Weiterhin sind die Umstände, die zu dem propagierten hohen Cobalamingehalt des Sanddorn führen sollen, nicht offengelegt.
Vitamin B12 wird sehr gut in der Leber gespeichert und ist in Nahrung tierischer Herkunft (auch Milchprodukten) fast überall enthalten. Bei einer streng veganen Ernährung sollte durch Blutuntersuchungen die Versorgung mit B12 überprüft werden und dieser Stoff gegebenenfalls durch Nahrungsergänzungsmittel zugeführt werden.
Bedarf
Der tägliche Mindestbedarf ist im Vergleich zu den meisten anderen Vitaminen sehr viel geringer, er beträgt nur ca. 3 Mikrogramm[15] . Ein Mangel an Vitamin B12 entwickelt sich sehr langsam, bei völligem Stopp der Zufuhr in der Regel erst nach zwei bis drei Jahren, da die biologische Halbwertszeit des Vitamins B12 450–750 Tage beträgt.
Das Vitamin wird ständig mit Gallensäuren in den Darm abgegeben und an dessen Ende (dem Ileum) mithilfe des Intrinsic-Faktors wieder aufgenommen. Der Bedarf ergibt sich also aus den Mengen, die im Illeum nicht wieder rückresorbiert werden konnten, abzüglich der Mengen, die möglicherweise schon dort durch Mikroorganismen produziert werden.
Falls es zur Störung bei der Bildung des Intrinsic-Faktors kommt kann das Vitamin gar nicht mehr aufgenommen oder rückresorbiert werden, wodurch die Speicher im Körper sehr schnell zurück gehen. Die meisten Fälle von Mangel an Vitamin B12 werden durch Störungen bei der Bildung des Intrinsic-Faktors verursacht.
Mangelerscheinungen
Bei einem Mangel an Vitamin B12 kann es zur perniziösen Anämie (Perniziosa), einer Erkrankung des Blutbildes, und zur funikulären Myelose kommen. Die Ursachen für diesen Mangel können zum einen in unzureichender Zufuhr durch Nahrung oder durch unzureichende Resorption verursacht werden. Bei mangelhafter Aufnahmefähigkeit im Magen-Darm-Trakt fehlt dem Organismus im Magensaft der intrinsic factor, ein Glykoprotein, das von den Belegzellen des Magens produziert wird und für die Vitamin B12-Aufnahme unabdingbar ist. Der intrinsic factor bindet Cobalamin in einem vor Verdauungsenzymen geschützten Komplex und ermöglicht so den Transport in die Darmzellen, von wo aus Vitamin B12 über Bindung an weitere Proteine (Transcobalamine) in die äußeren Gewebe gelangt. Auch eine Störung bei der Aufnahme im terminalen Ileum kann zu einem Mangel führen.
Die ersten Anzeichen von Vitamin B12-Unterversorgung bei erwachsenen Personen können Kribbeln und Kältegefühl in Händen und Füßen, Erschöpfung und Schwächegefühl, Konzentrationsstörungen und sogar Psychosen sein.
Typische Folgen eines Vitamin B12-Mangels sind:
- Methylmalonat-Acidurie (fehlende Methylmalonyl-CoA-Mutase-Aktivität)
- Homocystinurie (fehlende Methionin-Synthase-Aktivität, ggf. sekundär Methionin-Mangel)
- Megaloblastäre Anämie (Störung des Folsäurestoffwechsels durch Block der N5-Methyl-THF-Spaltung zu THF)
- Hypersegmentierte Leukozyten (Zeichen der Überalterung aufgrund der Syntheseprobleme)
- sensorische Neuropathie (wohl Folge der fehlenden Methylmalonyl-CoA-Mutase-Aktivität und der Anämie)
Vitamin B12, gebunden an das aus den Belegzellen des Magens stammende Glykoprotein intrinsic factor, wird physiologisch im terminalen Ileum absorbiert. Nach einer Magenresektion oder bei einer Autoimmungastritis (A-Gastritis), bei der sich die Immunreaktion gegen die den Intrinsic factor bildenden Belegzellen (=Parietalzellen) richtet, ist daher die Aufnahme des Vit. B12 – zumindest bei normalem Angebot – kaum möglich, so dass sich in der Folge ein Vitamin-B12-Mangel ausbilden kann. Auch bei einer schweren Entzündung des Ileums, insbesondere dem Morbus Crohn (= Ileitis terminalis), aber auch anderen intestinalen Erkrankungen mit Malabsorptionssyndrom, oder nach Resektionen des terminalen Ileum bzw. des Magens, kommt es typischerweise zu einem Vitamin-B12-Mangel.
In diesen Fällen ist eine Substitution von Vitamin B12 erforderlich, wobei diese jedoch nicht oral erfolgen darf, sondern durch intramuskuläre Injektion erfolgen sollte, da entweder der fehlende intrinsic factor oder das fehlende bzw. stark gestörte Ileum die Aufnahme des oral zugeführten Vitamin B12 weitgehend verhindern würde. Nur bei Gabe sehr hoher Dosen wird Vitamin B12 auch unspezifisch aufgenommen. Dabei ist jedoch die Resorptionsquote nicht vorhersehbar und daher ist eine orale Vitamin B12-Substitution in diesen Fällen im allgemeinen ungenügend.
Überdosierung
Therapeutische - meist intravenöse - Überdosen werden mit lokalen allergischen Beschwerden[16] sowie einer Form der Akne (Acne medicamentosa) in Verbindung gebracht.[17]
Weitere Verwendung
Hydroxycobalamin ist ein Antidot bei Vergiftungen durch Cyanide- bzw. Blausäure. Cyanidvergiftungen kommen hauptsächlich im Rahmen von Rauchgasvergiftungen bei Bränden in geschlossenen Räumen vor. Weitere Ursachen können die versehentliche oder absichtliche Einnahme, das Einatmen oder ein Hautkontakt bei Industrieunfällen sein.
Unter dem Handelsnamen Cyanokit® erhielt die Firma Merck KGaA am 29. November 2007 für Hydroxocobalamin über das zentralisierte Verfahren von der Europäischen Kommission die Marktzulassung zur Behandlung erwiesener oder vermuteter Cyanidvergiftung bei Erwachsenen und Kindern.[18] Der Wirkstoff Hydroxocobalamin ist eine Vorstufe von Vitamin B12, das Cyanid-Ionen bindet. Dabei entsteht Cyanocobalamin, eine natürliche Form von Vitamin B12, das über die Nieren ausgeschieden wird. Dadurch wird die Bindung des Cyanids an die Cytochrom c Oxidase verhindert. Die Anfangsdosis für Cyanokit bei Erwachsenen liegt bei 5 g, die als intravenöse Infusion zu verabreichen ist. In Abhängigkeit von der Schwere der Vergiftung und der klinischen Reaktion kann eine zweite Dosis von 5 g bis zu einer Gesamtdosis von 10 g verabreicht werden.
Siehe auch
- Corrinoide
- Vitamine
- Hypovitaminose, Hypervitaminose
- Vegane Ernährung
- Portal:Essen & Trinken
Quellen
- ↑ http://www.dge.de/modules.php?name=Content&pa=showpage&pid=3&page=7
- ↑ Herstellerangaben der Firma Sigma-Aldrich: http://www.sigmaaldrich.com/catalog/search/ProductDetail/FLUKA/27591. 14. Okt. 2007
- ↑ Cobalamine bei ChemIDplus
- ↑ Kaim, W., Schwederski, B., 2005: Bioanorganische Chemie - Zur Funktion chemischer Elenemte in Lebensprozessen, 4. Auflage, Teubner Verlag
- ↑ Langley, G., 2005: Vegane Ernährung, Echo Verlag
- ↑ Folkers, K. 1984, Perspectives from research on vitamins and hormones, J. Chem. Educ., 61, 747
- ↑ Manuskript ihres Festvortrages anlässlich der Verleihung des Nobelpreises
- ↑ Kaim, W., Schwederski, B., 2005: Bioanorganische Chemie - Zur Funktion chemischer Elenemte in Lebensprozessen, 4. Auflage, Teubner Verlag
- ↑ Methionine Synthase (Schaubild)
- ↑ Habermehl, Hammann, Krebs: Naturstoffchemie. Eine Einführung. 2. Auflage, Springer, Berlin 2002, ISBN 978-3540439523
- ↑ BfR: Verwendung von Vitaminen in Lebensmitteln, S. 212.
- ↑ "Vegetarische Ernährung", Claus Leitzmann & Andreas Hahn, UTB, Stuttgart
- ↑ "Obst und Gemüse als Medizin", Klaus Oberbeil & Christiane Lentz, 2008, ISBN 3517083836
- ↑ "Lebensmittel-Biotechnologie und Ernährung", Heinz Ruttloff & Jürgen Proll & Andreas Leuchtenberger, Springer-Verlag 1996, ISBN 3540611355, Seite 150-152
- ↑ http://www.dge.de/modules.php?name=Content&pa=showpage&pid=3&page=7
- ↑ F. v. d. Berg, L. Gifford, J. Cabri, L. Arendt-Nielsen, E. Bader: Angewandte Physiologie: Organsysteme verstehen und beeinflussen. 2. Auflage, S. 236, Georg Thieme Verlag, 2005, ISBN 9783131170828
- ↑ O. Braun-Falco, H. Lincke (1976). In: Münchener medizinische Wochenschrift. Bd 118, S. 155-160. PMID 130553
- ↑ http://www.prnewswire.co.uk/cgi/news/release?id=213947
Weblinks
- Cyanocobalamin (Vitamin B12) im Biochemikalien-Lexikon
- Die Aufnahme von Vitamin B12 (Übersichtsgrafik)
- Vitamin B12 in der veganen Ernährung
- Herrmann, Wolfgang; Obeid, Rima: „Ursachen und frühzeitige Diagnostik von Vitamin-B12-Mangel.“ Dtsch Arztebl 2008; 105(40): S. 680-5 Artikel (Übersichtsarbeit)
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.