- Lupus erythematodes
-
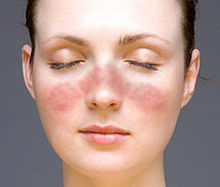
Klassifikation nach ICD-10 M32.- Systemischer Lupus erythematodes M32.0 Arzneimittelinduzierter systemischer Lupus erythematodes M32.1+ Systemischer Lupus erythematodes mit Beteiligung von Organen oder Organsystemen L93.- Lupus erythematodes L93.0 Diskoider Lupus erythematodes L93.1 Subakuter Lupus erythematodes cutaneus ICD-10 online (WHO-Version 2011) Der Lupus erythematodes (lat. lupus „Wolf“, griech. ἐρύθημα [erýtʰēma|tos] „Röte“ + -ώδης [-ṓdēs] „ähnlich wie“) ist eine systemische Autoimmunerkrankung aus der Gruppe der Kollagenosen. „Erythematodes“ (engl. erythematosus) – „errötend“ leitet sich von den bei dieser Krankheit häufig (bei 71 % der Patienten) vorkommenden Rötungen her. Besonders charakteristisch für SLE (systemischer Lupus erythematodes) ist das so genannte Schmetterlingserythem.
Herkunft des Namens
Der Name „Lupus“ – „Wolf“ leitet sich von der Möglichkeit von Verstümmelungen im Gesicht durch CDLE-Läsionen her[1], Ärzte früherer Generationen verglichen diese Läsionen mit Wolfsbissen. Heutzutage kommt es dazu dank moderner Behandlungsmöglichkeiten nur noch selten.
Epidemiologie
Neun von zehn Betroffenen sind aufgrund des geschlechtsspezifischen Signalwegs der Interferon-alpha-Induktion weiblich[2], die Erkrankung ist also gynäkotrop. In Europa tritt der systemische Lupus erythematodes mit einer Inzidenz von 25 bis 27 jährlich Neuerkrankten pro 100.000 Personen auf. Schätzungen zufolge leiden in Deutschland etwa 40.000 Menschen, vor allem junge Frauen im gebärfähigen Alter, an Lupus erythematodes. Afro- und asiatischstämmige Menschen sind auffällig häufiger betroffen als kaukasischstämmige (Europide, Weiße) Menschen.[3] Beim SLE liegt die 5-Jahresüberlebensrate bei 50 % bis 95 %, wobei die schlechteren Werte vor allem bei sozialen Randgruppen zu finden sind[4]. Die durchschnittliche 10-Jahresüberlebensrate liegt bei 85 %.
Formen und Symptome
Systemischer Lupus erythematodes (SLE)
Der systemische Lupus erythematodes (SLE, andere Bezeichnung: Lupus erythematosus disseminatus, abgekürzt LED) beginnt oft mit Fieber, Abgeschlagenheit und Empfindlichkeit gegenüber Sonnenlicht folgen häufig. Außerdem klagen die Betroffenen meist über rheuma-ähnliche Gelenkschmerzen. Auf der Haut bilden sich oft Erytheme.
Überblick über mögliche Symptome bei systemischem Lupus erythematodes[5][6] Häufigkeit in % Symptom 100 Hämatologische Symptome 85 Gelenkschmerzen 84 Allgemeinbeschwerden
(Müdigkeit, Leistungsschwäche …)81 Hautveränderungen 77 Nierenbefunde 63 Gelenkentzündung 58 Raynaud-Syndrom 54 Beschwerden d.
Zentralnervensystem54 Schleimhautveränderungen 47 Magen-Darm Beschwerden 37 Rippenfellentzündung 32 Lymphknotenerkrankung 29 Herzbeutelentzündung 17 Lungenbeteiligung 5 Muskelentzündung 4 Herzmuskelentzündung 4 Bauchspeicheldrüsenentzündung Es kann auch jedes andere Körperorgan befallen werden (systemisch = alle „Systeme“ betreffend). Es können Entzündungen der Gelenke, von Herz, Lungen, Nieren und Gehirn entstehen. Die Gefahr dabei liegt insbesondere im Multi-Organsystemversagen.
Der SLE kann akut-entzündlich mit schweren Schüben, foudroyant, verlaufen. Diese Verlaufsform führte früher häufig und schnell durch Befall von Muskeln, Gelenken, Hirn, Haut und Nieren zum Tod. Sie ist heute dank moderner Behandlungsmethoden sehr selten geworden. Meist verläuft der SLE heute milder und mit weniger Krankheitszeichen. Es gibt langsam-schleichende und schubweise Verlaufsformen.
Es gibt auch sehr milde Verlaufsformen, bei denen nur ein oder zwei ACR-Kriterien erfüllt sind.[1] Diese Verlaufsformen können nach jahrelangem Verlauf in einen SLE übergehen.
SLE mit sekundärem Sjögren-Syndrom
Bei einem Teil der Betroffenen liegt eine Überlappung mit dem Sjögren-Syndrom vor, das insgesamt die häufigste Kollagenose ist. Typisch sind Autoantikörper gegen Anti-SS-A (Ro) und teilweise auch gegen Anti-SS-B (La). Bei diesen Betroffenen ist eine ausgeprägte Photosensibilität vorhanden. Beim so genannten ANA-negativen Lupus erythematodes sind nur niedrige oder gar keine antinukleären Antikörper (ANA) nachweisbar, jedoch mitunter hochtitrige SS-A (Ro)- und evtl. auch Anti-SS-B (La)-Antikörper. Deswegen ist es wichtig, bei einem Screening auf Kollagenosen auch die ANA-Subtypen mitzubestimmen. Schwangere Frauen mit Antikörpern gegen Anti-SS-A (Ro) und Anti-SS-B (La) haben eine erhöhte Wahrscheinlichkeit für einen kongenitalen Herzblock beim ungeborenen Kind und einen neonatalen Lupus erythematodes.
SLE mit sekundärem Antiphospholipid-Syndrom (APS)
Bei manchen Formen (etwa 40 % der Betroffenen) des Lupus erythematodes kommt es zum Antiphospholipid-Syndrom. Dabei bilden sich Antikörper gegen Phospholipid-Protein-Komplexe (anti-Cardiolipin und anti-β-2-Glykoprotein I Antikörper als Hauptvertreter), was man sich bei der Diagnostik zunutze macht, da diese in immunologischen Tests nachgewiesen werden können. Außerdem können diese Komplexe zu Thrombembolien führen, welche sich zudem negativ auf die Prognose auswirken. Weibliche Patienten mit APS haben ein erhöhtes Risiko für wiederkehrende Fehlgeburten (ein Merkmal bei APS-Patientinnen).
Medikamenteninduzierter SLE
Die mildere Verlaufsform des LE, ausgelöst durch Antihypertensiva (wie Dihydralazin), Antiarrhythmika: Procainamid), Antikonvulsiva und Antibiotika, aber auch andere Medikamente, bessert sich meist nach Absetzen des Medikaments. Laborparameter dafür sind ANA und Histon-AK.
SLE im Spätstadium
Da das späte Krankheitsstadium heute medikamentös fast immer vermieden werden kann, tritt das Vollbild des SLE nur noch sehr selten auf. Die typischen Organschäden durch den akuten SLE kommen daher in der Regel nur noch abgemildert vor. Heutzutage wird durch Medikamente versucht, diese Schäden zu vermeiden oder zu verringern; viele Patienten erreichen daher das späte, früher oft letal ausgehende Krankheitsstadium nicht. Neben einer regelmäßigen Kontrolle durch einen versierten Rheumatologen ist auch die medikamentöse Behandlung unbedingt wichtig. Die möglichen, durch SLE ausgelösten, schweren Organschäden Niereninsuffizienz, nephrotisches Syndrom, Arteriosklerose, Herzklappenschäden, Thromboembolien, Knochennekrosen, neurologische und psychiatrische Erkrankungen, Lungenfibrose[1] sind dadurch in der heutigen Zeit seltener geworden.
Chronisch-diskoider Lupus erythematodes (CDLE)
Beim Hautlupus (CDLE) ist nur die Haut betroffen. Der Verlauf ist milde. Nur bei etwa 5 % entwickelt sich ein SLE. Der Hautlupus manifestiert sich meist in Scheibenform („diskoider“ Lupus erythematodes). Diese Hautveränderungen zeigen einen dreiphasigen Aufbau:
- Am Rand besteht eine Rötung, die in einen
- schuppenden Bereich übergeht. Die Hautschuppen sitzen fest. Nach Entfernung einer Schuppe findet man an deren Unterseite einen sog. keratotischen Sporn (Tapeziernagel-Phänomen).
- Zentral zeigt sich ein Gewebsschwund (Atrophie), der vernarbt und in behaarten Hautbezirken zum dauerhaften Haarausfall (Alopezie) führt. UV-Licht und bestimmte Medikamente provozieren die Hautveränderungen.
Tumider Lupus erythematodes
Der Lupus erythematodes tumidus ist eine seltene Variante des diskoiden Lupus erythematodes mit entzündlichen tumorförmigen Infiltraten, die oft im Gesicht entstehen. Die rötlichen Herde sind geschwollen, überwärmt und haben durch Vernarbungen eine gesprenkelte Oberfläche.
Subakut kutaner Lupus erythematodes (SCLE)
Der subakute kutane Lupus erythematodes ist eine seltene Form der Lupus-erythematodes-Gruppe. Er hat eine Intermediärstellung zwischen dem chronisch-kutanen und dem systemischen Lupus erythematodes und zeichnet sich klinisch vor allem durch die erhöhte Lichtempflichkeit speziell gegenüber UV-B aus. Er zeigt psoriasis-ähnliche, runde Herde auf meist Sonnenlicht ausgesetzten Hautarealen. Darüber hinaus sind Gelenk- und Muskelschmerzen, selten auch Nierenbeteiligungen mit milder Symptomatik beschrieben. Bei chronisch schubhaftem Verlauf kann der SCLE sowohl spontan ausheilen als auch in einen systemischen Lupus erythematodes übergehen.[7]
Neonatales LE-Syndrom
Im Falle einer mütterlichen Autoimmunerkrankung wie dem systemischen Lupus erythematodes ist das Risiko für eine Fehlgeburt bis auf etwa 20 % erhöht. Von den übrigen 80 % entwickelt nur ein geringer Anteil einen neonatalen Lupus erythematodes. Grundsätzlich können die Autoantikörper der Mutter ab der 16. Schwangerschaftswoche über den Mutterkuchen auf das Kind übertragen werden. Hier rufen sie bevorzugt Symptome an der Haut und am Herzen hervor. Die Mutter selbst kann zu diesem Zeitpunkt durchaus noch symptomlos sein. In einer prospektiven Studie wurden Hautveränderungen in 16 %, ein AV-Block °III in 1,6 %, erhöhte Leberwerte in 26 % und hämatologische Auffälligkeiten in 27 % der Fälle beschrieben.[8] Symptome an anderen Organen wie den Nieren, den Lungen, dem Nervensystem oder den Blutzellen treten sehr viel seltener auf. Der AV-Block ist auch durch eine immunsuppressive Therapie nicht wieder rückgängig zu machen und muss meist mit einem Schrittmacher behandelt werden. Ansonsten hat die Erkrankung eine gute Prognose, weil die übrigen Symptome mit Abbau der passiv von der Mutter übertragenen Autoantikörper von alleine wieder verschwinden. Da längst nicht alle Kinder von Müttern mit den entsprechenden Autoantikörpern auch Symptome entwickeln, ist eine prophylaktische immunsuppressive Therapie nicht grundsätzlich indiziert. Allerdings wird empfohlen, in solchen Fällen ab der 16. Schwangerschaftswoche regelmäßig Ultraschalluntersuchungen des Herzen des Feten durchzuführen. Wird hierbei ein AV-Block °I oder II gefunden, wird die prophylaktische Behandlung der Mutter mit einem Steroid [9] oder Plasmapherese [10] diskutiert. Wichtig ist die Bestimmung von SS-A/Ro- und SS-B/La-Antikörpern im Blut der Mutter, denn sie verursachen die Veränderungen im Herzmuskelgewebe des ungeborenen Kindes.
Ursache
Die Ätiologie des SLE ist weitgehend unbekannt. Man geht allerdings davon aus, dass Viren (wie der Eppstein-Barr-Virus) oder UV-Licht als ursächliche Faktoren in Frage kommen. Es kommt zur Apoptose von Zellen, sodass deren Kernbestandteile (Autoantigene) freigesetzt werden. Dies gilt insbesondere dann, wenn die Phagozytose der apoptotischen Zellen gestört ist, wie es für eine Subgruppe der SLE-Patienten beschrieben ist.[11] Diese Zellen werden durch das fehlgesteuerte Immunsystem als fremd erkannt, und es werden Antikörper gegen sie gebildet, sogenannte Autoantikörper. Autoantigene und Autoantikörper bilden Immunkomplexe. Diese können vom mononukleären phagozytären System (Makrophagen) nicht beseitigt werden und lagern sich an den verschiedensten Orten (etwa an der Gefäßwand) ab. Es kommt zur Komplementaktivierung, Thrombozytenaktivierung …, und eine Gefäßentzündung (Vaskulitis) entsteht. Daraus entstehen ein Gefäßverschluss und später die Organläsion. Die Kernbestandteile werden jedoch auch auf der Oberfläche der verschiedenen Zellen präsentiert (etwa von Keratinozyten). Das fehlregulierte Immunsystem reagiert darauf, und es kommt zur polyklonalen B-Zell-Aktivierung und zur Produktion von weiteren Autoantikörpern, was dann zur Zerstörung der Zellen führt (s. Schmetterlingserythem).
Die Ursache für diese krankhafte Reaktion des Immunsystems ist bisher unbekannt. Es gibt eine starke genetische Disposition. Familienangehörige ersten und zweiten Grades zeigen eine erhöhte SLE-Prävalenz.[12] Die Wahrscheinlichkeit, dass ein SLE-Patient mindestens einen Verwandten ersten Grades mit SLE hat, wird mit 3 bis 10 Prozent angegeben.[13]. Für eineiige Zwillinge wird eine gemeinsame SLE-Erkrankung von 57 % berichtet, für zweieiige Zwillinge von 5 %.[12] Auch weitere Autoimmunkrankheiten kommen im Verwandtenkreis gehäuft vor.
Clearance Defizienz als ein mögliches Entstehungsmodell für SLE
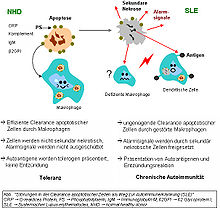
Der präzise Entstehungsmechanismus des Systemischen Lupus erythematodes (SLE) ist ein multifaktorielles Geschehen und noch unklar. Neben den bereits erwähnten Ursachen ist die gestörte Clearance von sterbenden Zellen ein weiterer Grund zur Ausprägung dieser Autoimmunerkrankung. Dies bezieht sich, neben der gesteigerten Apoptoseanfälligkeit, auf die gestörte Phagozytoseaktivität von Monozyten oder Gewebsmakrophagen und Granulozyten sowie auf fehlende oder ineffiziente Serumkomponenten.
Isolierte Monozyten aus peripherem Venenblut von SLE-Patienten zeigen eine verminderte Ausprägung des CD44 Oberflächenmoleküls, das am Phagozytose-Prozess beteiligt ist. Die meisten dieser Monozyten sowie einige der „Sternhimmel-Makrophagen“ (tingible body macrophages, TBM), die in den Keimzentren der Lymphknoten zu finden sind, zeigen außerdem ganz klar einen morphologischen Unterschied bei SLE-Patienten: Sie sind nicht nur vermindert und sterben eher, sondern sie sind auch kleiner und fehlgebildet. Serumkomponenten, wie Komplementfaktoren, C-reaktives Protein und einige Glykoproteine, sind außerdem ausschlaggebend für den funktionierenden Phagozytose-Prozess. Solche Komponenten fehlen oder sind im Serum vieler SLE-Patienten vermindert oder ineffizient.
Die Clearance von früh apoptotischen Zellen ist eine wichtige Funktion im Organismus. Ist diese Fähigkeit gestört und kommt es zum Fortschreiten der Apoptosephasen, so kommt es zur sekundären Nekrose der Zelle. Von nekrotischen Zellen, die ihre Membranintegrität verloren haben, werden Kernbestandteile als Autoantigene sowie danger signals präsentiert, womit die Reifung dendritischer Zellen (DC) stimuliert wird. Eine „ineffiziente Clearance“ wird auch durch ein hohes Aufkommen apoptotischer Zellen ausgelöst. Eine erhöhte Apoptoserate löst somit auch die Reifung der DC aus, sowie die Präsentation der intrazellulären Antigene spät-apoptotischer Zellen oder sekundär-nekrotischer Zellen über deren MHC-Moleküle.
Autoimmunität kann unter anderem durch eine verlängerte Exposition intrazellulärer und nukleärer Autoantigene spät-apoptotischer und sekundär-nekrotischer Zellen initiiert werden. Die B- und T-Zell-Toleranz gegenüber Autoantigenen apoptotischer Zellen geht verloren, und die Lymphozyten werden durch Autoantigene aktiviert. Die Entzündungsreaktion und die Antikörperproduktion durch Plasmazellen resultieren als typisches Krankheitsbild des SLE. Bei Patienten mit Chronisch-diskoidem Lupus erythematodes (CDLE / Hautlupus) wurde dieser Clearance-Defekt ebenfalls festgestellt.
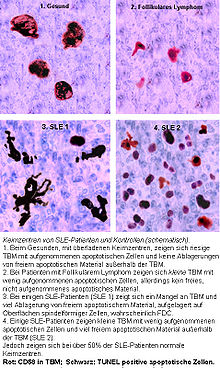
Akkumulation in Keimzentren
Beim Gesunden werden apoptotische Lymphozyten in den Keimzentren der Lymphknoten durch spezialisierte Phagozyten, TBM, effizient abgeräumt, wodurch kein freies apoptotisches und potentiell autoantigenes Material dort vorkommt. Bei SLE-Patienten kommt es dort, aufgrund der ineffizienten Clearance, zur Ablagerung und Anhäufung apoptotischen Materials. In enger Nachbarschaft zu den TBM sind, in dem besonderen Mikromilieu des Keimzentrums, follikuläre dendritische Zellen (FDC) lokalisiert, die im Gegensatz zu den im Knochenmark gereiften dendritischen Zellen (DC) die Antigene auf ihrer Oberfläche binden und sie weder aufnehmen, noch über MHC-Moleküle präsentieren. Autoreaktive B-Lymphozyten gehen, wie nicht-autoreaktive B-Zellen, aus der somatischen Hypermutation von Zentroblasten hervor und wandern in die helle Zone ein. Die durch Zufall gebildeten autoreaktiven B-Lymphozyten erhalten normalerweise keine Überlebenssignale durch FDC und sterben durch Apoptose. Ist die Clearance ineffizient, so kommt es zur Ansammlung apoptotischen Kernmaterials in der hellen Zone der Keimzentren, das durch FDC fixiert wird.
Die FDC, die mit abgelagerten Kern-Autoantigenen beladen sind, können Kurzzeit-Überlebenssignale für autoreaktive B-Lymphozyten darstellen. Finale Überlebenssignale, die die Differenzierung zu autoantikörperproduzierenden Plasmazellen und zu B-Gedächtniszellen zulassen, erhalten die autoreaktiven B-Zellen durch Interaktion mit autoreaktiven T-Helfer-Zellen nach dem Einwandern in die Mantelzone. Die chronische Autoimmunerkrankung SLE kann die Folge sein.
Untersuchung
CDLE (Hautlupus)
Neben dem typischen Hautbild wird oft eine kleine Hautprobe entnommen (Biopsie) und feingeweblich untersucht, um die Diagnosestellung zu sichern. Bei der Untersuchung unter dem Mikroskop zeigen sich in den betroffenen Hautarealen eine Hyperkeratose, Verstärkung der Basalmembran und eine hohe Anzahl von CD4-T-Lymphozyten. Im Rahmen einer Spezialuntersuchung werden fluoreszierende Antikörper eingesetzt, die sich an bestimmte Bereiche der Hautprobe binden und ein typisches Bandenmuster bilden (positiver Lupusband-Test).
SLE (systemischer LE)
Die Diagnose systemischer Lupus erythematodes richtet sich nach den sogenannten ARA-Kriterien (ARA steht für: American Rheumatology Association – 1988 in American College of Rheumatology (ACR) umbenannt). Bei Vorhandensein von 4 der 11 Kriterien kann mit 80- bis 90-prozentiger Sicherheit die Diagnose eines SLE gestellt werden.
ACR- Kriterien (vormals ARA-Kriterien)
Die 11 ACR-Kriterien (1982, revidiert 1997) lauten:[1]
- Schmetterlingserythem: Darunter versteht man eine umschriebene, symmetrische, hellrote, flache bis leicht erhabene Rötung der Wangen, die über dem Nasenrücken zusammenläuft.
- CDLE- typische Hautveränderungen
- Photosensibilität (Überempfindlichkeit gegenüber Licht: Nach Sonneneinstrahlung können beispielsweise Kopfschmerzen, Abgeschlagenheit und Fieber auftreten – dies hat in diesem Zusammenhang nichts mit Sonnenbrand oder Sonnenstich zu tun!)
- Erosionen oder Geschwüre der Mundschleimhaut
- Gelenksschmerzen und Gelenkserguss
- Serositis (Entzündung von sogenannten serösen Häuten wie dem Lungenfell oder dem Herzbeutel)
- Nierenbefall
- Mehr als 0,5 g Eiweiße pro Tag im Urin oder
- krankhafte Harnsedimente wie Blutreste oder Harnzylinder
- Befall des Zentralnervensystems:
- epileptische Anfälle oder
- psychische Krankheiten ohne bekannte metabolische oder medikamentöse Ursache als Auslöser
- hämatologische Symptome
- Hämolytische Anämie oder
- Leukopenie mit Leukozytenzahlen unter 4000 pro mm³ Blut oder
- Lymphopenie mit Lymphozytenzahlen unter 1500 pro mm³ Blut oder
- Thrombozytopenie mit Thrombozytenzahlen unter 100000 pro mm³ Blut
- Immunologische Befunde
- Positives LE-Zellzeichen: In Blutausstrichen sichtbare „hematoxylin bodies“: Darunter versteht man phagozytierte Kernreste in Leukozyten. Diese Kernreste stammen von zerstörten Zellen, an die ein bestimmter, gegen Desoxyribonukleoproteine gerichteter Autoantikörper, der sogenannte „LE-Faktor“, gebunden hatte. Die Untersuchung auf das LE-Zellzeichen wird heutzutage kaum mehr durchgeführt und ist nurmehr von historischem Interesse [1]; oder
- Autoantikörper gegen native DNA oder
- Autoantikörper gegen das Ribonukleoprotein Sm
- Autoantikörper gegen Phospholipide
- Antinukleäre Antikörper (ANA) in der Immunfluoreszenz-Mikroskopie
Behandlung
Allgemeines
Regelmäßige Untersuchungen sind erforderlich, um frühzeitig den Befall von Organen wie etwa Niere oder Herz erkennen zu können. Da UV-Licht die Hauterscheinungen des Lupus erythematodes verschlimmert, ist konsequenter Sonnenschutz notwendig.
Medikamente
Die medikamentöse Therapie des Lupus ist stufenförmig aufgebaut und richtet sich nach der Stärke der Beschwerden, der Organbeteiligung und der Wirksamkeit bei den einzelnen Patienten.
Bei leichter Erkrankung ist in einigen Fällen gar keine oder nur eine symptomatische Behandlung mit Hautcremes und/oder sogenannten NSAR (nichtsteroidalen Antirheumatika) nötig.
Die nächste Stufe ist zumeist das Basistherapeutikum Chloroquin (den DMARDs zugehörig), das auch zur Behandlung von Malaria angewendet wird, häufig kombiniert mit Cortison.
Erreicht man mit diesen Mitteln keine Verbesserung des Zustandes, werden zumeist immunsuppressive Medikamente eingesetzt. Das häufigste und in der Behandlung von Lupus am besten erprobte Medikament ist Azathioprin. Auch mit Cyclosporin A und Mycophenolat-Mofetil werden Erfolge erzielt. Außerdem kommen gelegentlich Zytostatika wie Cyclophosphamid oder Methotrexat zum Einsatz. Auch Thalidomid wird unter strenger Überwachung eingesetzt. Mitunter werden einzelne dieser Medikamente untereinander kombiniert, häufiger ist die Kombination mit Cortison.
Andere Behandlungsmethoden
Andere Behandlungsverfahren sind Immunadsorption, Plasmapherese, Stammzelltransplantation, Immunglobuline und physikalische Therapie.
Empfängnisverhütung
Lange Zeit galt die Einnahme der „Pille“ (orale Empfängnisverhütung – Kontrazeption) bei Patientinnen mit Lupus erythematodes als gefährlich, da man befürchtete, die in der Pille enthaltenen Östrogene könnten zu einem Aufflackern oder zur Verschlimmerung der Erkrankung führen.
Andererseits gibt es gute Gründe für die Anwendung der „Pille“ gerade bei Patientinnen mit Lupus erythematodes
- Geplante Schwangerschaften haben in einer Phase geringer Krankheitsaktivität (Remission) weniger Komplikationen.
- Patienten mit hoher Krankheitsaktivität oder Patientinnen, die fruchtschädigende (teratogene) Medikamente einnehmen müssen, benötigen eine zuverlässige Verhütungsmethode.
- Bei Patientinnen, die Glukokortikoide einnehmen müssen, kann die Einnahme der „Pille“ den damit verbundenen Knochenschwund vermindern und so einer Osteoporose vorbeugen.
- Die Anwendung der Spirale bei gleichzeitiger immunsuppressiver Therapie schützt nicht zuverlässig vor Schwangerschaften und verschleiert unter Umständen Entzündungen im Genitaltrakt.
2005 konnten mehrere Studien[14][15][16] zeigen, dass bei Patientinnen mit inaktiver Erkrankung oder moderater, aber stabiler Krankheitsaktivität die Einnahme von hormonellen Kombinationspräparaten sicher ist, wenn keine Phospholipid-Antikörper nachweisbar sind. Patientinnen mit schwerer Erkrankung, Störungen der Blutgerinnung oder Phospholipid-Antikörpern im Blut sollten die Pille hingegen nicht einnehmen.
Unverträglichkeiten
Allgemein bekannt sind die Unverträglichkeiten auf Carotin (insbesondere in Karotten) und Anisol (insbesondere in Anis, Kümmel und Fenchel).
Besonders zu erwähnen ist die Unverträglichkeit mit dem Wirkstoff Diclofenac (wie in Voltaren), der in verschiedenen Rheumamedikamenten vorkommt. Dieser Wirkstoff kann bei Lupuspatienten zu einem Schub der Krankheit bis zum (tödlichen) allergischen Schock führen. Bei Einnahme ist besondere Vorsicht und Rücksprache mit dem Arzt nötig[17].
Geschichte
Die Erkrankung ist seit dem Mittelalter bekannt. Der Name Lupus stammt von dem Lombarden Roger Frugardi (um 1140–1195). Der Franzose Pierre Louis Alphée Cazenave beschrieb 1851 die Erkrankung als Erster in einer wissenschaftlich akkuraten Form.[18]
Trivia
Durch die TV-Serie Dr. House wurde Lupus einer breiteren Öffentlichkeit als Krankheit bekannt, da die (Ablehnung einer) Diagnose auf Lupus zu einem wiederkehrenden Element in der Serie wurde. Der Erfinder von House, David Shore, erhielt vom Los-Angeles-Zweig der Lupus-Stiftung den Loop Award dafür, das Bewusstsein für Lupus zu fördern[19].
Siehe auch
- Lupus pernio
- Lupus vulgaris (Hauttuberkulose)
- Antiphospholipid-Syndrom
- CREST-Syndrom
Weiterführende Literatur
- J. J. Manson und A. Rahman: Systemic lupus erythematosus. In: Orphanet Journal of Rare Diseases 1, 2006, 6. doi:10.1186/1750-1172-1-6 (Review, Open Access)
Weblinks
 Commons: Systemic lupus erythematosus – Sammlung von Bildern, Videos und Audiodateien
Commons: Systemic lupus erythematosus – Sammlung von Bildern, Videos und Audiodateien- Bilder der Lupus-Hautveränderungen bei DermIS
- Engl. Informationen zu SLE (U.S. National Library of Medicine und NIH)
- Manson JJ, Rahman A: Systemic lupus erythematosus. Orphanet J Rare Dis. 2006 Mar 27;1:6. PMID 16722594
- "Associations between ambient fine particulate levels and disease activity in systemic lupus erythematosus (SLE)": [1]
- Sandra Stocks: Dissertation (Uni Düsseldorf, 2006)
Einzelnachweise
- ↑ a b c d e Peter Fritsch: „Dermatologie und Venerologie“, Springer Verlag, 2. Auflage 2004, ISBN 3-540-00332-0
- ↑ G. Bein und H. Hackstein: Warum ist Lupus Erythematodes eine Frauenkrankheit? In: Biol Unserer Zeit 2007;3(27): S. 154–155
- ↑ Mona Holdack-Janssen: Assoziation von MICB-Allelen mit dem Systemischen Lupus Erythematodes, S. 4 (Zugriff am 18. August 2010)
- ↑ Meller S, Homey B, Ruzicka T: Socioeconomic factors in lupus erythematosus. In: Autoimmun Rev. 4, Nr. 4, April 2005, S. 242–6. doi:10.1016/j.autrev.2004.11.008. PMID 15893719.
- ↑ Hettenkofer, Hans-Jürgen [Hg.]: Rheumatologie. Stuttgart: Thieme Verlag, 1998, S. 91
- ↑ Kumar, Vinay et al. [Hg]: Robbins and Cotran Pathologic Basis of Disease, 8th Edition. Philadelphia: Saunders Elsevier, 2010, S. 217
- ↑ Gernot Rassner: Dermatologie. Lehrbuch und Atlas. 9., durchgesehene und aktualisierte Auflage. Elsevier, München 2009, ISBN 978-3-437-42763-3, S. 183.
- ↑ R. Cimaz, D. L. Spence, L. Hornberger et al.: Incidence and spectrum of neonatal lupus erythematosus: a prospective study of infants born to mothers with anti-Ro autoantibodies. In: J Pediatr 2003;142: 678–683
- ↑ V. Wahn: Neonataler Lupus erythematodes. In: Monatsschrift Kinderheilkunde 2006, 154:1203–1206
- ↑ E. Feist et al: Erfolgreiches therapeutisches Management einer Risikoschwangerschaft bei primärem Sjögren-Syndrom mit Plasmapherese und Dexamethason. In: Zeitschrift für Rheumatologie 55 (1996), Nr. 2, S. 127-132
- ↑ M. Herrmann u. a.: Arthritis and Rheumatism. 41, 1998, S. 1241–1250.
- ↑ a b Peter, Pichler: Klinische Immunologie. 1996, S. 348.
- ↑ Miehle: Rheumatologie in Praxis und Klinik. 2000, S. 911.
- ↑ Petri M, Kim MY, Kalunian KC, et al: Combined oral contraceptives in women with systemic lupus erythematosus. N Engl J Med 2005;353:2550–2558
- ↑ Sánchez-Guerrero J, Uribe AG, Jiménez-Santana L, et al: A trial of contraceptive methods in women with systemic lupus erythematosus. N Engl J Med 2005;353:2539–2549.
- ↑ Sánchez-Guerrero J, Uribe AG, Jiménez-Santana L, et al. A trial of contraceptive methods in women with systemic lupus erythematosus. N Engl J Med 2005;353:2539–2549. „One patient receiving combined oral contraceptives died from amoxicillin-related severe neutropenia“
- ↑ Nachzulesen im Beipackzettel von Diclofenac
- ↑ D. J. Wallacea: Pierre Cazenave and the first detailed modern description of lupus erythematosus. In: Seminars in Arthritis and Rheumatism 28, 1999, S. 305–313. doi:10.1016/S0049-0172(99)80014-6
- ↑ Lupus LA – Lupus LA Presents An Evening of Love, Light & Laughter

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- Krankheitsbild in der Rheumatologie
- Autoimmunerkrankung
Wikimedia Foundation.