- Atmosphärengase
-
Als Luft bezeichnet man das Gasgemisch der Erdatmosphäre. Trockene Luft besteht hauptsächlich aus den zwei Gasen Stickstoff (rd. 78 %) und Sauerstoff (rd. 21 %). Daneben gibt es noch die Komponenten Argon (0,9 %), Kohlenstoffdioxid (0,04 %), Wasserstoff und andere Gase in Spuren. Wasserdampf ist in wechselnden Mengen (im Mittel 0,4 %) enthalten, aber in den obigen Werten nicht mitgerechnet. Im natürlichen Zustand ist die Luft geruch- und geschmacklos.
Der in der Luft enthaltene Sauerstoff ist für alle aeroben Landlebewesen überlebensnotwendig, die ihn zur Atmung benötigen. Pflanzen nutzen das in der Luft enthaltene Kohlenstoffdioxid zur Photosynthese. Für fast alle Pflanzen ist dies die einzige Kohlenstoffquelle.
Inhaltsverzeichnis
Zusammensetzung
Zusammensetzung der Luft Gas Formel Volumenanteil Massenanteil Hauptbestandteile der trockenen Luft bei Normalnull Stickstoff N2 78,084 % 75,518 % Sauerstoff O2 20,942 % 23,135 % Argon Ar 0,934 % 1,288 % Zwischensummen 99,960 % 98,941 % Gehalt an Spurengasen Kohlenstoffdioxid CO2 0,038 % 0,058 % Neon Ne 18,180 ppm 12,67 ppm Helium He 5,240 ppm 0,72 ppm Methan CH4 1,760 ppm 0,97 ppm Krypton Kr 1,140 ppm 3,30 ppm Wasserstoff H2 ~500 ppb 36 ppb Distickstoffoxid N2O 317 ppb 480 ppb Kohlenstoffmonoxid CO 50–200 ppb 50–200 ppb Xenon Xe 87 ppb 400 ppb Dichlordifluormethan (CFC-12) CCl2F2 535 ppt 2200 ppt Trichlorfluormethan (CFC-11) CCl3F 226 ppt 1100 ppt Chlordifluormethan (HCFC-22) CHClF2 160 ppt 480 ppt Tetrachlorkohlenstoff CCl4 96 ppt 510 ppt Trichlortrifluorethan (CFC-113) C2Cl3F3 80 ppt 520 ppt Methylchloroform CH3-CCl3 25 ppt 115 ppt 1,1-Dichlor-1-Fluorethan (HCFC-141b) CCl2F-CH3 17 ppt 70 ppt 1-Chlor-1,1-difluorethan (HCFC-142b) CClF2-CH3 14 ppt 50 ppt Schwefelhexafluorid SF6 5 ppt 25 ppt Bromchlordifluormethan CBrClF2 4 ppt 25 ppt Bromtrifluormethan CBrF3 2,5 ppt 13 ppt Gesamtmasse (trocken) 5,135 · 1015 t Gesamtmasse (feucht) 5,148 · 1015 t Die Zusammensetzung der Luft in der Höhe von Normalnull ist in der Tabelle rechts wiedergegeben, wobei man zwischen Hauptbestandteilen und Spurengasen unterscheidet. Luft kann mittels Destillation von flüssiger Luft in ihre Bestandteile zerlegt werden, dies erfolgt meistens mit Hilfe des Linde-Verfahrens.
Stickstoff
Als ein chemisch inertes Gas ist der in molekularer Form auftretende Stickstoff äußerst reaktionsträge. Im Stickstoffkreislauf kann er nur durch die Prozesse der Stickstofffixierung in für Lebewesen nutzbare Verbindungen überführt werden, die ihn für den Aufbau ihrer Aminosäuren benötigen. Den gegenteiligen Prozess bezeichnet man als Denitrifikation. Diese Prozesse gleichen sich weitestgehend aus und haben mengenmäßig keinen Effekt auf die Konzentration des Stickstoffs in der Atmosphäre. Technisch wird der Luftstickstoff über das Haber-Bosch-Verfahren zur Düngemittelherstellung verwendet.
Beim Tauchen in größere Tiefen (mehr als 60 m) wird Stickstoff in der Druckflasche durch Helium ersetzt, da Stickstoff bei einem zu hohem Partialdruck (ab 3,2 bar, entspricht ca. 30 m) zunehmend narkotisch wirkt, was zu dem sogenannten Tiefenrausch führt. (siehe auch Atemgas)
Sauerstoff
Der Sauerstoff der Luft ist über die Photosynthese entstanden, wobei die im Laufe der Erdgeschichte hergestellte Menge etwa das zwanzigfache der heute in der Atmosphäre vorliegenden Menge beträgt. Er verleiht der heutigen Atmosphäre ihren oxidierenden Charakter und stellt das wichtigste Oxidationsmittel dar, das für die biologische Atmung und die chemischen Verbrennungsvorgänge benötigt wird.
Auf den menschlichen Körper wirkt Sauerstoff ab einem Partialdruck von rd. 1,5 Bar giftig, das entspricht bei der Sauerstoffkonzentration der Luft einem Überdruck von sechs Bar.
Argon
Argon ist ein Edelgas, als solches reaktionsträge und ohne große Bedeutung für die Chemie. Dank seiner Reaktionsträgheit wird Argon beim Schweißen als Schutzgas eingesetzt oder auch wegen seiner relativ zur Luft kleineren Wärmeleitfähigkeit als Dämmung für Fensterscheiben (Isolierverglasung). In Glühlampen kommt Argon wegen dieser beiden Eigenschaften zum Einsatz.
Wasserdampf
Umgebungsluft ist nicht komplett trocken, sondern enthält zusätzlich je nach Luftfeuchtigkeit bis zu etwa vier Volumenprozent Wasserdampf. Der Wasserdampfgehalt schwankt zwischen einem Zehntel Volumenprozent an den Polen und drei Volumenprozent in den Tropen, mit einem Mittelwert von 1,3 % in Bodennähe; er wird durch unterschiedliche Feuchtemaße angegeben. Wasserdampf ist leichter als Luft (62,5 % des Luftgewichtes) und steigt daher nach oben, kondensiert aber zu Wassertröpfchen (Wolken), sobald er entsprechend kalte Luftschichten erreicht. Oberhalb davon ist der Wasserdampfgehalt deshalb sehr gering, sodass er gemittelt über die gesamte Atmosphäre nur 0,4 % beträgt.
Variabilität in der Zeit
Die Konzentrationen der Atmosphärengase sind ihrem Charakter nach metastabil, denn auch wenn sie sich in der Lebenszeit eines Menschen nur geringfügig ändern, so sollten sie deswegen nicht mit Naturkonstanten verwechselt werden. Dies zeigt sich in der seit Jahrmilliarden andauernden Entwicklung der Erdatmosphäre, die auch heute noch nicht abgeschlossen ist und in deren Zuge sich die Zusammensetzung der Erdatmosphäre mehrmals grundlegend gewandelt hat. Erst seit etwa 350 Millionen Jahren kann man dabei von unserer heutigen Atmosphäre sprechen.
Die größten aktuellen Veränderungen der Luftzusammensetzung stellt die Zunahme des Kohlenstoffdioxidgehaltes um etwa 40 % seit Beginn der Industrialisierung dar. Dies ist im Zusammenhang mit dem anthropogenen Treibhauseffekt eine der Ursachen für die globale Erwärmung. Formal gehört Kohlenstoffdioxid dabei zu den Spurengasen, es wird als das fünfthäufigste Atmosphärengas und aufgrund seiner Bedeutung für Klima und Lebewesen jedoch häufig zu den Hauptbestandteilen der Luft gerechnet.
Größere Schwankungen über teils wenige Jahre und Jahrzehnte sind auch bei den Spurengasen zu verzeichnen. Deren niedrige Konzentrationen können schon durch vergleichsweise geringe anthropogene Emissionen beeinflusst werden. Ebenso zeigen Vulkanausbrüche häufig einen kurzfristigen Einfluss.
Variabilität im Raum
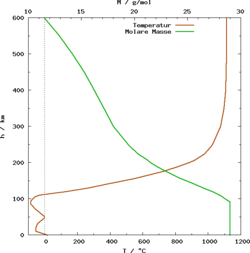 Durchschnittliche Temperatur und molare Masse in Abhängigkeit von der Höhe. (Grafik muss überarbeitet werden, Daten sind falsch abgetragen.)
Durchschnittliche Temperatur und molare Masse in Abhängigkeit von der Höhe. (Grafik muss überarbeitet werden, Daten sind falsch abgetragen.)Die angegebenen Konzentrationen stellen globale Mittelwerte dar und beziehen sich auf Normalnull, besitzen aber eine weitestgehende Gültigkeit in der gesamten Homosphäre, also bis in eine Höhe von etwa 100 Kilometern. Da in verschiedenen Höhenlagen spezifische Prozesse der Atmosphärenchemie wirken, gibt es jedoch auch teilweise erhebliche Abweichungen. Ab der Homopause stellt die Abnahme der Konzentration schwerer Gase mit der Höhe und damit die relative Anreicherung leichterer Gase einen generellen Trend dar. In der hohen Atmosphäre sind daher Wasserstoff und Helium anteilsmäßig sehr viel bedeutender als in Bodennähe, jedoch ist die Luftdichte und damit das absolute Vorkommen der Gase entsprechend gering.
Substanzen geringerer Konzentration
Zusätzlich sind auch hier nicht aufgelistete Anteile von Wasserdampf, Methan, Distickstoffoxid (sinkend ab 7 km), Kohlenstoffmonoxid und Ozon vorhanden.
Außerdem treten folgende Stoffe in geringen Spuren auf:
- Fluoroform
- Peroxyacetylnitrat
- Chloroxide
- andere Stickoxide (neben N2O)
- Schwefeldioxid
- Radon
- Quecksilber
Kohlenstoffdioxid
Die biologische Hauptbedeutung des Kohlenstoffdioxids (umgangssprachlich oft auch als Kohlendioxid bezeichnet) liegt in seiner Rolle als Kohlenstofflieferant für die Photosynthese, weshalb sich die atmosphärische Kohlenstoffdioxidkonzentration stark auf das Pflanzenwachstum auswirkt. Durch den lichtabhängigen Stoffwechselzyklus der Pflanzen, also der Wechselbeziehung zwischen Atmung und Photosynthese, können die bodennahen CO2-Konzentration im Tagesgang schwanken. Es zeigt sich bei ausreichender Pflanzendecke ein nächtliches Maximum und dementsprechend ein Minimum am Tag. Der gleiche Effekt kommt auch im Jahresverlauf zum tragen, da die außertropische Vegetation ausgeprägte Vegetationsperioden besitzt. Dies hat auf der Nordhalbkugel ein Maximum im Zeitraum März bis April und ein Minimum im Oktober oder November zur Folge. Auch anthropogene (vom Menschen herbeigeführte) Emissionszyklen können eine Rolle spielen, zum Beispiel mit dem Einsetzen der Heizperiode bei sinkenden Temperaturen.
Ozon
Ozonwerte werden nicht in Anteilen, sondern in der Dobson-Einheit angegeben. Da die Werte zudem von der Höhe (Ozonschicht, Bodennahes Ozon), sowie von Wetterlage, Temperatur, Schadstoffbelastung und Uhrzeit abhängen, und Ozon sich sowohl schnell bildet als auch wieder zerfällt, ist es in obiger Tabelle nicht aufgelistet.
Kohlenstoffmonoxid
Kohlenstoffmonoxid (umgangssprachlich oft auch als Kohlenmonoxid bezeichnet) ist ein unsichtbares brennbares giftiges Gas, das bei Verbrennungen mit Sauerstoffmangel entsteht. Es blockiert den Sauerstofftransport im Blut und kann schon in geringen Dosen zum Tod führen. Auch schädigt es die Photosynthese der Pflanzen. Es wird u. a. in Automotoren erzeugt, so dass Autoabgase ohne Abgasnachbehandlung durch einen Katalysator bis zu 4 % Kohlenstoffmonoxid enthalten sollen. Die Hauptquelle für Kohlenstoffmonoxid sind jedoch mit ca. 60 % Emissionen aufgrund von Bränden der Vegetation.
Physikalische Größen der Luft
Temperaturabhängigkeit Temperatur
[°C]Schallgeschwindigkeit
[m/s]Luftdichte
[kg/m3]Schallkennimpedanz
[N·s/m3]−10 325,4 1,341 436,6 −5 328,5 1,317 432,5 0 331,5 1,293 428,5 +5 334,5 1,270 424,6 +10 337,5 1,247 420,8 +15 340,5 1,225 417,1 +20 343,4 1,204 413,5 +25 346,3 1,184 410,0 +30 349,2 1,164 406,6 Luftdichte
Unter Normalbedingungen ist die Luftdichte gleich 1,293 kg/m3.
Luftdruck
Die Gewichtskraft der von der Erdanziehung beschleunigten Luftsäule erzeugt einen statischen Luftdruck, der mit dem jeweiligen Messpunkt variiert. Dieser ist jedoch zusätzlich von thermischen (Temperatur) und dynamischen Einflüssen (Wetterbedingungen) abhängig. Über einem Quadratmeter Bodenfläche beträgt die Luftmasse dem Luftdruck entsprechend etwa 10.000 kg.
Lufttemperatur
Als Lufttemperatur wird jene Temperatur der bodennahen Atmosphäre bezeichnet, die weder von Sonnenstrahlung noch von Bodenwärme oder Wärmeleitung beeinflusst ist.
Die genaue Definition durch Wissenschafter und Techniker ist je nach Fachgebiet etwas verschieden. In der Meteorologie wird die Lufttemperatur in einer Höhe von zwei Metern gemessen, wofür die klassischen, weiß gestrichenen Wetterhäuschen in freier Umgebung dienen.
Luftfeuchtigkeit
Bei der Luftfeuchtigkeit handelt es sich um den Anteil des Wasserdampfes an der Luft. Sie wird über verschiedene Feuchtmaße wie Dampfdruck und Taupunkt sowie relative, absolute und spezifische Luftfeuchte quantifiziert.
Andere
Unter Normalbedingungen ist die Schallgeschwindigkeit gleich 331,5 m/s.
Trockene Luft hat eine molare Masse von 28,9644 g/mol (Wert der Standardatmosphäre; der tatsächliche Wert schwankt etwas mit der genauen Zusammensetzung der Luft). Die Molmasse von Wasserdampf beträgt nur ca. 18 g/mol. Deshalb ist feuchte Luft geringfügig leichter.
Die Brechzahl der Luft beträgt unter Normalbedingungen für sichtbares Licht ungefähr 1,00029. Sie hängt von Druck, Temperatur und Zusammensetzung der Luft ab, vor allem aber von der Luftfeuchtigkeit. Entsprechend der Brechzahl ändert sich auch die Lichtgeschwindigkeit innerhalb der Luft.
Spezifische Wärmekapazität:
- cp = 1,005 kJ/(kg·K) = 0,279 kWh/(Tonne·K) (isobar)
- cv = 0,718 kJ/(kg·K) = 0,199 kWh/(Tonne·K) (isochor)
Luftverunreinigung und Luftreinhaltung
Die Luftverschmutzung ist der auf die Luft bezogene Teilaspekt der Umweltverschmutzung. Gemäß dem Bundes-Immissionsschutzgesetz ist Luftverunreinigung eine Veränderung der natürlichen Zusammensetzung der Luft, insbesondere durch Rauch, Ruß, Staub, Aerosole, Dämpfe oder Geruchsstoffe. Von besonderer Schädlichkeit sind dabei erhöhte Ozonwerte (Smog) und Schwefeldioxidkonzentrationen (saurer Regen).
In den meisten Industrieländern ist die lokale Luftverschmutzung aufgrund von gesetzlichen Vorgaben zur Luftreinhaltung in den letzten Jahrzehnten stark zurückgegangen. Gleichzeitig hat jedoch der Ausstoß von Treibhausgasen wie Kohlendioxid weiter zugenommen. Die lokale und regionale Luftverschmutzung ist aber insbesondere für Länder der Dritten Welt sowie Schwellenländer wie zum Beispiel China noch ein erhebliches Problem.
Kulturelle Bedeutung
Die griechischen Naturphilosophen hielten Luft für eines der vier Grundelemente, aus denen alles Sein besteht. Dem Element Luft wurde der Oktaeder als einer der fünf Platonischen Körper zugeordnet.
Siehe auch
Weblinks
Wikimedia Foundation.
