- Helium
-
Eigenschaften Allgemein Name, Symbol, Ordnungszahl Helium, He, 2 Serie Edelgase Gruppe, Periode, Block 18, 1, s Aussehen Farbloses Gas CAS-Nummer 7440-59-7 ATC-Code V03AN03
Massenanteil an der Erdhülle 0,004 ppm[1] Atomar [2] Atommasse 4,002602(2)[3] u Kovalenter Radius 28 pm Van-der-Waals-Radius 140 pm Elektronenkonfiguration 1s2 1. Ionisierungsenergie 2372,3 kJ/mol 2. Ionisierungsenergie 5250,5 kJ/mol Physikalisch [2] Aggregatzustand gasförmig Dichte 0,1785 kg·m−3[4] Magnetismus diamagnetisch (χm = −1,1 · 10−9)[5] Schmelzpunkt 0,95 K (-272,2 °C)(bei 2,5 MPa) Siedepunkt 4,22 K (-268,93 °C) Molares Volumen (fest) 21,00 · 10−6 m3/mol Verdampfungswärme 0,083 kJ/mol Schmelzwärme 0,02 kJ/mol Schallgeschwindigkeit 970 m/s bei 273,15 K Spezifische Wärmekapazität 5193 J/(kg · K) Wärmeleitfähigkeit 0,1513 W/(m · K) Chemisch [2] Oxidationszustände 0 Oxide (Basizität) keine (keine) Elektronegativität 5,2 (Durchschnitt),[6] 2,2[7] (Pauling-Skala) Isotope Isotop NH t1/2 ZM ZE (MeV) ZP 3He 0,000137 %
Stabil 4He 99,999863 %
Stabil 5He 7,618 · 10−22 s n 0,60 4He 6He 806,7 ms β− 3,508 6Li Weitere Isotope siehe Liste der Isotope NMR-Eigenschaften Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [4] 
Achtung
H- und P-Sätze H: 280 EUH: keine EUH-Sätze P: 403 [4] Gefahrstoffkennzeichnung [8] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: 9-23 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet.
Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen.Helium (altgr. ἥλιος hélios „Sonne“) ist ein chemisches Element mit dem Elementsymbol He und der Ordnungszahl 2. Im Periodensystem steht es in der 18. Gruppe (früher 8. Hauptgruppe) und zählt damit zu den Edelgasen. Es ist ein farbloses, geruchloses, geschmacksneutrales, ungiftiges Gas.
Helium bleibt bis zu sehr tiefen Temperaturen gasförmig, erst nahe dem absoluten Nullpunkt wird es flüssig. Es ist die einzige Substanz, die bei Normaldruck selbst am absoluten Nullpunkt (0 K bzw. −273,15 °C) nicht fest wird. Helium ist die Substanz mit der größten bekannten chemischen Reaktionsträgheit. Auch unter Extrembedingungen konnten bis jetzt keine Verbindungen des Heliums nachgewiesen werden, die nicht sofort nach der Bildung zerfallen. Soweit bekannt, kommt Helium nur atomar vor. Das häufigste stabile Isotop ist 4He; ein weiteres stabiles Isotop ist das sehr seltene 3He.
Das Verhalten der beiden flüssigen Phasen Helium I rsp. Helium-I sowie Helium II bzw. Helium-II (insbesondere das Phänomen der Suprafluidität) von 4He ist Gegenstand aktueller Forschungen auf dem Gebiet der Quantenmechanik. Weiterhin ist flüssiges Helium ein unverzichtbares Hilfsmittel zur Erzielung der tiefsten Temperaturen, die unter anderem zur Kühlung von Infrarotdetektoren von Weltraumteleskopen und zur Untersuchung von Eigenschaften wie zum Beispiel der Supraleitung von Materie bei Temperaturen nahe dem absoluten Nullpunkt erforderlich sind.
Helium ist, nach Wasserstoff, das zweithäufigste Element im Universum. Nach anerkannter Theorie vereinigten sich 10 Sekunden nach dem Urknall Protonen und Neutronen durch Kernfusion zu ersten Atomkernen. Aus deren gesamter Masse bildeten sich dabei unter anderem 25 % 4He und 0,001 % Deuterium, sowie Spuren von 3He. Somit ist der größte Teil Helium schon beim Urknall entstanden. Das im Inneren von Sternen durch Fusion von Wasserstoff entstandene Helium fusionierte zum größten Teil weiter zu schwereren Elementen.
Auf der Erde wird 4He in Form von Alphateilchen bei dem Alphazerfall verschiedener radioaktiver Elemente wie zum Beispiel Uran oder Radium gebildet. Helium entsteht daraus, wenn das Alphateilchen anderen Atomen zwei Elektronen entreißt. Das so entstandene Helium sammelt sich in natürlichen Erdgas-Vorkommen in Konzentrationen bis zu sieben Volumenprozent. Daher kann Helium durch Fraktionierte Destillation aus Erdgas gewonnen werden.
Erste Hinweise auf Helium wurden 1868 durch den französischen Astronomen Jules Janssen bei Untersuchungen des Lichtspektrums der Chromosphäre der Sonne entdeckt, wobei er die bis dahin unbekannte gelbe Spektrallinie von Helium fand.
Helium findet Anwendungen in der Tieftemperaturtechnik, besonders als Kühlmittel für supraleitende Magneten, in Tiefsee-Atemgeräten, bei der Altersbestimmung von Gesteinen, als Füllgas für Luftballons, als Traggas für Luftschiffe und als Schutzgas für verschiedene industrielle Anwendungen (zum Beispiel beim Metallschutzgasschweißen und bei der Herstellung von Silizium-Wafern). Nach dem Einatmen von Helium verändert sich aufgrund der im Vergleich zu Luft höheren Schallgeschwindigkeit kurzzeitig die Stimme („Micky-Maus-Stimme“).
Inhaltsverzeichnis
Geschichte
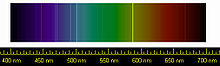 Die Spektrallinien von Helium (nicht nur die gelbe)[9]
Die Spektrallinien von Helium (nicht nur die gelbe)[9]
Hinweise auf das Element Helium erhielt man zum ersten Mal aufgrund einer hellen gelben Spektrallinie bei einer Wellenlänge von 587,49 Nanometern im Spektrum der Chromosphäre der Sonne. Diese Beobachtung machte der französische Astronom Jules Janssen während einer totalen Sonnenfinsternis in Indien am 18. August 1868. Als er seine Entdeckung bekannt machte, wollte ihm zunächst niemand glauben, da bislang noch nie ein neues Element im Weltall gefunden wurde, bevor der Nachweis auf der Erde geführt werden konnte. Am 20. Oktober desselben Jahres bestätigte der Engländer Norman Lockyer, dass die gelbe Linie tatsächlich im Sonnenspektrum vorhanden ist und schloss daraus, dass sie von einem bislang unbekannten Element verursacht wurde. Weil diese Spektrallinie nahe an der so genannten Fraunhofer D-Linie lag, nannte er die Linie D3, um sie von den nahe liegenden D1- und D2-Linien des Natriums unterscheiden zu können. Er und sein englischer Kollege Edward Frankland schlugen vor, das neue Element nach dem griechischen Wort für Sonne zu benennen. Da sie annahmen, dass es sich bei dem Element um ein Metall handelte, hängten sie statt der für Edelgase üblichen Endung -on die neutrale Endung -ium an.
Luigi Palmieri gelang es 1882, durch die Spektralanalyse von Vesuv-Lava erstmals das Element Helium auf der Erde nachzuweisen.
Am 23. März 1895 gewann der britische Chemiker William Ramsay Helium, indem er das Uran-Mineral Cleveit, eine Varietät des Uraninits, mit Mineralsäuren versetzte und das dabei austretende Gas isolierte.[10] Er war auf der Suche nach Argon, konnte jedoch die gelbe D3-Linie beobachten, nachdem er Stickstoff und Sauerstoff von dem isolierten Gas getrennt hatte. Dieselbe Entdeckung machten fast gleichzeitig der britische Physiker William Crookes und die schwedischen Chemiker Per Teodor Cleve und Nicolas Langlet in Uppsala in Schweden. Diese sammelten ausreichende Mengen des Gases, um dessen Atommasse feststellen zu können.
Bei einer Ölbohrung in Dexter in Kansas wurde eine Erdgasquelle gefunden, deren Erdgas zwölf Volumenprozent eines unbekannten Gases enthielt. Die amerikanischen Chemiker Hamilton Cady (1874–1943) und David McFarland der Universität von Kansas fanden 1905 heraus, dass es sich dabei um Helium handelte. Sie publizierten eine Meldung, dass Helium aus Erdgas gewonnen werden kann. Im selben Jahr stellten Ernest Rutherford und Thomas Royds fest, dass Alphateilchen Heliumkerne sind.
Die erste Verflüssigung von Helium wurde 1908 vom niederländischen Physiker Heike Kamerlingh Onnes durchgeführt, indem er das Gas auf eine Temperatur von unter 1 K kühlte. Festes Helium konnte er auch bei weiterem Abkühlen nicht erhalten, dies gelang erst 1926 Willem Hendrik Keesom, einem Schüler Onnes’, durch Komprimieren des Heliums auf 25 bar bei analoger Temperatur. Onnes beschrieb zuerst das Phänomen suprafluider Flüssigkeiten, das heute als Onnes-Effekt bekannt ist.
Im frühen 20. Jahrhundert wurden große Mengen Helium in Erdgasfeldern der amerikanischen Great Plains gefunden und damit wurden die Vereinigten Staaten zum führenden Weltlieferanten für Helium. Nach einem Vorschlag von Sir Richard Threlfall (1861–1932) förderte die US-Marine drei kleine experimentelle Heliumproduktionsbetriebe während des Ersten Weltkrieges, um Helium als Füllgas für Sperrballone zu gewinnen. Eine Gesamtmenge von 5.700 Kubikmeter Gas mit einem Heliumanteil von 92 % wurde von diesen Betrieben hergestellt. Dieses Helium wurde im ersten heliumgefüllten Luftschiff der Welt benutzt, dem C-7 der US-Navy, das seine Jungfernfahrt auf der Strecke von Hampton Roads in Virginia nach Boiling Field in Washington, D. C. am 7. Dezember 1921 bestritt.
Die Regierung der USA ließ 1925 die National Helium Reserve in Amarillo in Texas errichten, um eine Versorgung von militärischen Luftschiffen in Kriegszeiten und Verkehrsluftschiffen in Friedenszeiten zu sichern. Das Lager befindet sich in einer natürlichen Gesteinsformation 20 km nordwestlich von Amarillo. Obwohl die Nachfrage nach dem Zweiten Weltkrieg sank, wurde die Förderungsanlage in Amarillo erweitert, damit flüssiges Helium als Kühlmittel für Sauerstoff-Wasserstoff-Raketentreibstoff und andere zu kühlende Gegenstände bereitgestellt werden konnte. Der Heliumverbrauch der USA stieg im Jahr 1965 auf das Achtfache des Spitzenverbrauchs in Kriegszeiten.
Nachdem in den USA das Helium Acts Amendments of 1960 (Public Law 86-777) beschlossen wurde, wurden weitere fünf private Heliumförderanlagen errichtet. Das US-Minenministerium ließ dafür eine 685 Kilometer lange Pipeline von Bushton in Kansas nach Amarillo in Texas bauen; dieses Lager enthielt 1995 rund eine Milliarde Kubikmeter Helium und 2004 etwa das Zehnfache des Weltjahresbedarfs an Helium.
Die Reinheit des gewonnenen Heliums stieg nach dem Zweiten Weltkrieg rasant an. Wurde 1945 noch eine Mischung von 98 % Helium und 2 % Stickstoff für Luftschiffe benutzt, konnte 1949 bereits Helium mit einer Reinheit von 99,995 % kommerziell vertrieben werden. Um diesen Reinheitsgrad zu erreichen, ist Aktivkohle nötig, um verbliebene Verunreinigungen – meistens bestehend aus Neon – mittels Druckwechsel-Adsorption zu entfernen.
Vorkommen
Im Weltall
 Helium macht ungefähr 19 % von Neptuns äußeren Gasschichten aus. Neptuns Hauptbestandteil ist Wasserstoff; die blaugrüne Färbung entsteht durch Methan.
Helium macht ungefähr 19 % von Neptuns äußeren Gasschichten aus. Neptuns Hauptbestandteil ist Wasserstoff; die blaugrüne Färbung entsteht durch Methan.
Nach der Urknalltheorie entstand der größte Teil des heute im Weltraum vorhandenen Heliums in den ersten drei Minuten nach dem Urknall. Helium ist nach Wasserstoff das zweithäufigste Element. 23 % der Masse der sichtbaren Materie bestehen aus Helium, obwohl Wasserstoffatome achtmal häufiger sind. Außerdem wird Helium durch Kernfusion in Sternen produziert. Dieses so genannte Wasserstoffbrennen liefert die Energie, die die Sterne auf der Hauptreihe, also die Mehrheit aller Sterne, zum Leuchten bringt. Dieser Prozess liefert den Sternen die Energie für den größten Teil ihres Lebens. Wenn der größte Teil des Wasserstoffes am Ende des Lebens eines Sterns im Kern aufgebraucht ist, zieht sich der Kern zusammen und erhöht seine Temperatur. Dadurch kann nun Helium zu Kohlenstoff verbrannt werden (Heliumflash, Heliumbrennen). In einer Schale um diesen Kern findet weiterhin das Wasserstoffbrennen statt. Auch Kohlenstoff kann weiter zu anderen Elementen verbrannt werden. Dieser Prozess wird normalerweise bis zum Eisen fortgesetzt, falls keine Supernovaexplosion auftritt. Bei einer Supernovaexplosion werden auch schwerere Elemente als Eisen synthetisiert, die durch die Explosion im Weltraum verteilt werden. Im Verlauf der Zeit reichert sich die interstellare Materie dadurch mit Helium und schwereren Elementen an, sodass später entstandene Sterne auch einen größeren Anteil an Helium und schwereren Elementen haben.
Auf Sternoberflächen und in Nebeln kommt Helium bevorzugt neutral oder einfach ionisiert vor. Anders als in der Physik und Chemie üblich wird in der Astronomie aber nicht die Notation mit hochgestelltem „+“ (He+) verwendet, da andere Elemente so hochionisiert vorkommen können, dass diese Notation unpraktisch wird, zum Beispiel sechzehnfach ionisiertes Eisen in der Sonnenkorona. Daher werden Ionisationsstufen in der Astronomie mit römischen Ziffern bezeichnet, wobei neutrales Helium als He I bezeichnet wird, einfach ionisiertes entsprechend He II und vollständig (= zweifach) ionisiertes als Helium III (Helium-III).
Helium ist auch in verschiedenen Planetatmosphären vorhanden:
Neptun 19 % ± 3,2 % Uranus 15,2 % ± 3,3 % Jupiter 10,2 % Merkur 6 % Saturn 3,25 % Venus 12 ppm Erde 5,2 ppm Meteoriten und Mond
Helium kann in Meteoriten auch durch Wechselwirkung (Spallation) mit Kosmischer Strahlung erzeugt werden. Besonders 3He kann deswegen benutzt werden, um das sogenannte Bestrahlungsalter, welches meist dem Zeitraum vom Losschlagen des Meteoriten vom Mutterkörper bis zu seiner Ankunft auf der Erde entspricht, zu bestimmen. Daneben entsteht 4He in Meteoriten durch Zerfall schwerer radioaktiver Elemente. Auch gibt es in Meteoriten weitere Heliumanteile, welche aus der Zeit der Entstehung des Sonnensystems stammen, zum Teil aber auch aus dem Sonnenwind aufgefangen wurden.
Ähnliches gilt auch für Mondgestein, welches von der Oberfläche des Mondes stammt. Da dieses oft sehr lange dem Sonnenwind bzw. der Kosmischen Strahlung ausgesetzt war, ist solches Mondgestein besonders reich an Helium, insbesondere dem Isotop 3He. Sollte es gelingen, Kernfusionsreaktoren für die Deuterium-3He-Fusion zu entwickeln, könnte die Gewinnung von 3He vom Mond wirtschaftlich interessant werden. Der gegenwärtige Energiebedarf Chinas erforderte jährlich 3 Tonnen 3He.[11]
Auf der Erde
4He entsteht im Erdkörper beim radioaktiven Zerfall (Alphazerfall) schwerer Elemente wie Uran oder Thorium, wobei Helium-Kerne als Alphateilchen ausgesandt werden und anschließend Elektronen einfangen. Es kann in verschiedenen uran- und thoriumhaltigen Mineralen wie der Pechblende gefunden werden.
Aus der Entstehungszeit der Erde stammt ein Anteil von 3He im Erdmantel, der weit über dem atmosphärischen Wert liegt, das sogenannte Mantelhelium; das 4He/3He-Verhältnis liegt im oberen Erdmantel, der weitgehend entgast ist und dessen Heliumbestand daher im Wesentlichen durch 4He aus Alpha-Zerfällen wiederaufgefüllt wird, bei etwa 86.000. Wenn das Konvektionssystem des unteren Erdmantels weitgehend von dem des oberen getrennt und der Massenaustausch zwischen beiden entsprechend gering ist, liegt das Verhältnis im unteren, kaum entgasten Mantel zwischen 2500 und 26.000, das heißt, der Anteil von 3He ist noch höher. Von besonderem geodynamischen Interesse ist dies im Hinblick auf die Ursachen von Hotspot-Vulkanismus: während für Basalte von mittelozeanischen Rücken, die durch Schmelzprozesse von Material des oberen Mantels entstehen, 4He/3He = 86.000 typisch ist, weisen Basalte von einigen Hotspots, zum Beispiel ozeanischen Vulkaninseln wie Hawaii und Island, Verhältniswerte auf, die rund ein Drittel oder Viertel von 86.000 betragen, sind also drei- bis viermal 3He-reicher. Dies wird gemeinhin damit erklärt, dass dieser Vulkanismus durch Mantelplumes verursacht wird, deren Ursprung an der Kern-Mantel-Grenze liegt und die daher zumindest teilweise aus Material des unteren Erdmantels bestehen.
Helium kommt – durch den gleichen Mechanismus der Ansammlung – in Erdgas und in geringen Mengen im Erdöl (0,4 %) vor. In unteren Schichten der Erdatmosphäre, besonders der vom Wetter durchmischten Troposphäre beträgt sein Anteil etwa 5,2 ppm. In sehr hoher Schichtung entmischen sich Gase tendenziell entsprechend ihrer unterschiedlichen Dichte etwa entgegen der durchmischenden Wirkung der ungerichteten molekularen Wärmebewegung. Oberhalb 100 km Höhe (Homosphäre) liegt die Atmosphäre zunehmend entmischt vor, Helium wird so in großen Höhen (>400 km, partikelanzahlmässig) das vorherrschende Gas. Auch entweichen Heliumatome in diesen Höhen in den Weltraum - im Gleichgewichtsfall durchschnittlich so viel, wie aus der Erdoberfläche durch Diffusion, Förderung und Vulkanismus nachgeliefert wird.
Künstliche Gewinnung
Erdgas mit einem Heliumanteil bis zu 7 % ist der größte und wirtschaftlich wichtigste Heliumlieferant. Da Helium eine sehr niedrige Siedetemperatur besitzt, ist es durch Herunterkühlen des Erdgases möglich, das Helium von den anderen im Erdgas enthaltenen Stoffen, wie Kohlenwasserstoffen und Stickstoffverbindungen, zu trennen.
Viele Jahre lang gewannen die USA über 90 % des kommerziell benutzbaren Heliums der Welt. Noch 1995 wurden in den USA insgesamt eine Milliarde Kubikmeter Helium gefördert. Der restliche Anteil wurde von Förderungsanlagen in Kanada, Polen, Russland (wobei große Mengen in den unzugänglichen Gebieten Sibiriens liegen) und anderen Ländern geliefert. Nach der Jahrtausendwende kamen Algerien und Katar dazu. Algerien konnte sich rasch zum zweitwichtigsten Heliumlieferanten entwickeln. 2002 stellte Algerien 16 % des Heliums her, das in der Welt vertrieben wurde.
Bei Amarillo in Texas lagerte 2004 etwa das Zehnfache des Weltjahresbedarfs an Helium. Diese ehemals strategische Reserve der amerikanischen Regierung muss jedoch aufgrund des Helium Privatization Act der Clinton-Regierung aus dem Jahr 1996 innerhalb der nächsten Jahre an die Privatwirtschaft verkauft werden.
Mittlerweile wird in den USA angenommen, dass die nationalen Vorräte an Helium innerhalb der kommenden zehn Jahre aufgebraucht sein werden. Dies hätte wegen der Bedeutung von Helium unter anderem bei der Glasfaser- und der Computerchipherstellung erhebliche Auswirkungen auf die entsprechenden Industrien.[12]
Das Isotop 3He ist nur zu etwa 1,4 ppm in natürlichem Helium enthalten und ist daher sehr teuer. Prinzipiell kann es auch in Kernreaktionen gewonnen werden. Tritium und 4He können durch Neutronenbeschuss von Lithium 6Li in einem Kernreaktor gewonnen werden:
Das Tritium zerfällt durch Betazerfall zu 3He.
Auch werden sehr geringe Mengen von Helium 3He in mit Wasser moderierten Reaktoren erbrütet, wenn die im Wasser enthaltenen Wasserstoffatome Neutronen einfangen. Aus dem normalen Wasserstoff bildet sich dadurch Schwerer Wasserstoff (Deuterium) und daraus durch einen weiteren Neutroneneinfang Überschwerer Wasserstoff (Tritium), der durch Betazerfall zu Helium 3He wird. Bei normalem Wasserstoff ist die Einfangrate höher als beim darauf folgenden Schritt des Neutroneneinfanges durch schweren Wasserstoff (deshalb können Kernkraftwerke, die Schweres Wasser als Moderator verwenden, auch mit Natururan betrieben werden):
- Die angegebenen Zeiten sind Halbwertszeiten.
Eigenschaften
Physikalische Eigenschaften
Helium ist nach Wasserstoff das chemische Element mit der geringsten Dichte und besitzt die niedrigsten Schmelz- und Siedepunkte aller Elemente. Daher existiert es nur unter sehr tiefen Temperaturen als Flüssigkeit oder Feststoff. Bei Temperaturen unter 2,17 K liegt 4He in einer suprafluiden Phase vor. Bei Normaldruck wird Helium selbst bei einer Temperatur von 0 K nicht fest. Erst bei einem Druck oberhalb 2,5 MPa (rund 25-facher Atmosphärendruck) geht Helium bei hinreichend tiefen Temperaturen in eine feste Phase über.
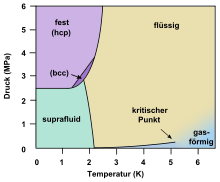 Phasendiagramm von 4He, hcp: hexagonal-dichteste Kugelpackung, bcc: kubisch-raumzentriertes Kristallsystem
Phasendiagramm von 4He, hcp: hexagonal-dichteste Kugelpackung, bcc: kubisch-raumzentriertes Kristallsystem
Im gasförmigen Zustand
 Helium-Gasentladungsröhre
Helium-Gasentladungsröhre
Helium ist ein farbloses, geruchloses und ungiftiges Gas. Unter Standardbedingungen verhält sich Helium nahezu wie ein ideales Gas. Helium ist unter praktisch allen Bedingungen einatomar. Ein Kubikmeter Helium hat bei Standardbedingungen eine Masse von 179 g. Luft hat dagegen die etwa siebenfache Dichte. Helium weist nach Wasserstoff die größte thermische Leitfähigkeit unter allen Gasen auf, und seine spezifische Wärmekapazität ist außergewöhnlich groß. Helium ist ein guter elektrischer Isolator. Die Wasserlöslichkeit von Helium ist geringer als bei jedem anderen Gas. Seine Diffusionsrate durch Festkörper beträgt das Dreifache von Luft und ca. 65 % von Wasserstoff.[13] Helium hat bei Standardbedingungen einen negativen Joule-Thomson-Koeffizienten, das heißt, dieses Gas erwärmt sich bei Ausdehnung. Erst unterhalb der Joule-Thomson-Inversionstemperatur (circa 40 K bei Atmosphärendruck) kühlt es sich bei Expansion ab. Daher muss Helium unter diese Temperatur vorgekühlt werden, ehe es durch Expansionskühlung verflüssigt werden kann. Seine kritischen Daten sind ein Druck von 2,27 bar, eine Temperatur −267,95 °C (5,2 K) und eine Dichte 0,0696 g/cm3.[14]
Im flüssigen Zustand
Helium I
Bei Normaldruck bildet Helium zwischen dem Lambdapunkt bei 2,1768 K und dem Siedepunkt bei 4,21 K eine farblose Flüssigkeit.
Helium II
Flüssiges 4He entwickelt unterhalb seines Lambdapunktes sehr ungewöhnliche Eigenschaften. Helium mit diesen Eigenschaften wird als Helium II bezeichnet. Das Sieden von Helium II ist wegen seiner hohen Wärmeleitfähigkeit nicht mehr möglich. Erhitzen bewirkt stattdessen eine direkte Verdampfung der Flüssigkeit in den gasförmigen Zustand, wenn der „Siedepunkt“ erreicht ist.
Helium II ist ein suprafluider Stoff. So fließt es etwa durch kleinste Öffnungen in Größenordnungen von 10−7 bis 10−8 m und hat keine messbare Viskosität. Jedoch konnte bei Messungen zwischen zwei sich bewegenden Scheiben eine Viskosität ähnlich der von gasförmigem Helium festgestellt werden. Dieses Phänomen wird mit dem Zwei-Fluid-Model (rsp. Zwei-Flüssigkeiten-Modell) nach László Tisza erklärt. Laut dieser Theorie ist Helium II wie ein Gemisch aus 4He-Teilchen im normal-fluiden sowie im suprafluiden Zustand, demnach verhält sich Helium II so, als gäbe es einen Anteil an Heliumatomen mit und einen ohne messbarer Viskosität. Anhand dieser Theorie können viele Phänomene der Tiefentemperaturphysik wie zum Beispiel der „Thermomechanische Effekt“ relativ einfach und klar erklärt werden. Allerdings muss man deutlich darauf hinweisen, dass die zwei Flüssigkeiten weder theoretisch noch praktisch trennbar sind.[15]
 Onnes-Effekt des Helium II
Onnes-Effekt des Helium II
Helium II zeigt wie andere suprafluide Flüssigkeiten den Onnes-Effekt: Wenn eine Oberfläche aus dem Helium hinausragt, bewegt sich das Helium auf dieser Fläche auch gegen die Schwerkraft. Helium II entweicht auf diese Weise aus einem Behälter, der nicht versiegelt ist. Wenn es einen wärmeren Bereich erreicht, verdunstet es. Aufgrund dieses Kriechverhaltens und der Fähigkeit des Heliums II, selbst durch kleinste Öffnungen auszulaufen, ist es sehr schwierig, flüssiges Helium in einem begrenzten Raum zu halten. Es ist ein sehr sorgfältig zu konstruierender Behälter nötig, um Helium II aufzubewahren, ohne dass es entweicht oder verdunstet.
Die Wärmeleitfähigkeit von Helium II ist größer als die jeder anderen bekannten Substanz, was durch den Effekt des zweiten Schalls beschrieben wird. Sie ist eine Million mal höher als die von Helium I und mehrere hundert Mal höher als die des Kupfers. Sie ist so hoch, weil die Wärmeübertragung durch quantenmechanische Effekte bestimmt wird. Die meisten gut wärmeleitenden Materialien besitzen ein Valenzband freier Elektronen, die die Wärme gut leiten. Helium II hat kein solches, sondern leitet den Wärmepuls mit einer Geschwindigkeit von 20 m/s bei 1,8 K. Dieser Vorgang kann durch eine Wellengleichung beschrieben werden.
1971 gelang David M. Lee, Douglas D. Osheroff und Robert C. Richardson, das Helium-Isotop 3He ebenfalls in einen suprafluiden Zustand zu versetzen, indem sie das Isotop unter die Temperatur von 2,6 Millikelvin abkühlten. Dabei geht man davon aus, dass zwei Atome 3He ein Paar bilden, ähnlich einem Cooper-Paar. Dieses Paar besitzt ein magnetisches Moment und ein Drehmoment. Die drei Wissenschaftler erhielten für diese Entdeckung 1996 den Nobelpreis für Physik.
In festem Zustand
Helium kann als einziger Stoff unter Normaldruck nicht verfestigt werden. Dies gelingt nur unter erhöhtem Druck (etwa 2,5 MPa) und bei sehr niedriger Temperatur (weniger als 1,5 K). Der beim Phasenübergang entstehende, fast vollkommen durchsichtige Feststoff ist sehr stark komprimierbar. Im Labor kann dessen Volumen um bis zu 30 % verringert werden; Helium ist mehr als 50-mal leichter komprimierbar als Wasser. Im festen Zustand bildet es kristalline Strukturen aus. Festes und flüssiges Helium sind optisch kaum voneinander zu unterscheiden, da ihre Brechungsindizes fast gleich sind.
In einem anderen Fall kann bei Unterschreiten von etwa 200 mK und gleichzeitigem Zentrifugieren ein Zustand erreicht werden, den man suprasolide oder auch suprafest nennt.[16] Hierbei stoppt ein Teil des Feststoffes die eigene Rotation und durchdringt die restlichen Teile der Materie. Zu diesem teilweise umstrittenen Effekt gibt es noch keine bekannten Thesen oder Theorien.
Molekulare Eigenschaften
Die zwei Elektronen des Heliumatoms bilden die abgeschlossene, kugelsymmetrische Elektronenschale des 1s-Orbitals. Diese Elektronenkonfiguration ist energetisch äußerst stabil, es gibt kein anderes Element mit einer höheren Ionisierungsenergie und einer geringeren Elektronenaffinität. Helium ist trotz seiner größeren Elektronenzahl kleiner als Wasserstoff und damit das kleinste Atom überhaupt.
Abhängig von der Spinorientierung der zwei Elektronen des Heliumatoms spricht man vom Parahelium im Falle von zwei einander entgegengerichteten Spins (S = 0) und von Orthohelium bei zwei parallelen Spins (S = 1). Beim Orthohelium befindet sich eines der Elektronen nicht im 1s-Orbital, da dies das Pauli-Verbot verletzen würde.
Die Benennung dieser Zustände geht auf einen früheren Irrtum zurück: Da der elektromagnetische Übergang zwischen dem Grundzustand des Orthoheliums und dem Grundzustand des Paraheliums (also dem Helium-Grundzustand) verboten ist, erscheinen die beiden „Varianten“ des Heliums spektroskopisch wie zwei unterschiedliche Atome. Dies führte dazu, dass Carl Runge und Louis Paschen postulierten, Helium bestehe aus zwei getrennten Gasen, Orthohelium („richtiges Helium“) und Parahelium (für das sie den Namen Asterium vorschlugen).
Neben der Elektronenkonfiguration des Orthoheliums können die Elektronen – zum Beispiel durch Beschuss mit Elektronen – weitere angeregte Zustände einnehmen. Diese langlebigen angeregten Zustände werden als metastabile Energieniveaus bezeichnet.
Chemische Eigenschaften
Helium ist ein Edelgas. Die einzige Elektronenschale ist mit zwei Elektronen voll besetzt. Beide Elektronen sind durch die räumlich Nähe zum Atomkern sehr stark an diesen gebunden. Nicht zuletzt deswegen ist Helium selbst im Vergleich zu anderen Edelgasen ausgesprochen reaktionsträge. Das zeigt sich auch an den hohen Ionisierungsenergien des Heliumatoms.
Helium-Dimer
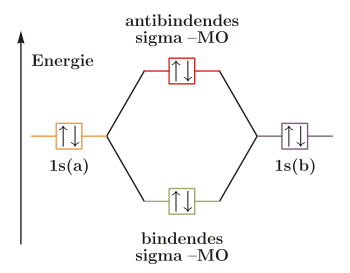
Wie anhand des Molekülorbital-Schemas ersichtlich wird, bilden Helium-Atome untereinander keine chemische Bindung. Beim Helium ist das 1s-Orbital mit einem Elektronenpaar besetzt. Bei der Kombination zweier dieser voll besetzten Atomorbitale (a) und (b) ist sowohl das bindende als auch das antibindende Molekülorbital mit je einem Elektronenpaar besetzt. Bei den sich (hypothetisch) ausbildenden Bindungsorbitalen wird der energetisch günstigere, sog. bindende Zustand durch den ebenfalls besetzten, aber energetisch ungünstigeren Antibindenden kompensiert. Das Gesamtsystem liegt energetisch nicht niedriger und es kommt keine Bindung zustande.
Besetzung der Orbitale eines hypothetischen He2-Moleküls. Aufgrund der für alle Atome und Moleküle wirksamen Van-der-Waals-Wechselwirkung existiert jedoch auch bei Helium ein Dimer, allerdings mit einer äußerst kleinen Bindungsenergie von circa 1,1 mK (= 9,5 · 10−26 J)[17] und einem entsprechend großen Bindungsabstand von circa 52 Å.[18]
Ionische Bindungen
Unter extremen Bedingungen ist es möglich, eine quasichemische Verbindung von Helium mit einem Proton (HeH+) zu erzeugen. Diese Verbindung ist bei Normalbedingungen sehr instabil und kann nicht in Form eines Salzes wie HeH+X− isoliert werden.

- In einem Gemisch aus Helium und Wasserstoff bildet sich während einer elektrischen Entladung ein Heliumhydrid-Ion
Eine entsprechende Reaktion kann zwischen zwei Helium-Atomen ablaufen, wenn die zur Ionisierung notwendige Energie zugeführt wird.
Diese Verbindungen können aber nicht als wirkliche chemische Verbindungen bezeichnet werden, sondern eher als ionische Agglomerationen, die unter Ausnahmebedingungen kurz entstehen und sofort wieder zerfallen.
Isotope
Verschiedene Eigenschaften der Heliumisotope 3He 4He Ruheenergie in MeV 2809 3728 Dichte in kg/m3 0,134 0,178 Kritische Temperatur in K 3,32 5,20 Lambdapunkt in K 0,0025 2,1768 Schmelzdruck bei T = 0 K in MPa 3,439 2,536 Siedepunkt in K 3,19 4,21 Von den acht bekannten Isotopen des Heliums sind lediglich 3He und 4He stabil. In der Erdatmosphäre existiert pro Million 4He-Atome nur ein 3He-Atom. Jedoch variiert die Proportion der beiden Isotope je nach dem Herkunftsort der untersuchten Heliumprobe. Im interstellaren Medium sind 3He-Atome hundert Mal häufiger. In Gesteinen der Erdkruste und des Erdmantels liegt die Proportion ebenfalls weit über dem atmosphärischen Wert und variiert je nach Herkunft um den Faktor 10. Diese Variationen werden in der Geologie benutzt, um die Herkunft des Gesteines zu klären (siehe auch Natürliches Vorkommen).
3He und 4He weisen aufgrund der unterschiedlichen Symmetrieeigenschaften (3He-Atome sind Fermionen, 4He-Atome sind Bosonen) einige unterschiedliche physikalische Eigenschaften auf, die sich insbesondere bei tiefen Temperaturen zeigen. So trennen sich gleiche Anteile von flüssigem 3He und 4He unter 0,8 Kelvin aufgrund ihrer unterschiedlichen Quanteneigenschaften in zwei unmischbare Flüssigkeiten, ähnlich Öl und Wasser. Dabei schwimmt eine Phase aus reinem 3He auf einer Phase, die hauptsächlich aus 4He besteht. Weiterhin unterscheiden sich die zwei Isotope deutlich in ihren suprafluiden Phasen (siehe Abschnitt „Helium II“).
Kernfusion
In Ankündigungen neuer Raumfahrt-Missionen der USA, Russlands und Chinas, weiterhin auch Europas, Indiens und Japans zum Mond wurden mehrfach die dortigen anteilig größeren Vorkommen von 3He als lohnende Quelle genannt, um Kernfusionsreaktoren auf Basis dieses Isotops auf der Erde zu ermöglichen. Im Gegensatz zur Deuterium-Tritium-Fusionsreaktion liefert die Deuterium-3He-Reaktion bei ähnlich großem Energiegewinn keine freien Neutronen, sondern Protonen. Dies würde die Radioaktivitätsprobleme der Fusionsenergiegewinnung dramatisch verringern. Andererseits ist die Herbeiführung dieser Reaktion wegen der nötigen viel höheren Plasmatemperatur eine noch ungelöste technische Herausforderung.[19]
Hypothetisches Diproton
Ein besonderes, fiktives Isotop des Heliums ist 2He, dessen Kern, das Diproton, im Falle seiner Existenz lediglich aus zwei Protonen bestünde. Für ein System aus zwei Protonen gibt es jedoch keinen gebundenen Zustand, da sich diese wegen des Pauli-Prinzips – im Gegensatz zum Proton und Neutron beim Deuteron – nur in einem Singulett-Zustand mit antiparallelen Spins befinden dürfen. Auf Grund der starken Spinabhängigkeit der Nukleon-Nukleon-Wechselwirkung ist dieser aber energetisch angehoben und daher nicht gebunden.
Verwendung
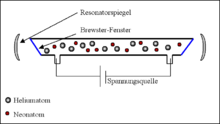 Schematische Darstellung eines Helium-Neon-Lasers
Schematische Darstellung eines Helium-Neon-Lasers
Im Handel angebotenes, komprimiertes Helium wird aus Erdgas gewonnen. Es wird vielseitig verwendet:
- Helium-Sauerstoff-Gemisch (80:20) dient in der Intensivmedizin als Atemgas. Das Gemisch strömt mit geringerem Widerstand durch Verengungen und lässt sich daher leichter atmen.
- Beim kommerziellen Tauchen werden verschiedene Gemische mit Helium wie Trimix (bestehend aus Sauerstoff, Stickstoff und Helium), Hydreliox (Wasserstoff, Helium und Sauerstoff) und Heliox (Helium und Sauerstoff) als Atemgas verwendet. Nachteilig wirkt sich hier die hohe Wärmeleitfähigkeit des Heliums aus, was zum Auskühlen der Lunge des Tauchers führt.[20]
- In der Lebensmittelindustrie wird es als Treibgas oder Packgas verwendet und ist als Lebensmittelzusatzstoff E 939 zugelassen.[21]
- Helium ist ein ideales Traggas für Ballons und Luftschiffe; es hat eine sehr geringe Dichte, brennt nicht und kann als Luft-Helium-Gemisch nicht explodieren. Helium hat Wasserstoff weitgehend verdrängt, auch wenn seine Dichte höher und damit seine Tragkraft etwas niedriger als die des Wasserstoffs ist. Die technische Anforderung an die Hülle ist aufgrund der hohen Diffusionsrate höher als bei anderen Gasen.
- In der Schweißtechnik wird Helium in Reinform oder als Zumischung als Inertgas eingesetzt, um die Schweißstelle vor Sauerstoff zu schützen. Zudem lässt sich bei Einsatz von Helium die Einbrenntiefe und die Schweißgeschwindigkeit steigern sowie die Bildung von Spritzern verringern, was insbesondere bei Roboterschweißungen und bei der Verarbeitung von Aluminium und rostfreien Stählen zum Einsatz kommt.
- Technisch wird verflüssigtes Helium (die Isotope 4He und 3He) als Kühlmittel zum Erreichen sehr tiefer Temperaturen eingesetzt (siehe dazu: Kryostat). Mit 4He lassen sich durch Verdampfungskühlen Temperaturen bis etwa 1 K erreichen, mit dem Isotop 3He bis etwa 240 mK.[22] Mit dem Verfahren der 3He-4He-Mischungskühlung werden bis etwa 5 mK erreicht,[22] wobei dieses Verfahren deutlich kostengünstiger als eine reine 3He-Kühlung ist. Beim Einsatz von supraleitenden Magneten dient Helium als Kühlmittel, um damit den Supraleiter unter seiner Sprungtemperatur zu halten. Praktische Anwendungen sind hier besonders die Kernspintomographie (MRT) für medizinische Anwendungen sowie die Magnetresonanzspektroskopie (NMR) und der Betrieb von Teilchenbescheunigern in der Forschung. In der Raumfahrt kühlt flüssiges Helium Infrarotteleskope und die hochempfindlichen Infrarotkameras in Weltraumteleskopen, die nur nahe dem Absoluten Nullpunkt ohne zu stark störende Eigenwärme arbeiten können. Beispiele sind: IRAS, ISO, das Spitzer- und das Herschel-Weltraumteleskop. Ein weiteres Anwendungsgebiet ist die Herstellung von optischen Glasfasern in heliumgekühlten Falltürmen.
- Komprimiertes Heliumgas kann als Kühlmittel eingesetzt werden, insbesondere dort, wo ein chemisch wie auch kernphysikalisch besonders inertes Kühlmittel benötigt wird. Kernphysikalisch inert ist allerdings nur die Hauptkomponente He-4, während He-3 durch thermische Neutronen leicht in radioaktives Tritium überführt wird. Als Beispiel sei der Thorium-Hochtemperaturreaktor (kurz: THTR) genannt, wo das Helium bei sehr hohen Temperaturen verwendet wurde. Zu beachten ist, dass Helium zwar eine hohe spezifische, aber eine niedrige molare Wärmekapazität besitzt. Dies ist insbesondere bei geschlossenen Apparaturen problematisch, da es im Falle eines Temperaturanstiegs (zum Beispiel bei Stromausfall) schnell zu einer massiven Druckerhöhung kommt.
 Helium-Entladungsröhre
Helium-Entladungsröhre
- Die Suche nach Undichtigkeiten in Druckgasarmaturen wird durch eine Befüllung mit Helium erleichtert. Außen an der Druckarmatur wird ein Lecksuchspray aufgebracht. Helium dringt besonders leicht durch Leckstellen und erzeugt deutlichere Schaumblasen als das Betriebsgas.
- Bei Vakuumanlagen wird Helium als diffusionsfreudigstes Lecksuchgas eingesetzt, indem die Vakuumapparatur mit einer Pumpe evakuiert wird und ein Massenspektrometer hinter die Pumpe gehängt wird. Wird nun die Apparatur – außen, nur lokal um Leckstellen zu finden – mit Helium angeblasen, kann mit Hilfe des Massenspektrometers ein eventueller Heliumeintritt in die Apparatur detektiert und die Leckrate gemessen werden. Diese rasche und empfindliche Lecksuchmethode wird auch an Chemieanlagen und bei der Fertigung von Wärmetauschern für Klimaanlagen oder Benzintanks für Autos benutzt.
- Helium wird in Gasform in der Raketentechnik eingesetzt, um bei pumpgeförderten Flüssigtreibstoffraketen den verbrauchten Treibstoff zu ersetzen, damit die dünnwandigen Treibstofftanks der Raketen nicht implodieren, wenn der Treibstoff von den Treibstoffpumpen der Triebwerke aus den Tanks gesaugt wird. Bei druckgasgeförderten Flüssigtreibstoffraketen drückt Helium den Treibstoff in die Triebwerke. Helium wird hier wegen seines niedrigen Gewichtes und seiner niedrigen Siedetemperatur benutzt. Da es als Edelgas nicht mit dem Treibstoff reagieren kann, stellen auch aggressive hypergolische Treibstoffe kein Problem dar.
- Helium wird in zwei Lasertypen eingesetzt: Dem Helium-Neon-Laser und dem Helium-Cadmium-Laser.
- Reinsthelium dient zudem als Trägergas in der Gaschromatographie (Analytik).
- In Gasentladungsröhren leuchtet Helium gelblich/weiß.
- Aufgrund seiner thermodynamischen Eigenschaften ist Helium das beste Arbeitsmedium für Stirlingmotoren.
- Hyperpolarisiertes 3He wird in der Diagnostik versuchsweise als Kontrastmittel für kernspintomografische Aufnahmen der Lunge verwendet.
- in Schlagschraubern beim Radwechsel in der Formel 1, damit konnten diese um 30% schneller betrieben werden.[23]
Gefahren
Obwohl Helium an sich ungiftig ist und unter Umweltbedingungen keine chemischen Verbindungen eingeht, wird davon abgeraten, das Gas einzuatmen oder in geschlossene Räume ausströmen zu lassen, da Helium den Sauerstoff verdrängt und somit zu Sauerstoffmangel führen kann. Dies kann zu dauerhaften Gesundheitsschäden bis hin zum Tod führen. Symptome können Orientierungsschwierigkeiten und Bewusstseinsverlust sein. Das Gefährliche daran ist, dass das Opfer die Erstickung kaum bis gar nicht bemerkt, bis es zu spät ist. Beim Verwenden von Helium-Flüssiggas ist die Verwendung von Schutzkleidung notwendig, um Erfrierungen zu vermeiden. Heliumdruckgasbehälter – meist nahtlose Stahlzylinder für 200 bar Hochdruck oder aber geschweißte (oft: Einweg-)Flaschen – stehen unter hohem Druck und dürfen daher nicht erhitzt oder mit Feuer in Verbindung gebracht werden, weil sie explodieren, wenn der Innendruck zu stark wird.
Sonstiges
Nach dem Einatmen von Helium ändert sich die eigene Stimme dramatisch (zu einem „Micky-Maus-Piepsen“). Diese Änderung ist auf zwei überlagerte Effekte zurückzuführen:
- Zum einen schwingen die Stimmlippen durch die deutlich geringere Viskosität von Helium gegenüber Luft bei gleichem Atemdruck und gleicher Muskelspannung schneller, was eine höhere Grundfrequenz der Stimme zur Folge hat.
- Zusätzlich hängt die Klangfarbe einer Stimme von der Lage der Formanten im Mundraum ab, die durch Faktoren wie Zungen- und Lippenstellung beeinflusst werden können. (Formanten sind diejenigen Frequenzbereiche, die am stärksten durch Resonanzwirkung verstärkt werden.) Diese Formanten hängen auch von der Schallgeschwindigkeit im entsprechenden Medium ab (cLuft = 350 m/s, cHelium = 1030 m/s). Beträgt zum Beispiel die Lage der ersten drei Formanten in Luft 220, 2270 und 3270 Hz, so ändert sich dies in Helium zu 320, 3900 und 5500 Hz. Dadurch ergibt sich ein anderes Stimmbild, und die Stimme erscheint insgesamt höher, selbst wenn die Höhe des Stimmtones selbst durch das Edelgas unverändert bliebe.
Literatur
- P. Häussinger, R. Glatthaar, W. Rhode, H. Kick, C. Benkmann, J. Weber, H.-J. Wunschel, V. Stenke, E. Leicht, H. Stenger: Noble Gases. In: Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim 2006 (doi:10.1002/14356007.a17_485).
- Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage, de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 417–429.
- F. A. Cotton, G. Wilkinson, C. A. Murillo, M. Bochmann: Advanced Inorganic Chemistry. Kap. 18. D. Wiley, New York 61999, ISBN 0-471-19957-5. S. 974.
- C. E. Housecroft, A. G. Sharpe: Inorganic Chemistry. Kapitel 22.8a. Pewson, Prentice Hall 2005, ISBN 0-13-039913-2. S. 666.
- Ekkehard Fluck, Klaus G. Heumann: Periodensystem der Elemente, Tafel. Wiley-VCH, Weinheim 2002, ISBN 3-527-30716-8.
- R. B. King (Hrsg.): Encyclopedia of Inorganic Chemistry. Bd 8. D. Wiley, New York 1994, ISBN 0-471-93620-0. S. 4094.
Weblinks
 Wiktionary: Helium – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Wiktionary: Helium – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen Commons: Helium – Album mit Bildern und/oder Videos und Audiodateien
Commons: Helium – Album mit Bildern und/oder Videos und Audiodateien Wikibooks: Wikijunior Die Elemente/ Elemente/ Helium – Lern- und Lehrmaterialien
Wikibooks: Wikijunior Die Elemente/ Elemente/ Helium – Lern- und Lehrmaterialien- Jahresbericht des Bureau of Land Management (englisch, PDF, 76 KiB)
- Fribourg group for Atomic Physics (englisch)
- Low Temperature Laboratoy Helsinki (englisch)
Einzelnachweise
- ↑ Harry H. Binder: Lexikon der chemischen Elemente, S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3.
- ↑ Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Helium) entnommen.
- ↑ Michael E. Wieser und Tyler B. Coplen: Atomic weights of the elements (IUPAC Technical Report) In: Pure and Applied Chemistry Vol. 83, No. 2, 2011, S. 359–396.
- ↑ a b c Eintrag zu Helium in der GESTIS-Stoffdatenbank des IFA, abgerufen am 12. Juli 2009 (JavaScript erforderlich).
- ↑ R. E. Glick: On the Diamagnetic Susceptibility of Gases. In: J. Phys. Chem.. 1961, 65, 9, S. 1552–1555, doi:10.1021/j100905a020.
- ↑ T. L. Meek: Electronegativities of the Noble Gases. In: Journal of chemical education. 72, 1, 1995, S. 17–18
- ↑ L. C. Allen, J. E. Huheey: The definition of electronegativity and the chemistry of the noble gases. In: Journal of Inorganic and Nuclear Chemistry. 42, 1980, S. 1523–1524, doi:10.1016/0022-1902(80)80132-1.
- ↑ Stoffdatenblatt Helium (verdichtet)
- ↑ Spektrum der Sonne und die Anteile von Wasserstoff und Helium
- ↑ Cleveit bei mindat.org (engl.)
- ↑ Rainer Kayser: Langer Marsch China will zum Mond. In: Die Rheinpfalz am Sonntag. 8. Juli 2007, S. 20.
- ↑ Depletion of helium supply causing prices to skyrocket. Herald Review, 5. Januar 2008.
- ↑ The Encyclopedia of Chemical Elements, S. 261.
- ↑ Römpps Chemielexikon, 8. Auflage, 1988.
- ↑ Enns, Hunklinger (2000): Tiefentemperaturphysik, Seite 13 ff.
- ↑ Angelika Leute: Atomphysik: Suprafestes Helium entdeckt. In: Physik in unserer Zeit. 35, Nr. 6, WILEY-VCH, Weinheim 2004, ISSN 1521-3943, S. 261, doi:10.1002/piuz.200490097.
- ↑ Zur Umrechnung von in Kelvin angegebenen Energieeinheiten in Joule siehe Kelvin#Temperatur und Energie
- ↑ R. E. Grisenti, W. Schöllkopf, J. P. Toennies, G. C. Hegerfeldt, T. Köhler, M. Stoll: Determination of the Bond Length and Binding Energy of the Helium Dimer by Diffraction from a Transmission Grating. Phys. Rev. Lett. 85, 11, 2000, S. 2284–2287 (online).
- ↑ 'Energie vom Mond', heise.de/tr, 31. August 2007.
- ↑ Technisches Tauchen in Unterwasser, Ausgabe 05/2010 vom 13. April 2010.
- ↑ ZZulV: Anlage 3 (zu § 5 Abs. 1 und § 7) Allgemein zugelassene Zusatzstoffe
- ↑ a b Jens Wiebe: Aufbau einer 300-mK-Ultrahochvakuum-Rastertunnelmikroskopie-Anlage mit 14-T-Magnet und Untersuchung eines stark ungeordneten zweidimensionalen Elektronensystems. Inauguraldissertation zur Erlangung des Doktorgrads des Fachbereichs Physik der Universität Hamburg. Vorgelegt von aus Hamburg, 2003. S. 17 (S. 23).
- ↑ Helium-Verbot in Schlagschraubern geplant, Artikel auf www.motorsport-total.com, abgerufen am 10. November 2011.
Alkalimetalle Erdalkalimetalle Lanthanoide Actinoide Übergangsmetalle Metalle Halbmetalle Nichtmetalle Halogene Edelgase 
Dieser Artikel wurde am 14. November 2005 in dieser Version in die Liste der exzellenten Artikel aufgenommen. Kategorien:- ATC-V03
- Edelgas
- Periode-1-Element
- Chemisches Element
- Wikipedia:Exzellent
- Lebensmittelzusatzstoff
Wikimedia Foundation.





![\mathrm{{}^{1}_{1}H\ \xrightarrow {(n,\gamma)} \ ^{2}_{1}H\ \xrightarrow {(n,\gamma)} \ ^{3}_{1}H\ \xrightarrow [12{,}33 \ a]{\beta^-} \ ^{3}_{2}He}](3/5232bcaf3bd78c14f5482518b5abe81f.png)