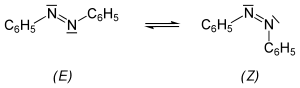- Azobenzol
-
Strukturformel 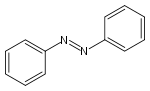
E-Azobenzol Allgemeines Name Azobenzol Andere Namen Di(phenyl)diazen (IUPAC)
Summenformel C12H10N2 CAS-Nummer 103-33-3 PubChem 2272 Kurzbeschreibung orangerote Blättchen[1]
Eigenschaften Molare Masse 182,22 g·mol−1 Schmelzpunkt Siedepunkt (E)-Azobenzol: 293 °C (unzersetzt)[1]
Löslichkeit kaum löslich in Wasser, aber leicht in organischen Lösungsmitteln[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [2] 


Gefahr
H- und P-Sätze H: 350-341-332-302-373-410 EUH: keine EUH-Sätze P: 201-273-281-308+313-501 [3] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Giftig Umwelt-
gefährlich(T) (N) R- und S-Sätze R: 45-20/22-48/22-68-50/53 S: 53-45-60-61 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Azobenzol ist die einfachste aromatische Azoverbindung und somit die Stammsubstanz der Azofarbstoffe. Es ist eine chemische Substanz, die aus zwei Phenylgruppen, die durch eine Azobrücke –N=N– miteinander verbunden sind, besteht.
Inhaltsverzeichnis
Geschichte
Bereits sechs Jahre nach dem allgemein anerkannten Beginn der „organischen Synthese“ (F. Wöhler, Harnstoff aus Ammoniumcyanat) und 22 Jahre vor W. H. Perkin (Mauvein) berichtet E. Mitscherlich[4][5] über eine rote Verbindung, die er durch Destillation von Nitrobenzol mit Kalilauge erhielt. Er nannte sie Azobenzol.
Lange Zeit wusste man nichts über die Konstitution dieser Verbindung. Mitscherlich selbst schlug als Summenformel C12 H5 N vor.[6] Aufgrund von Dampfdichtemessungen kamen andere Autoren zur Summenformel C24 H10 N2.[7][8] Erst im Jahre 1860 wurde die richtige Summenformel postuliert.[9] F. A. Kekulé machte 1866 schließlich den ersten korrekten Strukturvorschlag.[10]
Ungeklärt blieb die Frage der Konfiguration der N=N-Doppelbindung. Für analoge Verbindungen (Diazohydroxide) schlug A. Hantzsch 1921 eine Isomerie vor, damals „syn-/anti-Isomerie“ genannt.[11] (Die IUPAC empfiehlt heute die Verwendung der (E)/(Z)-Nomenklatur, siehe unten.)
Isomere
1937 fand S. Hartley durch Belichten von Azobenzol eine zweite, gelbe Modifikation (siehe unten).[12] Das gelbe Isomer konnte er chromatograpisch abtrennen. Die genaue Konfiguration der beiden Isomere wurde 1939 von H. P. Robertson et al. durch eine Röntgenstrukturanalyse bewiesen.[13] Azobenzol existiert demnach in Form von zwei Isomeren (siehe Cis-trans-Isomerie), die sich in Farbe, Löslichkeit, im chromatographischen Verhalten usw. unterscheiden.[14]
Bei der Bestrahlung einer Lösung von (E)-Azobenzol mit UV-Licht geht dieses in einer Gleichgewichtsreaktion teilweise in die (Z)-Form über, in Abhängigkeit vom Lösungsmittel entstehen dabei 15–40 % (Z)-Azobenzol.
Das stabilere, normalerweise vorliegende (E)-Azobenzol hat kein Dipolmoment (µ = 0 D), im Gegensatz zum metastabilen (Z)-Azobenzol (µ = 3 D).[15]
Darstellung und Gewinnung
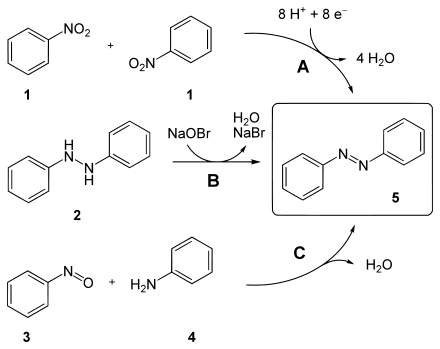
Azobenzol (5) lässt sich auf folgende Arten herstellen (vergleiche auch unteres Bild):
- durch Reduktion von Nitrobenzol (1) mit Natriumamalgam oder Lithiumaluminiumhydrid (Weg A)
- durch Oxidation von Hydrazobenzol (2) mit Natriumhypobromitlösung (Weg B)
- durch Kondensation von Nitrosobenzol (3) mit Anilin (4) in essigsaurer Lösung (besonders zur Herstellung von asymmetrischen Derivaten) (Weg C)
Verwendung
(E)-Azobenzol findet als Testsubstanz für das Kofler-Heiztischmikroskop bzw. als Eichsubstanz für die Kofler-Heizbank Verwendung. [16]
Einzelnachweise
- ↑ a b c d e Hans Beyer, Wolfgang Walter: Lehrbuch der Organischen Chemie. 20. Aufl., Hirzel, Stuttgart, 1984. S. 529.
- ↑ a b Eintrag zu CAS-Nr. 103-33-3 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ Eintrag zu CAS-Nr. 103-33-3 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. März 2011 (JavaScript erforderlich)
- ↑ E. Mitscherlich: Annalen der Physik und Chemie XXXII (1834). S. 224.
- ↑ E. Mitscherlich: Annalen der Chemie und Pharmacie XII. S. 311.
- ↑ Otto Linné Erdmann: Journal für praktische Chemie. Bd. 82, Verlag von Johann Ambrosius Barth, 1861, S. 444 (Online lesen in der Google Buchsuche).
- ↑ P. Hofmann: Annalen der Chemie und Pharmacie CXV. S. 362.
- ↑ Peter Griefs: Zur Kenntnifs des s. g. Azobenzols und verwandter Verbindungen. In: Justus Liebig (Freiherr von) (Hrsg.): Annalen der Chemie und Pharmacie. Bände 131–132, C.F. Winter'sche, 1864 (Online lesen in der Google Buchsuche).
- ↑ P. Hofmann: Annalen der Chemie und Pharmacie (1860). S. 324.
- ↑ Dr. Carl Glaser: Ueber eine neue Bildungsweise des Azobenzols. In: Zeitschrift für Chemie. 1866 (Online lesen in der Google Buchsuche).
- ↑ A. Hantzsch, G. Reddelien: Die Diazoverbindungen. Springer, Berlin, 1921.
- ↑ G. S. Hartley: Nature 140 (1937). S. 281.
- ↑ H. P. Robertson et al.: J. Chem. Soc. (1939). S. 398.
- ↑ A. H. Cook: J. Chem. Soc. (1938). S. 876.
- ↑ R. J. W. Le Fevre, G. S. Hartley: J. Chem. Soc. (1939). S. 531.
- ↑ M. Kuhnert-Brandstätter: Thermomicroscopy in the Analysis of Pharmaceuticals, Pergamon Press, Oxford (1971).
Literatur
- H. Zollinger: Chemie der Azofarbstoffe. (Chemische Reihe, Bd. 13). Birkhäuser-Verlag, Basel, 1958. ASIN B0000BPY7I
Kategorien:- Krebserzeugender Stoff
- Gesundheitsschädlicher Stoff
- Umweltgefährlicher Stoff
- Azobenzol
Wikimedia Foundation.