- Triphenylmethan
-
Strukturformel 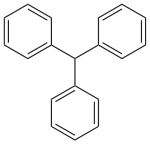
Allgemeines Name Triphenylmethan Andere Namen - Tritan
- Triarylmethan
Summenformel C19H16 CAS-Nummer 519-73-3 Kurzbeschreibung kristalliner, farbloser Feststoff[1]
Eigenschaften Molare Masse 244,34 g·mol−1 Aggregatzustand fest
Dichte 1,01 g·cm−3[2]
Schmelzpunkt Siedepunkt 359 °C[2]
Löslichkeit - unlöslich in Wasser[3]
- löslich in heißem Ethanol, Diethylether und Chloroform[3]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] keine GHS-Piktogramme H- und P-Sätze H: keine H-Sätze EUH: keine EUH-Sätze P: keine P-Sätze EU-Gefahrstoffkennzeichnung [2] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: 22-24/25 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Triphenylmethan, auch Tritan (davon abgeleitet Tritylgruppe für die Triphenylmethylgruppe) genannt, ist eine organische Verbindung, in der drei Phenylringe um ein zentrales Kohlenstoffatom gruppiert sind. Triphenylmethan ist die Muttersubstanz der Triphenylmethanfarbstoffe. Es ist farblos, in den Farbstoffen liegt jedoch ein delokalisiertes Elektronensystem des entsprechenden Kations oder Anions vor, das durch den mesomeren Effekt der Substituenten stabilisiert wird. Man spricht dann von einem konjugierten π-Elektronensystem.
Da sich die Wasserstoff-Atome der Phenylreste räumlich stören, ist eine planare Anordnung der Ringe nicht möglich, sie liegen daher propellerartig verdreht zueinander vor.
Triphenylmethan lässt sich leicht zu Triphenylmethanol oxidieren. Außerdem wirkt Triphenylmethan als sehr schwache Säure, z. B. kann es mit starken Basen (oder mit Alkalimetallen unter Abspaltung von Wasserstoff) zum Triphenylmethanid-Anion reagieren, das ebenfalls mesomeriestabilisiert ist.
Inhaltsverzeichnis
Synthese
Triphenylmethan kann per Friedel-Crafts-Alkylierung aus Benzol und Trichlormethan (Chloroform) oder in wesentlich besserer Ausbeute aus Benzol und Benzalchlorid synthetisiert werden. Es handelt sich hierbei um eine elektrophile aromatische Substitution. Für beide Reaktionen wird die Lewis-Säure Aluminiumtrichlorid (AlCl3) als Katalysator benötigt. Als Nebenprodukt entsteht Chlorwasserstoff.
Verwendung
Triphenylmethan bildet den Grundkörper für die Gruppe der Triphenylmethanfarbstoffe (z. B. Indikatoren, Textil- und Lebensmittelfarbstoffe). Zu diesen gehören u. a. Fuchsin, Kristallviolett, Phenolphthalein, Fluorescein, Eosin, Bromphenolblau usw.
Siehe auch
Einzelnachweise
Wikimedia Foundation.
