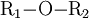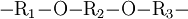- Äther (Chemie)
-
Als Ether, per IUPAC: Alkoxyalkane, nicht fachsprachlich Äther, werden organische Verbindungen mit einer Sauerstoffbrücke zwischen zwei Alkyl- oder Aryl-Resten als funktioneller Gruppe bezeichnet. Der in der Umgangssprache bekannte „Ether“ bezeichnet Diethylether (C2H5-O-C2H5), einen der einfachsten Ether.
Inhaltsverzeichnis
Natürliches Vorkommen
Ether sind in der Natur weit verbreitete Verbindungen. So liegen die meisten Monosaccharide in einer cyclischen Halbacetal-Form vor, die faktisch intramolekulare Ether sind. Die glycosidische Bindung der Polysaccharide ist eine Sauerstoffbrücke zwischen zwei Kohlenstoffatomen. Auch viele andere Naturstoffe, wie z.B. die Aromastoffe Anethol, 1,8-Cineol, Eugenol und Vanillin, sind Ether.
Struktur
Allgemein kann ein Ether als
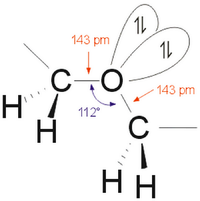
dargestellt werden. R1 und R2 sind hier Alkyl- oder Aryl-Reste, die im Fall eines cyclischen Ethers miteinander verbunden sind. Es sind auch Alkyl-Aryl-Ether möglich (siehe Anisol und Vanillin). Die Bindungsverhältnisse in Ethern ähneln denen in Alkoholen und im Wasser, das als Grundkörper dieser beiden Verbindungsklassen aufgefasst werden kann. Kohlenstoff- und Sauerstoff-Atome sind jeweils sp3 hybridisiert. Dies führt zu einer tetraedrischen Anordnung der Atomorbitale um alle beteiligten Atome. Der Bindungswinkel des Sauerstoffs ist aufgrund der gegenüber Wasserstoff (104,5° im H2O) voluminöseren Alkylsubstituenten mit 112° erweitert. Die C-O-Bindungen sind mit ca. 143 pm so lang wie in Alkoholen.
Nomenklatur
Gemäß den IUPAC-Richtlinien werden Ether als Alkoxy-Alkane bezeichnet: R1-O-R2, wobei die Gruppe O-R2 als Alkoxy-Substituent einer Alkan-Kette R1 behandelt wird. Der niederrangigere Substituent der Kette ist hierbei der Alkoxy-Rest (-O-R2), der höherrangigere bildet den Stamm des Stoffnamens. Ebenfalls von der IUPAC zugelassene Namen werden durch Nennung der beiden Alkylreste und der Endung ether gebildet und sind besonders für kleine, aliphatische Ether gebräuchlich. Bei symmetrischen Ethern ist dann die Bezeichnung sehr einfach durch Vorstellen eines Di möglich (z.B.: Diethylether (Ethoxyethan) oder Dimethylether (Methoxymethan)). Cyclische Ether sind fast sämtlich nur unter ihrem Trivialnamen bekannt.
Geradkettige und verzweigte Ether
Entsprechend verläuft die Benennung der Alkoxy-Alkane. Beispiele:
- Die Verbindung H3C-O-CH3 setzt sich zusammen aus einem H3C-O-Substituenten und dem Methyl-Rest (CH3) als Stamm, wobei hier allerdings beide Reste gleichwertig sind. Entsprechend heißt die Verbindung Methoxymethan oder Dimethylether.
- Die linke Strukturformel zeigt alle Atome und Bindungen, die rechte vereinfachte Struktur dagegen zeigt nur die Kohlenstoffkette (ohne Wasserstoffatome) und das Sauerstoffatom.
- H3C-O-CH-(CH3)2 heißt 2-Methoxypropan oder Isopropylmethylether. Die höherrangige Propan-Kette bildet den Stammnamen, an die ein Methoxy-Substituent an 2- (bzw. iso-) Position des Alkans gebunden ist.
- Auch hier zeigt die linke Strukturformel alle Atome, wobei jetzt mit Methylgruppe CH3 ohne Bindungen verkürzt dargestellt ist; die rechte vereinfachte Struktur dagegen zeigt wieder nur die Kohlenstoffkette (ohne Wasserstoffatome) und das Sauerstoffatom. Die eigentliche Struktur des Stoffes ist auch mit der vereinfachten rechten Darstellung gut erkennbar.
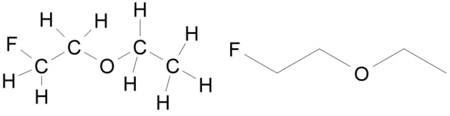
- FH2C-CH2-O-CH2-CH3 wird als 1-Ethoxy-2-fluorethan bezeichnet. Zwar sind beide Ketten prinzipiell gleichrangig, aber der fluorierte (und damit höher substituierte) Rest bildet den Namensstamm.
- Die linke Strukturformel zeigt wieder alle Atome und Bindungen und beginnt unübersichtlich zu werden, die rechte vereinfachte Struktur dagegen zeigt nur die Kohlenstoffkette (ohne Wasserstoffatome) und das Sauerstoff- und Fluoratom. Der eigentliche Molekülaufbau ist klar zu erkennen.
Cyclische Ether
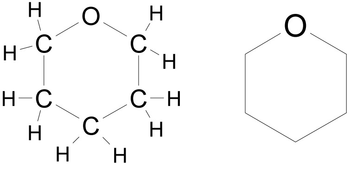
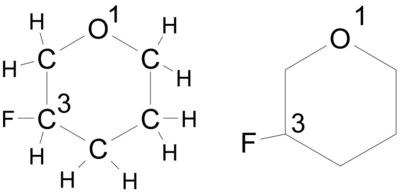
Cyclische Ether werden als Cycloalkane betrachtet, bei denen ein (oder mehrere) C-Atome durch (ein) O-Atom(e) ersetzt wurde(n). Um dies zu verdeutlichen, wird entsprechend dem Hantzsch-Widman-System die Silbe "Oxa" an der entsprechenden Position eingefügt. Beispiel:
Der IUPAC-Name ist Oxacyclohexan. Die Verbindung wird jedoch fast ausschließlich unter dem Namen Tetrahydropyran geführt. Die Verbindung ist cyclisch (cyclo), hat eine Ringgröße von 6 Atomen (hexan) und an einer Position ist ein C-Atom durch ein Sauerstoff-Atom ersetzt (oxa). Entsprechend gilt für die folgende Verbindung der Name 3-Fluor-oxacyclohexan oder gängiger: 3-Fluor-tetrahydropyran (das Heteroatom im Ring erhält die Position 1).
Eigenschaften
Die meisten Ether sind relativ reaktionsträge und werden daher oft als Lösungsmittel in der präparativen organischen Chemie verwendet. Da höhere Ether aufgrund wachsender sterischer Behinderungen schlechter Wasserstoffbrückenbindungen ausbilden können, nimmt die Löslichkeit in Wasser mit zunehmender Größe des Alkylrestes schnell ab.
Ausgewählte Daten einiger offenkettiger Ether Ether Struktur Smp. °C Sdp. °C Löslichkeit (in einem Liter H2O) Dipolmoment Dimethylether CH3-O-CH3 -138,5 -23,0 70g 1,30 D Diethylether C2H5-O-C2H5 -116,3 34,4 65 ml 1,14 D Di-n-propylether C3H7-O-C3H7 -123,2 90,1 0,5 g 1,32 D In starken Säuren sind Ether wegen der darin erfolgenden Protonierung unter Bildung von Oxoniumionen dagegen gut löslich.
Die physikalischen Eigenschaften der Ether unterscheiden sich erheblich von denen der entsprechenden Alkohole mit ähnlicher molarer Masse. Die Schmelz- und Siedepunkte der Ether sind erheblich niedriger als die der vergleichbaren Alkohole. Die hohe Elektronegativität des Sauerstoffs bestimmt jedoch ähnlich wie bei den Alkoholen wesentlich die Eigenschaften der Ether. Besonders bei cyclischen Ethern führt dies zur Ausbildung eines ausgeprägten Dipolmoments. Außerdem liegt das polare Sauerstoff-Atom in einer cyclischen Struktur exponierter vor. Dies wird von der Wasserlöslichkeit einiger cyclischer Ether bewiesen.
Ausgewählte Daten einiger cyclischer Ether Ether Struktur Smp. °C Sdp. °C Löslichkeit (in einem Liter H2O) Dipolmoment Tetrahydrofuran O-(CH2)4, cycl. -108,4 66,0 beliebige Menge 1,74 D 1,4-Dioxan O-(CH2)2-O-(CH2)2, cycl. 11,8 101,3 beliebige Menge 0,45 D Das niedrige Dipolmoment des 1,4-Dioxan wird durch seine symmetrische Struktur verursacht: die beiden sich im Ring gegenüberstehenden Sauerstoffatome verringern die Gesamtpolarität des Moleküls.
Strukturvergleich zweier cyclischer Ether 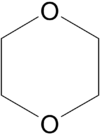
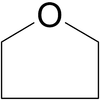
1,4-Dioxan Tetrahydrofuran Ethersynthese
Für Ether sind verschiedene Synthesewege möglich. Der wohl bekannteste Mechanismus ist die Ethersynthese nach Alexander William Williamson (1824-1904, Prof. am University College London). Hierbei wird ein Alkali-Alkoholat (hier ein Natrium-Alkoholat) mit einem Halogenalkan zur Reaktion gebracht, wobei neben dem entsprechenden Alkali-Halogen-Salz das gewünschte Produkt, der Ether, entsteht:
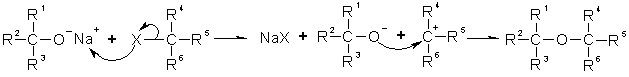
(R = Alkyl-Rest, Wasserstoff)Die Reaktion verläuft nach einem SN2-Mechanismus. Daher werden mit primären Alkoholaten + primären Halogenalkanen meist gute Ausbeuten erzielt; tertiäre Alkoholate ergeben häufig Elimination statt Substitution; mit tertiären Halogenalkanen ist die Synthese nicht durchführbar.
Die Williamson-Ethersynthese führt bei intramolekularer Reaktion zu cyclischen Ethern:

(nicht benannte Atome = Alkyl-Rest)Der einfachste Vertreter dieser Klasse ist das Oxacyclopropan (Ethylenoxid, Oxiran), der bekannteste Vertreter das Tetrahydrofuran (THF), welches ein beliebtes Lösemittel in der organischen Chemie ist.
weitere Mechanismen
- Säurekatalysierte Kondensation von Alkoholen
Unter Säurekatalyse (hier Salzsäure) können zwei Moleküle Alkohol zu einem Ether kondensiert werden:
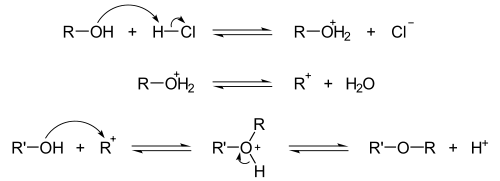
(R und R' = Alkyl-Rest)Bei Verwendung nur einer Alkoholart (R = R') können auf diesem Weg symmetrische Ether dargestellt werden.
- Addition von Alkoholen an Doppelbindungen
Alkohole können an Doppelbindungen addieren, wobei zunächst das Proton der Alkohol-Gruppe elektrophil an die Doppelbindung addiert wird. Anschließend lagert sich das Alkoholat nukleophil an:
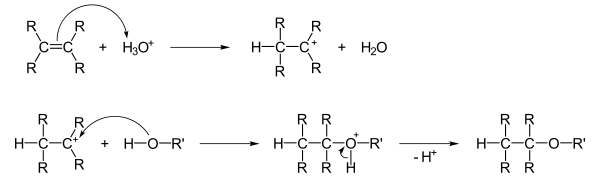
(R = Alkyl-Rest, Wasserstoff (evtl. Markownikow-Regel beachten))Besondere Ether
Heteroether
Neben den „normalen“ Ethern, also Alkylresten mit Sauerstoffbrücke, gibt es auch Analoga mit Verwandten des Sauerstoffs. In der 6. Hauptgruppe folgt auf den Sauerstoff der Schwefel. Dieser bildet entsprechend den oben beschriebenen Regeln so genannte Thioether. Bei diesen ist die Sauerstoffbrücke durch eine Schwefelbrücke ersetzt. Einer der bekanntesten Thioether dürfte das Senfgas sein.
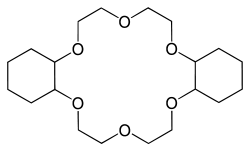
Kronenether
Kronenether sind eine besondere Gruppe von cyclischen Ethern, die aufgrund ihrer Bedeutung sowohl in der Chemie von Lebewesen, als auch in der technischen Chemie Erwähnung verdienen. Allgemein sind es cyclische Ether, die aus aneinander gebundenen 1,2-Diethern bestehen. Die gängige Nomenklatur von Kronenethern ist ungewöhnlich. Einer der einfachsten Kronenether ist [12]Krone-4. Hierbei gibt [12] die Gesamtzahl der Atome im Molekül (außer Wasserstoffatome) und -4 die Zahl der Sauerstoffatome im Molekül an. Kronenether besitzen die einzigartige Fähigkeit, Metallatome (bzw. Metallatomionen) in einer Art Käfigstruktur zu binden und dadurch als Bausteine zu Transportsystemen dieser Metalle zu dienen.
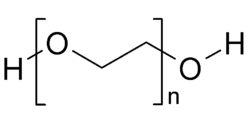
Polyether
Langkettige Verbindungen der Art
heißen Polyether (auch Polyalkylenglycole, Polyetherpolyole, Polyalkylenoxide). Beispiele für diese Gruppe polymerer Ether sind Polyethylenglykol und Polypropylenglykol, die beide durch katalytische Polymerisation der entsprechenden Epoxide (Oxirane) Ethylenoxid bzw. Propylenoxid hergestellt werden. In Fall von Polyethylenglykol und Polypropylenglykol sind alle Reste (R1, R2, R3...) mit Ausnahme der Endglieder der Ketten identisch. Bei der Umsetzung von Epoxiden mit Diolen können verschiedenste Polymere hergestellt werden. Die Zugabe eines einfachen Alkanols stoppt die Polymerisierung. Auch Epoxidharze sind Polyether mit endständigen Epoxidgruppen. Polyether sind, ebenso wie Polyester, wichtige Rohstoffe bei der Reaktion mit Isocyanaten zu Polyurethanen.
Gefahrenhinweise und Lagerung
Im Umgang mit Ethern (Ausnahme: Methyl-tert-butylether = MTBE) ist besonders darauf zu achten, dass Ether mit Luftsauerstoff hochexplosive Peroxide bilden. Diese können meist durch die Braunverfärbung von essigsauren Iodid-Lösungen nachgewiesen werden. Im Handel sind spezielle Teststäbchen erhältlich. Die Lagerung von Ethern für den Labor-Gebrauch sollte daher nur in kleinen Gebinden von maximal 1 Liter über Kaliumhydroxid-Plätzchen in Braunglasflaschen erfolgen. Bei dem Umgang mit niederen Ethern sollte deren niedriger Siedepunkt und leichte Entflammbarkeit nie unterschätzt werden. (Diethyl)Ether-Luft-Gemische sind zwischen 2 und 36 Vol% explosiv. Wichtig ist, dass Ether-Dämpfe nicht nur farblos, sondern auch schwerer als Luft sind. Sie sammeln sich also an tiefgelegenen Stellen. Aufgrund dieser Tatsache und der narkotisierenden Wirkung von Ethern sind sie nur in gut funktionierenden Abzügen zu verwenden.
Verwendung
Aufgrund ihres ambivalenten Charakters sind die meisten Ether hervorragende Lösungsmittel und lösen viele wasserunlösliche Verbindungen. So wird der Großteil des produzierten Diethylethers als Lösungsmittel im Umfeld der chemischen und medizinischen Industrie sowie im Laborbedarf verbraucht.
Sonstiges
- Der in der Umgangssprache bekannte „Ether“ bezeichnet Diethylether (C2H5-O-C2H5), einen der einfachsten Ether.
- Das Wort 'Ether' stammt aus dem Griechischen (aither, ᾿αιθήρ) und bedeutet in etwa "obere Luft" oder "Feuerluft".
- Diethylether diente zur Zeit der Prohibition teilweise als Ethanol-Ersatz (orale Einnahme) und vereinzelt sind auch noch heute Fälle des Etherkonsums bekannt. Die physiologische Wirkung ist ähnlich der des Alkohols. Beim Abbau des Diethylethers im Körper entsteht unter anderem auch Ethanol.
- Diethylether diente als einer der ersten Stoffe als Narkotikum. Aufgrund der starken Nebenwirkungen (ausgeprägte Erregungsphase, Übelkeit, Brennbarkeit), ist er jedoch in der Anästhesie nur noch von historischem Interesse.
Wikimedia Foundation.