- Flavonoid
-
Die Flavonoide sind eine Gruppe von wasserlöslichen Pflanzenfarbstoffen und spielen eine wichtige Rolle im Stoffwechsel vieler Pflanzen. Sie gehören zusammen mit den Phenolsäuren zu den Polyphenolen. Laut DGE gibt es über 6500 unterschiedliche Flavonoide. Die meisten Flavonoide sind an Glukose oder Rhamnose gebunden – daher nennt man sie Glykoside. Nur die Flavanole und die Proanthocyanidine sind nicht an Zuckermoleküle gebunden (= Aglykone). Flavonoide befinden sich in vielen pflanzlichen Lebensmitteln wie Zitronen, Nopal-Feigenkaktus Opuntia, Weintrauben bis zu Tee und der kakaohaltigen Schokolade (dort: Epicatechin).
Die Flavonoide wurden in den 1930er Jahren durch den Nobelpreisträger Albert von Szent-Györgyi Nagyrapolt entdeckt und zunächst als Vitamin P bezeichnet. Das "P" im Vitamin P steht für Permeabilitätsfaktor. Die Flavonoide zählen zu den sekundären Pflanzenstoffen. Der Name leitet sich von lat. flavus = gelb ab, weil Flavonoide häufig, aber nicht zwangsläufig eine gelbe Farbe besitzen.
Inhaltsverzeichnis
Nomenklatur und Einteilung der Flavonoide
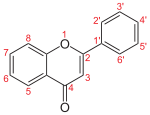
Flavan: 2,3 gesättigt
Flavon: 2,3 ungesättigt; 4 oxidiert (Keton)
Flavonol: 2,3 ungesättigt; 4 oxidiert (Keton), 3-hydroxyliert
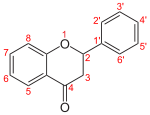
Flavanon: 2,3 gesättigt, 4 oxidiert (Keton)
Flavanonol 2,3 gesättigt, 4 oxidiert (Keton), 3-hydroxyliert
Flavonoide können in folgende Gruppen eingeteilt werden:
Flavonoid Beispiele Vorkommen 1. Flavone Luteolin, Apigenin Sellerie, Paprika 2. Flavonole Morin, Quercetin, Rutin, Kaempferol, Myricetin, Isorhamnetin, Fisetin Zwiebeln, Endivien 3. Flavanole Catechin, Gallocatechin, Epicatechin, Epigallocatechingallat, Theaflavin, Thearubigin Rotwein, Äpfel, Grüner Tee, Kakao 4. Flavanone Hesperetin, Naringenin, Eriodictyol Grapefruit, Orange 5. Flavanonole Taxifolin Ginkgo 6. Isoflavone Genistein, Daidzein, Licoricidin Sojabohnen 7. Anthocyanidine (Anthocyane) Cyanidin, Delphinidin, Malvidin, Pelargonidin, Peonidin, Petunidin Heidelbeeren, blaue Trauben, Kirschen Positive Effekte auf die Gesundheit
Einige Flavonoide haben gefäßverstärkende Wirkung, andere wirken gegen Entzündung und Histamin oder haben antivirale und krampflösende Wirkungen. Manche Flavonoide wie zum Beispiel Quercetin sind gute Antioxidantien. Gemäß mehreren Studien werden die gesundheitlichen Vorteile der Flavonoide jedoch durch Milch zunichte gemacht. Deshalb helfen sie z.B. nicht bei Milchschokolade[1] oder Schwarztee mit Milch[2]. Zahlreiche Studien bestätigen eine Korrelation zwischen der Zufuhr von Flavonoiden und der Risikoabnahme bei verschiedenen Krankheiten:
Schutz vor Krebs
Flavonoide sind Antioxidantien, wobei die antioxidative Wirkung strukturbestimmt und damit sehr unterschiedlich ausgeprägt ist. Viele Studien sprechen für die antikanzerogene Wirkung der Flavonoide und zwar sowohl in der Initiations- als auch der Promotionsphase der Krebsbildung. Catechine, Anthocyane und Flavonole wirken sich besonders positiv aus, da ein großer Teil nicht absorbiert wird und bis in den Dickdarm gelangt. Besonders wirksam sind offenbar die Flavonoide, die aus Äpfeln, Zwiebeln, grünem Tee, Heidelbeeren und Moosbeeren stammen.
Schutz vor Herz-Kreislauf-Erkrankungen
Flavonoide beeinflussen die Blutgerinnung. Sie senken indirekt die Thromboxanbildung. Auch hier kommt wieder die antioxidative Wirkung zum Tragen: Sie schützen LDL-Lipoproteide vor Oxidation und können den Blutcholesterinspiegel senken, jedoch ohne das HDL-Cholesterin abzusenken. Eine verbesserte Endothelfunktion wird in einigen Studien insbesondere nach Aufnahme von grünem Tee, rotem Traubensaft und dunkler Schokolade beschrieben.
Antibakterielle und antivirale Wirkung
Procyanidine, die vor allem in Heidel- und Moosbeeren vorkommen, hemmen Bakterien, die Harnwegserkrankungen verursachen. Ebenso konnten schützende Wirkungen verschiedener Flavanole aus grünem Tee bei Befall mit Grippe-Viren nachgewiesen werden.
Verbesserung des Langzeitgedächtnisses
Nach einer Studie von Pamela Maher vom Salk Institute for Biological Studies in La Jolla (Kalifornien), verbessert in großen Mengen das zu der Gruppe der Flavonoide gehörende Fisetin das Langzeitgedächtnis.[3] Anscheinend werden im Gehirn bestimmte Signalketten stimuliert, Nervenzellen reifen aus und differenzieren sich. Fisetin ist insbesondere in Weintrauben enthalten.
Negative Effekte auf die Gesundheit
Einige der Flavonoide besitzen eine hormonähnliche Wirkung (Phytoöstrogene) oder zeigen Wechselwirkungen mit Medikamenten (z.B. Quercetin und Kämperol). Bei einigen (z.B. Genistein, welches in Sojabohnen vorkommt) wurde eine zellschädigende Wirkung nachgewiesen.
Vorkommen
Schätzungsweise werden zwei Prozent des gesamten Kohlenstoffs, der durch die Photosynthese in den Pflanzen fixiert wird, zu Flavonoiden und deren Derivaten wie den Anthocyanen umgesetzt. Das sind nicht weniger als 109 Tonnen pro Jahr.
Biosynthese
Aus dem Pyruvat, das aus der bei der Photosynthese entstehenden Glucose stammt, entsteht bei der oxidativen Decarboxylierung zusammen mit dem Coenzym A und NAD Acetyl-CoA, Kohlenstoffdioxid und NADH. Das Acetyl-CoA ist der Ausgangsstoff, der Biosynthese der Flavonoide. Bereits hier teilt sich die Biosynthese in zwei Schritte, die später wieder aufeinander treffen.
Ein Teil des Acetyl-CoA wird über mehrere Schritte über den Shikimisäureweg (siehe dort für eine ausführliche Erklärung) in Phenylalanin umgewandelt. Teile des Phenylalanins werden in den Pflanzen nun für den Proteinaufbau benötigt. Der Rest wird durch das Enzym Phenylalanin-Ammoniak-Lyase (PAL) in Zimtsäure umgewandelt. Durch das Enzym Zimtsäure-4-Hydroxylase wird die Zimtsäure in Cumarsäure hydroxiliert. Diese wird wiederum mit Acetyl-CoA und dem Enzym Zimtsäure-CoA-Ligase in Cumaryl-CoA umgewandelt. Aus dem Cumaryl-CoA kann nun Cumarin gebildet werden, die Biosynthese der Flavonoide geht aber noch weiter.
Ein anderer Teil des Acetyl-CoA wird mit ATP und einem Hydrogencarbonatanion in Malonyl-CoA, ADP und H+ umgewandelt.
Drei der Malonyl-CoA-Moleküle reagieren nun mit dem Cumaryl-CoA (Chalkonsynthase). Durch Isomerase kann das entstehende Chalkon in Flavanon überführt werden. Von dem Flavanon aus lassen sich nun alle Flavonoide biosynthetisieren. Das Flavanon kann in die Flavone und Flavanonole umgewandelt werden. Aus diesem entstehen die Flavan-3-ole, Flavonole, Flavan-3,4-diole und über mehrere Schritte die Anthocyane.
Werden Pflanzen stärker belichtet, kann die Photosynthese häufiger ablaufen und es wird mehr Acetyl-CoA gebildet, wodurch die Biosynthese der Flavonoide also vermehrt ablaufen kann und damit mehr Flavonoide gebildet und die Pflanzen farbiger werden. Die Biosynthese der Flavonoide konnte über Deuterium-Tracer nachgewiesen werden.
Literatur
- Graf B.A., Milbury P.E., Blumberg, J.B.: Flovols, Flavanones, and Human Health: Epidemiological Evidence. J Med Food 8, 281–290 (2005) PMID 16176136
- Watzl B., Leitzmann C.: Bioaktive Substanzen in Lebensmitteln, 3. unveränderte Auflage, Hippokrates, Stuttgart 2005, ISBN 3-8304-5308-6
- Bernhard Watzl, Gerhard Rechkemmer. Basiswissen aktualisiert: Flavonoide. Ernährungs-Umschau 48 (2001) Heft 12 (PDF)
Einzelnachweise
Wikimedia Foundation.