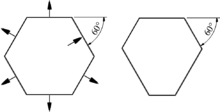
- Kristallmorphologie
-
Die Kristallmorphologie ist ein Begriff aus der Kristallographie und der Mineralogie und beschreibt die Form eines Kristalls, der aus geometrisch bestimmten Flächen, Kanten und Ecken besteht. Zwei aneinander stoßende Kristallflächen bilden dabei eine Kristallkante und mindestens drei Kanten bilden eine Kristallecke. Je nach Kristallsystem und Kristallklasse schließen die Kanten dabei bestimmte, für die betreffende Kristallklasse charakteristische Winkel ein.
Um die Lage von Kristallflächen und -kanten im Raum mathematisch zu beschreiben, bedient sich der Mineraloge verschiedener Indizes. Mit den millerschen Indizes (hkl) wird dabei die Lage der Flächen in Bezug auf das Achsensystem des Kristalls beschrieben, mit den Richtungsindizes [uvw] die Richtung der Kanten.
Inhaltsverzeichnis
Kristallfläche
 Kombination Würfel {100} mit Oktaeder {111}, würfeliger Habitus
Kombination Würfel {100} mit Oktaeder {111}, würfeliger Habitus
 gleiche Tracht: {100} und {111}, aber oktaedrischer Habitus
gleiche Tracht: {100} und {111}, aber oktaedrischer Habitus
Die Kristallflächen bilden die äußere Begrenzung des Kristallkörpers und liegen parallel zu den Gitter- beziehungsweise Netzebenen der dem Kristall innewohnenden Kristallstruktur, die wiederum von seiner chemischen Zusammensetzung abhängt. Durch Symmetrieoperationen ineinander überführbare kristallographische Flächen heißen Form (s. u.). Die Kombination der ausgebildeten Formen heißt Tracht. Dieser Begriff ist nicht zu verwechseln mit dem Habitus, der die geometrische Ausdehnung eines Kristalls beschreibt. Der Habitus kann z. B. stängelig, faserig, plattig oder isometrisch sein.
Kristallflächen bilden sich bevorzugt an den Netzebenen, die die dichteste Packung (größte Anzahl von Atomen) und gleichzeitig möglichst wenig freie, offene Valenzen aufweisen (chemische Neutralität). Bei idealen Kristallen besitzen die Flächen eine klare Geometrie (Dreieck, Viereck, Sechseck) und bilden zusammen regelmäßige Körper (siehe platonischer Körper, catalanischer Körper). Bei Kristallen, die ihre Eigengestalt störungsfrei voll entwickeln konnten, spricht man auch von idiomorphen Kristallen. Welche Gestalt dies ist, bestimmt die jeweilige Kristallklasse, der der Kristall angehört. Ein idiomorpher Kristall ist daher nicht gleichzusetzen mit einem holoedrischen Kristall.
Natürliche Kristalle bilden sich aber nur selten in der idealen Form, bedingt durch Störungen der Stoffzufuhr und das anisotrope Verhalten beim Wachsen des Kristalls während der Kristallisation oder durch gegenseitige Behinderung bei einer vielzahl gleichzeitig entstehender Kristalle, beispielsweise bei schneller Abkühlung. Kristallflächen können somit verzerrt sein oder sogar ganz fehlen. Sie stehen jedoch zum einen immer konvex zueinander, was bedeutet, dass sie sich vom Kristallmittelpunkt „wegbeugen“ und zum anderen bleiben trotz aller Verformungen die Winkel zwischen den Flächen immer konstant. Bei Kristallen, die ihre Eigengestalt aufgrund der genannten Störungen nur teilweise entwickeln konnten, spricht man von hypidiomorphen Kristallen.
Wird ein Kristall während des Wachstums so sehr gestört, dass er seine Eigengestalt gar nicht entwickeln konnte, spricht man von xenomorphen Kristallen.
Kristallform
 Beispiel für die Kombination einer offenen Form (hexagonales Prisma) mit einer geschlossenen (Rhomboeder)
Beispiel für die Kombination einer offenen Form (hexagonales Prisma) mit einer geschlossenen (Rhomboeder)
In der Kristallographie bezeichnet man als Form (seltener Kristallform oder Flächenform; engl. form, crystal form, face form, frz. forme[1]) die Gesamtheit aller zueinander symmetrieäquivalenten Kristallflächen. Eine Kristallform wird mit dem Symbol {hkl}, also den millerschen Indizes (hkl) einer der Flächen in geschweiften Klammern, bezeichnet. Man beachte, dass sich die kristallographische Bedeutung des Begriffs Kristallform deutlich von der umgangssprachlichen Bedeutung unterscheidet: die „Form“ eines Kristalls im umgangssprachlichen Sinn wird eher durch die Begriffe Tracht und Habitus beschrieben. Ein einzelner Kristall hat genau eine Tracht und einen Habitus, aber in der Regel mehrere (kristallographische) Formen.
Kristallformen können geschlossene Körper (Polyeder), wie Würfel oder Oktaeder, bilden. Daneben gibt es aber auch offene Formen, wie das Pinakoid, aber auch Prismen und Pyramiden. Solche offenen Formen müssen an einem Kristall notwendig mit anderen Formen kombiniert sein. Man beachte, dass die Basisflächen von Prismen oder Pyramiden – anders als in der Schulgeometrie – nicht zur Form dazugehören; sie sind nicht symmetrieäquivalent zu den eigentlichen Prismen- oder Pyramidenflächen. Ein tetragonales (quadratisches) Prisma hat in der Kristallographie also vier, nicht sechs Flächen.
Insgesamt gibt es 17 offene (18, wenn man das Dieder in Doma und Sphenoid unterteilt) und 30 geschlossene Sorten kristallographischer Formen.[2][1]
Man unterscheidet daneben allgemeine Formen und spezielle Formen, außerdem Grenzformen. Die allgemeine Form {hkl} geht aus einer „Fläche allgemeiner Lage“ (hkl) hervor, das heißt die Fläche liegt nicht parallel oder senkrecht zu einer Spiegelebene oder senkrecht zu einer Drehachse; die Indizes h, k, l sind im allgemeinen nicht null und paarweise verschieden. Andernfalls handelt es sich um spezielle Formen. Grenzformen nehmen eine Zwischenstellung ein: Sie haben die gleiche Flächenzahl und Symmetrie wie die allgemeine Form. Zum Beispiel ist die allgemeine Form der Kristallklasse 3 die trigonale Pyramide {hkil}; wird der Index l immer kleiner, die Flächen also immer steiler, so ergibt sich als Grenzform das trigonale Prisma {hki0}. Eine spezielle Form in dieser Kristallklasse wäre die Basisfläche (das Pedion) (0001).
Die folgenden Tabellen geben einen Überblick über alle Formen der 32 Kristallklassen. Nebeneinander stehen zunächst die allgemeine Form {hkl}, dann die speziellen und Grenzformen. Angegeben ist jeweils der Name der Form mit Synonymen sowie die Zahl der Flächen.
Triklines Kristallsystem Kristallklasse {hkl} 
triklin-pedial 
Pedion (1)
triklin-pinakoidal 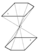
Pinakoid (2)Monoklines Kristallsystem Kristallklasse {hkl} {h0l} {010} 
monoklin-sphenoidisch 
Sphenoid (2)(Klino-) Pinakoid (2) Pedion (1) 
monoklin-domatisch 
Doma (2)Pedion (1) (Ortho-) Pinakoid (2) 
monoklin-prismatisch monoklines Prisma (4) (Klino-) Pinakoid (2) (Ortho-) Pinakoid (2) Orthorhombisches Kristallsystem Kristallklasse {hkl} {hk0} {h0l} und {0hl} {100} und {010} {001} 
rhombisch-pyramidal 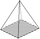
rhombische Pyramide (4)
rhombisches Prisma (4)Doma (2) Pinakoid (2) Pedion (1) 
rhombisch-disphenoidisch 
rhombisches Disphenoid (4)
rhombisches Prisma (4)
rhombisches Prisma (4)Pinakoid (2) 
rhombisch-dipyramidal 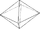
rhombische Dipyramide (8)
rhombisches Prisma (4)
rhombisches Prisma (4)Pinakoid (2) Tetragonales Kristallsystem Kristallklasse {hkl} {h0l} {hhl} {hk0} {100} und {110} {001} 
tetragonal-pyramidal 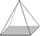
tetragonale Pyramide (4)
tetragonales Prisma (4)Pedion (1) 
tetragonal-disphenoidisch 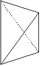
tetragonales Disphenoid (4)
tetragonales Prisma (4)Pinakoid (2) 
tetragonal-dipyramidal 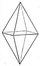
tetragonale Dipyramide (8)
tetragonales Prisma (4)Pinakoid (2) 
ditetragonal-pyramidal 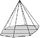
ditetragonale Pyramide (8)
tetragonale Pyramide (4)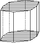
ditetragonales Prisma (8)
tetragonales Prisma (4)Pedion (1) 
tetragonal-skalenoedrisch 
tetragonales Skalenoeder (8)
tetragonale Dipyramide (8)
tetragonales Disphenoid (4)
ditetragonales Prisma (8)
tetragonales Prisma (4)Pinakoid (2) 
tetragonal-trapezoedrisch 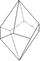
tetragonales Trapezoeder (8)
tetragonale Dipyramide (8)
ditetragonales Prisma (8)
tetragonales Prisma (4)Pinakoid (2) 
ditetragonal-dipyramidal 
ditetragonale Dipyramide (16)
tetragonale Dipyramide (8)
ditetragonales Prisma (8)
tetragonales Prisma (4)Pinakoid (2) Trigonales Kristallsystem Kristallklasse {hkil} {h0hl} {hh 2h l} {hki0} {1010} {1120} {0001} 
trigonal-pyramidal 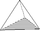
trigonale Pyramide (3)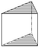
trigonales Prisma (3)Pedion (1) 
rhomboedrisch 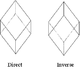
Rhomboeder (6)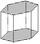
hexagonales Prisma (6)Pinakoid (2) 
ditrigonal-pyramidal 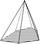
ditrigonale Pyramide (6)
trigonale Pyramide (3)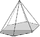
hexagonale Pyramide (6)
ditrigonales Prisma (6)
trigonales Prisma (3)
hexagonales Prisma (6)Pedion (1) 
trigonal-trapezoedrisch 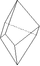
trigonales Trapezoeder (6)
Rhomboeder (6)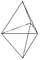
trigonale Dipyramide (6)
ditrigonales Prisma (6)
hexagonales Prisma (6)
trigonales Prisma (3)Pinakoid (2) 
ditrigonal-skalenoedrisch 
ditrigonales Skalenoeder (12)
Rhomboeder (6)
hexagonale Diyramide (12)
dihexagonales Prisma (12)
hexagonales Prisma (6)Pinakoid (2) Hexagonales Kristallsystem Kristallklasse {hkil} {h0hl} {hh 2h l} {hki0} {1010} {1120} {0001} 
hexagonal-pyramidal 
hexagonale Pyramide (6)
hexagonales Prisma (6)Pedion (1) 
trigonal-dipyramidal 
trigonale Dipyramide (6)
trigonales Prisma (3)Pinakoid (2) 
hexagonal-dipyramidal 
hexagonale Dipyramide (12)
hexagonales Prisma (6)Pinakoid (2) 
dihexagonal-pyramidal 
dihexagonale Pyramide (12)
hexagonale Pyramide (6)
dihexagonales Prisma (12)
hexagonales Prisma (6)Pedion (1) 
ditrigonal-dipyramidal 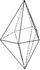
ditrigonale Dipyramide (12)
trigonale Dipyramide (6)
hexagonale Diyramide (12)
ditrigonales Prisma (6)
trigonales Prisma (3)
hexagonales Prisma (6)Pinakoid (2) 
hexagonal-trapezoedrisch 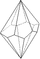
hexagonales Trapezoeder (12)
hexagonale Dipyramide (12)
dihexagonales Prisma (12)
hexagonales Prisma (6)Pinakoid (2) 
dihexagonal-dipyramidal 
dihexagonale Dipyramide (24)
hexagonale Dipyramide (12)
dihexagonales Prisma (12)
hexagonales Prisma (6)Pinakoid (2) Kubisches Kristallsystem Kristallklasse {hkl} {hhl} (h>l) {hll} (h>l) {hk0} {111} {110} {100} 
tetraedrisch-pentagondodekaedrisch 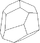
tetraedrisches Pentagondodekaeder (Pentagon-Tritetraeder, Tetartoeder) (12)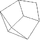
Deltoiddodekaeder (Tetragon-Tritetraeder) (12)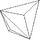
Triakistetraeder (Tristetraeder, Trigon-Tritetraeder) (12)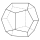
Pentagondodekaeder (Pyritoeder) (12)
Tetraeder (4)
Rhombendodekaeder (Granatoeder) (12)
Würfel (Hexaeder) (6)
disdodekaedrisch 
Disdodekaeder (Dyakisdodekaeder, Diploeder, Diploid) (24)
Triakisoktaeder (Trisoktaeder, Trigon-Trioktaeder) (24)
Deltoidikositetraeder (Ikositetraeder, Tetragon-Trioktaeder, Trapezoeder, Leucitoeder) (24)
Pentagondodekaeder (Pyritoeder) (12)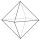
Oktaeder (8)
Rhombendodekaeder (Granatoeder) (12)
Würfel (Hexaeder) (6)
pentagonikositetraedrisch 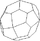
Pentagonikositetraeder (Gyroeder, Gyroid) (24)
Triakisoktaeder (...) (24)
Deltoidikositetraeder (...) (24)
Tetrakishexaeder (Tetrahexaeder) (24)
Oktaeder (8)
Rhombendodekaeder (Granatoeder) (12)
Würfel (Hexaeder) (6)
hexakistetraedrisch 
Hexakistetraeder (Hexatetraeder) (24)
Deltoiddodekaeder (Tetragon-Tritetraeder) (12)
Triakistetraeder (...) (12)
Tetrakishexaeder (Tetrahexaeder) (24)
Tetraeder (4)
Rhombendodekaeder (Granatoeder) (12)
Würfel (Hexaeder) (6)
hexakisoktaedrisch 
Hexakisoktaeder (Hexaoktaeder) (48)
Triakisoktaeder (...) (24)
Deltoidikositetraeder (...) (24)
Tetrakishexaeder (Tetrahexaeder) (24)
Oktaeder (8)
Rhombendodekaeder (Granatoeder) (12)
Würfel (Hexaeder) (6)Morphologische Gesetze
Das Gesetz der Winkelkonstanz
Das Gesetz der Winkelkonstanz besagt:
Alle zur selben Kristallart gehörenden Einzelkristalle schließen zwischen analogen Flächen – gleichen Druck, gleiche Temperatur und chemische Zusammensetzung vorausgesetzt – stets gleiche Winkel ein.
Der Däne Niels Stensen (lat. Nicolaus Steno) bemerkte um 1669 bei der Untersuchung von Quarz, dass die Flächen der Kristalle – unabhängig von ihrer Größe und Form – immer gleiche Winkel bilden. Er vermutete, dass dies eine Eigenschaft aller Mineralkristalle sei.[3] Bestätigt wurde diese Vermutung nach weiteren Vorarbeiten durch Torbern Olof Bergman schließlich von Jean-Baptiste Romé de L’Isle. Romé de L’Isle und sein Assistent Arnould Carangeot vermaßen systematisch Kristalle mit dem von Carangeot entwickelten Anlegegoniometer. 1783 veröffentlichte Romé de L’Isle eine detaillierte Beschreibung von 500 Kristallarten, die auf diesen Messungen basierte.[4] Dabei konnte er empirisch bestätigen, dass das Gesetz der Winkelkonstanz – wie von Steno vermutet – für jede Kristallart gilt. Romé de L’Isles systematische Messungen und der daraus folgende induktive Beweis des Gesetzes der Winkelkonstanz sind das erste Beispiel für wissenschaftliches (methodisch-empirisches) Vorgehen in der Kristallographie. Insofern kann Romé de L’Isle als Begründer der wissenschaftlichen Kristallographie gelten.
Wenn man bedenkt, auf welche Weise Kristalle wachsen, ist dieses Gesetz nur logisch. Die chemische Zusammensetzung und die Bindungsart der Grundbausteine eines Minerals bestimmt die Ausbildung des Kristallsystems mit den entsprechenden Atomen und Molekülen an den Kreuzungspunkten des Raumgitters. Weitere Atome werden immer parallel zu den einzelnen Ebenen des Raumgitters eingebaut. Durch Konvektionsströme innerhalb der mineralischen Lösung kommt es zur unregelmäßigen Verteilung der aufbauenden Atome und damit zur Bevorzugung oder Benachteiligung einzelner Flächen. Dennoch bleiben die Winkel zwischen den Ebenen des Raumgitters durch das vorbestimmte Kristallsystem zwingend erhalten.
Das Bravaissche Gesetz
Mit Auguste Bravais begannen Versuche, Gesetze zu finden, mit denen sich die Kristallmorphologie aus der inneren Kristallstruktur vorhersagen lässt (und umgekehrt). Bravais sagte um 1848 voraus, dass die „relative Wichtigkeit“ einer Kristallfläche proportional ist zu ihrer Besetzungsdichte, d.h. dass Formen um so wahrscheinlicher am Kristall auftreten, je mehr Gitterpunkte je Flächeneinheit auf der entsprechenden Gitterebene liegen. Gleichbedeutend damit ist, dass die morphologische Wichtigkeit einer Fläche umgekehrt proportional zum Netzebenabstand ist.
Im 20. Jahrhundert wurde das Bravaissche Gesetz (auch Bravaissches Prinzip, frz. „loi de Bravais“, engl. „Bravais rule“) von Georges Friedel[5] sowie von J. D. H. Donnay und David Harker (Donnay-Harker-Regel)[6] wieder aufgegriffen. Während Bravais bei seinen Überlegungen nur Zentrierungen (die Bravais-Gitter) berücksichtigte, bezogen Donnay und Harker auch andere Symmetrielemente (Gleitspiegelebenen und Schraubenachsen) ein, die zu veränderten Besetzungsdichten von Gitterebenen führen. Sie konnten so jeder Raumgruppen eine Flächenrangfolge zuordnen, die sie morphologischer Aspekt nannten.
Die Goldschmidtsche Komplikationsregel
Victor Mordechai Goldschmidt stellte 1897 das Komplikationsgesetz (Komplikationsregel) auf, welches besagt, dass sich aus zwei Kristallflächen, z.B. (100) und (010), durch wiederholte Addition oder Subtraktion ihrer millerschen Indizes alle weiteren Flächen dieser Zone ableiten lassen. Durch umfangreiche statistische Untersuchungen konnte Goldschmidt zeigen, dass Flächen im Allgemeinen um so seltener auftreten, je „komplizierter“ diese Ableitung ist, also je größer ihre Indizes werden.[7]
Literatur
- Paul Ramdohr, Hugo Strunz: Lehrbuch der Mineralogie (16. Aufl.), Ferdinand Enke Verlag (1978), ISBN 3-432-82986-8
- Hans-Joachim Bautsch, Will Kleber, Joachim Bohm: Einführung in die Kristallographie. Oldenbourg Wissenschaftsverlag, 1998 (Eingeschränkte Vorschau in der Google Buchsuche).
Einzelnachweise
- ↑ a b IUCr Online Dictionary of Crystallographie: Form
- ↑ Paul Niggli: Zur Topologie, Metrik und Symmetrie der einfachen Kristallformen. Schweiz. Mineral. u. Petrogr. Mitt. 43 (1963) S. 49–58
- ↑ Nicolaus Steno: De solido intra solidum naturaliter contento dissertationis prodromus. (Vorläufer einer Dissertation über feste Körper, die innerhalb anderer fester Körper von Natur aus eingeschlossen sind.) Florenz 1669
- ↑ Jean-Baptiste Romé de L’Isle: Cristallographie, ou Déscription des formes propres à tous les corps du règne minéral. 1783
- ↑ Georges Friedel: Études sur la loi de Bravais. Bull. Soc. Franc. Miner. 30 (1907), S. 326–455
- ↑ J. D. H. Donnay, David Harker: A new law of crystal morphology extending the law of Bravais. Amer. Miner. 22 (1937), S. 446–?
- ↑ Victor Mordechai Goldschmidt: Über Entwicklung der Krystallformen. Z. Kristall. 28 (1897), S. 1–35, 414–451
Weblinks
Wikimedia Foundation.