- Zungengrundstruma
-
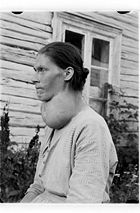
Die Struma oder der Kropf (veraltet: Satthals) bezeichnen eine tastbare, sichtbare oder messbare Vergrößerung der Schilddrüse zunächst unabhängig von der Stoffwechsellage (Überfunktion, Unterfunktion oder normale Funktion der Schilddrüse) und von der feingeweblichen Struktur oder mit dem bloßen Auge zu erkennenden Gestalt.
Die Struma ist weltweit die häufigste Erkrankung der Hormondrüsen (eine Endokrinopathie). Die häufigste Ursache für das Entstehen einer Struma ist ein Jodmangel. Die Behandlungsmöglichkeiten umfassen neben einer medikamentösen Therapie mit Gabe von Jod und/oder Schilddrüsenhormonen eine Schilddrüsenoperation und eine Radiojodtherapie.
Die Bezeichnung „Kropf“, welche auch eine Aussackung der Speiseröhre bei Vögeln bezeichnet, wird auf das indogermanische greup zurückgeführt. „Greup“ bedeutet „krümmen“ und verweist auf die auf einer Struma gekrümmt verlaufenden Halsvenen.[1] Das Synonym „Struma“ (lateinisch struma, „Drüsenschwellung“; Mehrzahl Strumae oder eingedeutscht Strumen) wurde 1718 von Lorenz Heister und später von Albrecht von Haller in die medizinische Literatur eingeführt.
Inhaltsverzeichnis
Einteilung
Klassifikation nach ICD-10 E01 jodmangelbedingte Schilddrüsenkrankheiten und verwandte Zustände E01.0 jodmangelbedingte diffuse Struma (endemisch) E01.1 jodmangelbedingte mehrknotige Struma (endemisch) E01.2 jodmangelbedingte Struma (endemisch), nicht näher bezeichnet E04 sonstige nichttoxische Struma E04.0 nichttoxische diffuse Struma E04.1 nichttoxischer solitärer Schilddrüsenknoten E04.2 nichttoxische mehrknotige Struma E05 Hyperthyreose (Thyreotoxikose) E05.0 Hyperthyreose mit diffuser Struma
- Morbus BasedowE05.1 Hyperthyreose mit toxischem solitärem Schilddrüsenknoten E05.2 Hyperthyreose mit toxischer mehrknotiger Struma ICD-10 online (WHO-Version 2006) Nach der Ausprägung (morphologisch) wird eine Struma diffusa (gleichmäßig vergrößert) von der Struma nodosa (bereits Knoten vorhanden) unterschieden. Die Struma uninodosa weist einen einzelnen Knoten auf, die Struma multinodosa mehrere.
Nach der Lage wird die eutope Struma (normale anatomische Lage) von der dystopen Struma (Struma im Brustkorb (retrosternal), hinter der Luftröhre oder unter der Zunge) abgegrenzt.
Nach ihrer Funktion (funktionell) unterscheidet man die euthyreote Struma (normale Stoffwechselwerte) von der hypothyreoten Struma (bei Unterfunktion) und hyperthyreoten Struma oder toxischen Struma (bei Überfunktion).
Nach ihrem Auftreten (epidemiologisch): Sind innerhalb eines Gebietes mehr als 10 % der Bevölkerung betroffen, spricht man von einer endemischen Struma, sonst von einer sporadischen Struma.
Nach ihrer Dignität wird zwischen der Struma maligna, die einen bösartigen Tumor enthält, wobei es sich meist um ein Schilddrüsenkarzinom handelt, und der blanden Struma unterschieden, bei der es sich um eine nicht-entzündliche, gutartige Schilddrüsenvergrößerung bei normaler Stoffwechsellage handelt. Eine nach Therapie erneut auftretende Struma heißt Rezidivstruma.
Die Weltgesundheitsorganisation (WHO) unterscheidet folgende Struma-Grade nach Größe, die jeweils mit minimalen Unterschieden zitiert werden:
Einteilungen der Struma-Grade nach Hotze und Schumm-Dräger[2] nach AWMF-Leitlinie[3] Grad 0a Keine Struma Stadium 0 Keine Struma Grad 0b Tastbare, aber nicht sichtbare Struma Stadium 1a Palpatorische, aber nicht sichtbare Vergrößerung Grad I Tastbare und bei zurückgebeugtem Kopf eben sichtbare Struma Stadium 1b Bei maximaler Halsreklination sichtbare Vergrößerung Grad II Sichtbare Struma Stadium 2 Bei normaler Kopfhaltung sichtbare Schilddrüse Grad III Große sichtbare Struma Stadium 3 Stark vergrößerte Schilddrüse Die Einstufung eines Patienten in diese Grade hängt einerseits von subjektiven Faktoren beim Untersucher ab, andererseits vom Ernährungszustand des Patienten und der Ausprägung der Halsmuskulatur. Daher kann sie nur zur orientierenden Beschreibung des Befundes dienen, nicht zur exakten Größenangabe der Schilddrüse.
Ursachen
Die weltweit häufigste Ursache der Struma ist mit etwa 90 Prozent ein ernährungsbedingter, sogenannter alimentärer, Jodmangel.[4]
Hiervon müssen andere, weniger häufige ätiologische Faktoren abgegrenzt werden. Zu diesen gehören Schilddrüsenautonomien, Autoimmunerkrankungen der Schilddrüse (die Autoimmunthyreopathien Morbus Basedow und Hashimoto-Thyreoiditis), bestimmte kropfverursachende, sogenannte strumigene, Medikamente (zum Beispiel Lithium und Thyreostatika) sowie andere strumigene Substanzen (zum Beispiel Thiocyanat und Nitrate), Entzündungen des Schilddrüsengewebes (Thyreoiditis), Zysten in der Schilddrüse sowie gutartige und bösartige Tumoren der Schilddrüse, wobei es sich bei den bösartigen Veränderungen der Schilddrüse insbesondere um Schilddrüsenkrebs und seltener um Metastasen bösartiger Tumoren anderer Gewebe und Organe des Körpers in die Schilddrüse handelt.
Weitere seltene Ursachen einer Struma sind gutartige Tumoren der Hirnanhangsdrüse (Hypophyse), eine Blasenmole, eine Akromegalie, Störungen der Schilddrüsenhormonsynthese, eine periphere Schilddrüsenhormonresistenz, eine Sarkoidose, eine Amyloidose, Parasiten und weitere. Das Rauchen von Tabak und ein Mangel an Selen werden zudem als Ursachen für eine Struma diskutiert.
Häufigkeit
Weltweit leben etwa eine Milliarde Menschen in Jodmangelgebieten. Etwa 200 Millionen Menschen leiden an einer durch Jodmangel bedingten Struma. Weil früher die Struma in diesen Jodmangelgebieten so häufig vorkam, spricht man auch von einer endemischen Struma. Etwa 20 Millionen Menschen, die in Gebieten mit ausgeprägtem Jodmangel leben, leiden unter den Folgen eines angeborenen Jodmangels (Kretinismus).
In Deutschland weisen mehr als 30 Prozent der Erwachsenen eine Schilddrüsenvergrößerung oder Schilddrüsenknoten auf. Das früher angenommene Nord-Süd-Gefälle in der Häufigkeit hat sich nicht bestätigt. Ebenfalls entgegen früheren Annahmen gibt es keine wesentlichen Unterschiede in der Häufigkeit zwischen Männern und Frauen. In der Schweiz ist die Prävalenz der Jodmangelstruma deutlich gesunken, da dort wegen der jodarmen Böden das Speisesalz seit 1922 mit Jod angereichert wird.
Entstehung der Jodmangelstruma
Die Vorstellungen zur Pathogenese der Struma haben sich in den letzten Jahrzehnten geändert. Bis in die Mitte der 1980er Jahre ging man davon aus, dass Jodmangel zu einer leichten Hypothyreose führe und dass nachfolgend die Hirnanhangsdrüse (Hypophyse) die Produktion des Hormons TSH erhöht, um die Schilddrüse zum Wachstum, zur Jodaufnahme und zur Schilddrüsenhormonproduktion zu stimulieren. Experimentelle Arbeiten an kultivierten Schilddrüsenzellen haben aber gezeigt, dass ein erhöhter TSH-Spiegel nur dann zur Proliferation der Schilddrüsenzellen (Thyreozyten) führt, wenn gleichzeitig innerhalb der Zellen ein Jodmangelzustand herrscht.
Heute können folgende Mechanismen als gesichert gelten: Jodarmes Schilddrüsengewebe setzt bestimmte Wachstumsfaktoren frei (den IGF, den EGF, den TNF-α und den FGF), die auf die freisetzende Zellen selbst und ihr benachbartes Gewebe wirken (autokrine und parakrine Sekretion). Diese Faktoren führen zu einer Zellvermehrung (Hyperplasie) der Schilddrüsenfollikel, sowie zur Vermehrung bestimmter Bindegewebszellen (Fibroblasten) und zum Einsprießen von Blutgefäßen. Ausreichend mit Jod versorgte Thyreozyten produzieren hingegen die wachstumshemmenden Faktoren TGF-b und Jod-Lactone. Das TSH fördert zusätzlich das Wachstum der einzelnen Thyreozyten (Hypertrophie), ändert die Wirkung der einzelnen Wachstumsfaktoren aber durchaus in verschiedene Richtungen.
Diese Vorgänge sind zunächst nicht krankhaft, sondern dienen der normalen (physiologischen) Anpassung der Schilddrüse an Phasen eines relativen Jodmangels. Bei jahrelangem Jodmangel kommt es aber zu zusätzlichen degenerativen Veränderungen der Schilddrüse, in deren Verlauf knotige Veränderungen auftreten, sowie zur Bildung autonomer Areale, die sich vom Regelkreis zwischen Hypophyse und Schilddrüse abgekoppelt haben. Sie reagieren also nicht mehr auf die Steuerungsversuche des TSH.
Beschwerdebild
Das klinische Bild eines Struma-Patienten hängt vor allem von der Größe der Schilddrüse und von der Stoffwechsellage ab.
Eine geringe Vergrößerung der Schilddrüse macht meist keine lokalen Beschwerden. Mit zunehmender Größe der Schilddrüse klagen aber immer mehr Patienten über ein Druck-, Enge- oder Kloßgefühl, Missempfindungen beim Tragen enger Kragen, Schluckbeschwerden, Luftnot bei Belastung, Luftnot abhängig von der Position des Kopfes, sowie eine Neigung zu Bronchitiden. Eine drittgradige Struma kann benachbarte Strukturen (Luftröhre, Halsgefäße, Speiseröhre) mechanisch verdrängen und zu entsprechenden Symptomen führen, wie ausgeprägten Schluckbeschwerden oder Luftnot (eventuell schon in Ruhe) sowie Stridor.
Sollte eine stoffwechselbestimmende Schilddrüsenautonomie entstanden sein, klagen die Patienten oft über Beschwerden im Sinne einer Hyperthyreose (siehe dort). Insbesondere nach exzessiven Jodgaben in Form von jodhaltigen Kontrastmitteln oder Amiodaron droht die Entwicklung einer thyreotoxischen Krise.
Untersuchungen
→ Hauptartikel: Untersuchung der Schilddrüse
Neben dem Abtasten (Palpation) des Halses dient vor allem der Ultraschall als diagnostische Methode, um eine Struma zu erkennen. Dabei kann die Ausdehnung der Schilddrüse in den drei Raumachsen gemessen und daraus das Volumen berechnet werden (Ellipsoid). Neuere Ultraschallgeräte liefern auch eine direkte 3D-Volumetrie der Schilddrüse. Die Schilddrüse hat bei der Frau ein normales Volumen von bis zu 18 ml, beim Mann bis zu 25 ml.
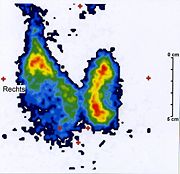
Zur weiteren Abklärung bestimmt man im Labor die Schilddrüsenhormone T3 und T4, das Thyreotropin (TSH) und eventuell Autoantikörper (TRAK, TPO-AK). Bei Knoten folgen die Schilddrüsenszintigrafie mit 99mTc und bei Verdacht auf ein Schilddrüsenkarzinom gegebenenfalls eine zytopathologische Untersuchung nach Feinnadelbiopsie. Ein Jodmangel lässt sich durch die Messung der Jodausscheidung im Sammelurin oder einfacher durch eine erhöhte Aufnahme des Tracers im Szintigramm nachweisen.
Die Röntgen-Zielaufnahme der Luftröhre und der Speiseröhre (gegebenenfalls mit Kontrastmittel) wurden weitgehend durch die Ultraschalluntersuchung verdrängt. Bei einem Strumawachstum bis in den Brustkorb hinein wird gelegentlich eine Computertomografie (CT) oder eine Kernspintomografie (MRI) notwendig, bei einer dystopen Schilddrüse (abweichende Lage) selten ein Szintigramm mit 123I.
Falls eine Operation geplant ist, erfolgt zudem eine Vorstellung beim Hals-Nasen-Ohren-Arzt, um bereits bestehende Störungen der Stimmbandbeweglichkeit oder eine Rekurrensparese (Lähmung des Stimmbandnerven, Nervus recurrens) auszuschließen.
Behandlung
Zur Behandlung (Therapie) der Struma stehen folgende Therapieformen zur Verfügung: medikamentöse Therapie, Operation und Radiojodtherapie.
Medikamentöse Therapie
Entsprechend den Vorstellungen zu Pathogenese (siehe Entstehung der Jodmangelstruma) bestand die medikamentöse Behandlung der Struma bis vor wenigen Jahren in einer Gabe von Schilddrüsenhormonen in einer Dosierung, die über den thyreotropen Regelkreis zu einer Erniedrigung des TSH-Wertes unterhalb den Normbereich führte (TSH-Suppression). Damit hat man für den Patienten aber die negativen Folgen einer latenten Hyperthyreose erkauft, insbesondere die erhöhte Wahrscheinlichkeit für das Auftreten bestimmter Herzrhythmusstörungen (Vorhofflimmern) und dem Verlust an Knochenmasse (Osteoporose).
Bei der Struma diffusa, sowie der Struma nodosa ohne relevante Autonomie und ohne Karzinomverdacht besteht die Standardtherapie heute aus der Gabe von Jodid oder L-Thyroxin je nach Hormonlage und Begleiterkrankungen [5]. Kombinationspräparate aus beiden Substanzen werden ebenfalls eingesetzt, da beide Substanzen synergistisch auf Hypertrophie und Hyperplasie der Schilddrüse wirken. Ziel ist es, das Entstehen neuer Knoten zu verhindern, weiteres Wachstum eventuell vorhandener Knoten zu verhindern, und das nicht-knotige Gewebe zu verkleinern. Die gleiche Behandlung erfolgt zur Vorbeugung (Prophylaxe) einer Rezidiv-Struma nach Strumaresektion und bei latenter oder manifester Hypothyreose nach OP oder Radiojodtherapie.
Die tägliche Dosis des Jodids beträgt meist 100 bis 200 µg. Die Menge des verabreichten L-Thyroxins orientiert sich am TSH-Wert, der im unteren Normbereich liegen, aber nicht supprimiert sein soll. Die Behandlungsdauer beträgt meist 12 bis 18 Monate, dann kann oft auf eine Therapie mit Jodid allein umgestellt werden. Bei Hypothyreose erfolgt die Therapie grundsätzlich lebenslang, nach Schilddrüsen-Operation meist ebenfalls lebenslang.
Absolute Kontraindikationen zur medikamentösen Therapie sind eine vorbestehende latente oder manifeste Hyperthyreose wegen der Gefahr einer thyreotoxischen Krise sowie der Verdacht auf ein Schilddrüsenkarzinom. Relative Kontraindikationen sind eine bestehende Autonomie bei normaler Stoffwechsellage (Euthyreose) oder die Entwicklung einer latenten Hyperthyreose unter der Therapie. Beim Vorliegen einer Autoimmunthyreoiditis wird allein mit L-Thyroxin behandelt. Als Nebenwirkungen werden eine Hyperthyreose bei zu hoher Dosierung des L-Thyroxins und neu auftretende oder sich verschlimmernde Akne beschrieben.
Operative Therapie
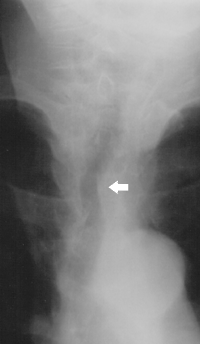 Indikation zur Operation: ausgeprägte Struma nodosa mit Einengung der Luftröhre und dadurch bedingter Verengung der Luftwege (Stridor).
Indikation zur Operation: ausgeprägte Struma nodosa mit Einengung der Luftröhre und dadurch bedingter Verengung der Luftwege (Stridor).Die Operation der Schilddrüse ist absolut indiziert bei konkretem Verdacht auf ein Schilddrüsenkarzinom sowie bei mechanischer Beeinträchtigung benachbarter Strukturen (Einengung der Luftröhre über 50 %, Tracheomalazie, Einengung oder Verlagerung der Speiseröhre, obere Einflussstauung). Eine relative Indikation besteht bei Wachstumstendenz der Schilddrüse trotz medikamentöser Therapie, kalten Knoten ohne konkreten Malignomverdacht und dystopem Schilddrüsengewebe, sowie aus kosmetischen Gründen.[6]
Die Schilddrüsenoperation wird in der Regel durchgeführt als:
- Strumaresektion (Teilentfernung der Schilddrüse) bei jeder gutartigen (benignen) Knotenstruma
- Thyreoidektomie (vollständige Entfernung aller sichtbaren Anteile der Schilddrüse) bei vorbekanntem oder intraoperativ gesichert bösartigem Tumor (Malignom)
- Hemithyreoidektomie (vollständige Entfernung aller sichtbaren Anteile eines Schilddrüsenlappens) bei einseitig vorliegenden (multiplen oder solitärem) Schilddrüsenknoten mit gesunder Gegenseite
Seltene, aber typische Komplikationen aller Schilddrüsenoperationen sind die Schädigung des Stimmbandnervs (Rekurrensparese) und eine postoperative Unterfunktion der Nebenschilddrüsen (Hypoparathyreoidismus). Das Risiko für diese Komplikationen ist bei einem Zweit-Eingriff und bei Operationen bösartiger Tumoren der Schilddrüse höher. Durch den Einsatz spezieller Geräte zur intraoperativen Darstellung des Nervus laryngeus recurrens (Neuromonitoring) kann die Häufigkeit der Stimmbandnerven-Lähmung bei allen Schilddrüsen-Operationen deutlich vermindert werden und liegt in der Hand des erfahrenen Chirurgen bei unter 1 %. Sehr selten treten Nachblutungen, Schädigungen des Nervus laryngeus superior und Wundinfektionen nach einer Schilddrüsenoperation auf.
Die verschiedenen Schilddrüsen-Operationen beseitigen nicht die Ursache der Strumabildung, sondern verstärken im Gegenteil durch die Verminderung der körpereigenen Möglichkeiten zur Bereitstellung von Schilddrüsenhormonen noch die Wachstumsreize auf das Restgewebe der Schilddrüse. Daher wird als Vorbeugung (Prophylaxe) eines erneuten Schilddrüsenwachstums und einer erneuten Knotenbildung nach der Operation eine meist lebenslange Kombinationsbehandlung mit Jodid und L-Thyroxin gefordert (Siehe Medikamentöse Therapie).
Radiojodtherapie
→ Hauptartikel: Radiojodtherapie
Die Radiojodtherapie ist ein wirksames Verfahren zur Verkleinerung der Schilddrüse und zur Ausschaltung autonomer Areale sowie zur Behandlung der Basedow-Krankheit. Außerdem wird sie bei der Behandlung der Struma maligna nach zuvor erfolgter Operation eingesetzt. Sie spielt zur Behandlung der gutartigen Struma mit normaler Funktion (blande Struma) eine untergeordnete Rolle, kommt aber zum Einsatz, wenn eine Operation nicht gewollt oder nicht möglich ist.
Vorbeugung
Zur allgemeinen Vorbeugung (Prophylaxe) der Schilddrüsenvergrößerung werden in zahlreichen Ländern das Speisesalz sowie zunehmend auch weitere Lebensmittel und bestimmte Sorten an Futtermittel für verschiedene Nutztiere mit Jod angereichert. Dadurch ist die Jodversorgung der Bevölkerung in den betroffenen Ländern deutlich besser geworden und die Häufigkeit der Struma ist vor allem bei Kindern und Jugendlichen stark zurückgegangen.
Eine Häufung von Autoimmunerkrankungen der Schilddrüse durch das erhöhte Jodangebot wird diskutiert. So finden sich nach Einnahme von mehr als 500 µg Jod pro Tag über ein Jahr zwar gehäuft Schilddrüsen-Autoantikörper im Blut, aber nicht gehäuft eine Hypothyreose.[7] Das Bundesinstitut für Risikobewertung (BfR) „sieht kein erhöhtes Risiko für die Verschlimmerung von Schilddrüsen-Erkrankungen oder gar für die Auslösung von Folgeerkrankungen durch die derzeitige Praxis der Verwendung von Jodsalz im Haushalt, in der Gemeinschaftsverpflegung und insbesondere auch bei der Herstellung von Back- und Fleischwaren. Dies gilt auch für den Verzehr von jodhaltigen tierischen Lebensmitteln wie Milch, Käse, Eier oder Fleisch infolge der Jodierung von Futtermitteln.“[8]
Eine Indikation zu einer darüberhinausgehenden Gabe von Jodid (in Tablettenform) besteht bei Personen, in deren Familien bereits zu einem früheren Zeitpunkt eine Struma aufgetreten war (positive Familienanamnese), während Schwangerschaft und Stillzeit sowie nach Abschluss einer medikamentösen Therapie. Für Kleinkinder und Kinder bis 10 Jahre werden 100 µg/Tag empfohlen, für Kinder über 10 Jahre und Erwachsene 150 bis 250 µg/Tag.
Medizingeschichte
Älteste Hinweise auf Kropfleiden sind über 4000 Jahre alt und finden sich in China, Indien und Ägypten. In Mitteleuropa war schon früh bekannt, dass es regionale Unterschiede in der Häufigkeit gab. So beschrieb Vitruv bereits um das Jahr 16 n. Chr. das Vorkommen von Kröpfen bei den Bewohnern der Alpen und der Sabiner Berge. Er vermutete die Ursache im Wasser.
Der Chinese Sun Si Miao hat bereits im 7. Jahrhundert n. Chr. Strumatherapien mit Arzneien aus tierischen Schilddrüsen durchgeführt. Diese sollen der Quellenlage zufolge zu einer Verkleinerung der Struma geführt haben. [9]
1791 führte Pierre-Joseph Desault als vermutlich erster Arzt die operative Entfernung eines vergrößerten Schilddrüsenlappens durch. Erste systematische Untersuchungen zur regionalen Verteilung der Struma gab es 1845 im Königreich Sardinien. Erste Therapieversuche mit Jod führte 1820 Jean-Francois Coindet (1774–1834) in der Schweiz durch. Ab 1850 wurden in Frankreich Jodgaben zur Prophylaxe (Vorbeugung) versucht. Aufgrund einer viel zu hohen Dosierung gab es aber zum Teil tödlich endende Therapieverläufe. In den 1850er Jahren hielt Louis Pasteur den Kropf für eine Infektionskrankheit. Moritz Schiff führte 1880 Versuche mit Schilddrüsenextrakten von Schafen durch. 1901 behandelte Philipp Schech Kropfpatienten mit „Thyrojodin“, Schilddrüsensubstanzen von Hammel oder Schwein.
1922 wurde im Kanton Appenzell Ausserrhoden in der Schweiz das Jodsalz eingeführt, 1924 in den USA. 1976 wurde auch in der Bundesrepublik Deutschland Jodsalz eingeführt, wobei dieses bis 1981 mit dem Warnhinweis „Nur bei ärztlich festgestelltem Jodmangel zu verwenden“ versehen war. Ab 1983 wurde in der DDR das Speisesalz flächendeckend jodiert. Übergangsregelungen für die neuen Bundesländer galten bis 1991.
Kulturelle Aspekte
Zu früheren Zeiten dachte man, die Ursache eines Kropfes läge in erlittenem Ärger und dem damit verbundenen Anhalten des Atems. Aus dieser Vorstellung resultieren verschiedene Redensarten. Sich den Kropf leeren bedeutet seine Meinung sagen, allen Ärger ablassen. Etwas ist überflüssig wie ein Kropf weist auf den hinderlichen Charakter einer Sache hin.[10]
Das Kropfband ist als Schmuckstück Teil der bayerischen und österreichischen Tracht. Seinen Ursprung soll das Kropfband im Salzburger Land haben. Der dortige Jodmangel führte seit Jahrhunderten gehäuft zur Vergrößerung der Schilddrüse. Mindestens seit dem 19. Jahrhundert wurden von den Frauen zu festlichen Anlässen Kropfbänder getragen, die entweder den Kropf selbst oder aber die Narben nach einer Kropf-Operation verdecken sollten.[11]
Weiterführende Informationen und Belege
Literatur
- Lothar-Andreas Hotze, Petra-Maria Schumm-Draeger. Schilddrüsenkrankheiten. Diagnose und Therapie. Berlin 2003 ISBN 3-88040-002-4
- Wieland Meng. Schilddrüsenerkrankungen. Jena 1992 ISBN 3-334-60392-X
- Thorsten Kuwert. Schilddrüse. in: Thorsten Kuwert, Frank Grünwald, Uwe Haberkorn, Thomas Krause (Hrsg.) Nuklearmedizin. Stuttgart 2008 ISBN 978-3-13-118504-4
- J. Larry Jameson, Anthony P. Weetman (für die deutsche Ausgabe: Jens Zimmermann und George Kahaly). Erkrankungen der Schilddrüse. In: Manfred Dietel, Joachim Dudenhausen, Norbert Suttorp (Hrsg.) Harrisons Innere Medizin. Berlin 2003 ISBN 3-936072-10-8
Einzelnachweise
- ↑ Ursus-Nikolaus Riede, Martin Werner, Hans-Eckart Schäfer (Hrsg.): Allgemeine und spezielle Pathologie. Thieme, Stuttgart 2004. S.1014. ISBN 3-13-683305-8
- ↑ Lothar-Andreas Hotze, Petra-Maria Schumm-Draeger. Schilddrüsenkrankheiten. Diagnose und Therapie. Berlin 2003 ISBN 3-88040-002-4 S. 152
- ↑ Leitlinien der Deutschen Gesellschaft für Kinderchirurgie: Struma
- ↑ R. Hörmann: Schilddrüsenkrankheiten. ABW-Wissenschaftsverlag, 4. Auflage 2005, Seite 15-37. ISBN 3-936-07227-2
- ↑ Grußendorf M: Strumatherapie in der hausärztlichen Praxis. Seminar HausarztPraxis 1/06
- ↑ Medizin-Netz.de
- ↑ R. Gärtner. Hat Jod einen Einfluss auf die Entstehung und den Verlauf einer Haschimoto-Thyreoiditis? Jodversorgung aktuell 2007
- ↑ Bundesinstitut für Risikobewertung
- ↑ Cheng-Tsai Liu, Liu Zheng-cai, Ka Hua: A Study of Daoist Acupuncture & Moxibustion, 1999, S. 20-21, ISBN 189184508X
- ↑ Lutz Röhrich. Lexikon der sprichwörtlichen Redensarten. Freiburg 2006 ISBN 978-3451054006
- ↑ Kropfband bei planet-wissen.de
Weblinks
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Untersuchung der Schilddrüse — Die Untersuchung der Schilddrüse des Menschen umfasst je nach Anlass und Fragestellung sowie je nach durchführender Fachdisziplin (Allgemeinmediziner, allgemeiner Internist, Endokrinologe, Radiologe oder Nuklearmediziner) verschiedene… … Deutsch Wikipedia
Branchiogene Fistel — Klassifikation nach ICD 10 Q18.1 Laterale Halsfistel / Halszyste Q18.8 Mediane Halsfistel / Halszyste … Deutsch Wikipedia
Glandula thyroidea — Schilddrüse und Nebenschilddrüsen beim Menschen Die Schilddrüse (lat. Glandula thyr(e)oidea) ist eine Hormondrüse bei den Wirbeltieren. Sie befindet sich bei Säugetieren am Hals unterhalb des Kehlkopfes vor der Luftröhre. Beim Menschen hat sie… … Deutsch Wikipedia
Halsfistel — Klassifikation nach ICD 10 Q18.1 Laterale Halsfistel / Halszyste Q18.8 Mediane Halsfistel / Halszyste … Deutsch Wikipedia
Halszyste — Klassifikation nach ICD 10 Q18.1 Laterale Halsfistel / Halszyste Q18.8 Mediane Halsfistel / Halszyste … Deutsch Wikipedia
Schilddrüse — und Nebenschilddrüsen beim Menschen Die Schilddrüse (lat. Glandula thyr(e)oidea) ist eine Hormondrüse bei den Wirbeltieren. Sie befindet sich bei Säugetieren am Hals unterhalb des Kehlkopfes vor der Luftröhre. Beim Menschen hat sie die … Deutsch Wikipedia
Schilddrüsendiagnostik — Die Untersuchung der Schilddrüse des Menschen umfasst je nach Anlass und Fragestellung sowie je nach durchführender Fachdisziplin (Allgemeinmediziner, allgemeiner Internist, Endokrinologe, Radiologe oder Nuklearmediziner) verschiedene… … Deutsch Wikipedia
Thyroid — Schilddrüse und Nebenschilddrüsen beim Menschen Die Schilddrüse (lat. Glandula thyr(e)oidea) ist eine Hormondrüse bei den Wirbeltieren. Sie befindet sich bei Säugetieren am Hals unterhalb des Kehlkopfes vor der Luftröhre. Beim Menschen hat sie… … Deutsch Wikipedia
Thyroidea — Schilddrüse und Nebenschilddrüsen beim Menschen Die Schilddrüse (lat. Glandula thyr(e)oidea) ist eine Hormondrüse bei den Wirbeltieren. Sie befindet sich bei Säugetieren am Hals unterhalb des Kehlkopfes vor der Luftröhre. Beim Menschen hat sie… … Deutsch Wikipedia