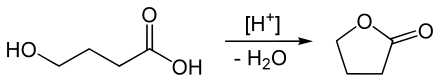- Butyro-1,4-lacton
-
Strukturformel 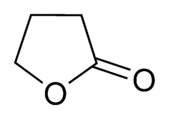
Allgemeines Name Butyro-1,4-lacton Andere Namen - γ-Butyrolacton
- Dihydrofuran-2-on
- 1-Oxa-cyclopentan-2-on
- 4-Butanolid
Summenformel C4H6O2 CAS-Nummer 96-48-0 PubChem 7302 DrugBank DB04699 Kurzbeschreibung farblose Flüssigkeit[1]
Eigenschaften Molare Masse 86,09 g·mol−1 Aggregatzustand flüssig
Dichte 1,13 g·cm−3[1]
Schmelzpunkt Siedepunkt 204–206 °C[1]
Dampfdruck Löslichkeit vollständig mischbar mit Wasser und Ethanol[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] 

Gefahr
H- und P-Sätze H: 302-318 EUH: keine EUH-Sätze P: 280-305+351+338-313 [2] EU-Gefahrstoffkennzeichnung [2] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22-36 S: 26-36 LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Butyro-1,4-lacton, veraltet auch γ-Butyrolacton (GBL) genannt, ist das Lacton der γ-Hydroxybuttersäure (GHB) und wird hauptsächlich als Lösungsmittel in der Industrie und als Ausgangsstoff zur Herstellung von Pharmazeutika und Chemikalien eingesetzt. Daneben dient es als Vorläuferstoff des Betäubungsmittels GHB; in Europa und den USA wird die Abgabe von GBL daher durch das sogenannte Monitoring (Name für freiwillige Selbstkontrolle der Händler und Hersteller) überwacht.
Inhaltsverzeichnis
Vorkommen
In der Natur kommt GBL in Spuren z. B. als Umbauprodukt des natürlichen GHB und auch in Wein vor.[4] Es wird industriell aus Bernsteinsäure oder BDO synthetisiert.
Gewinnung
Bei der Synthese von GBL wird zuerst Maleinsäure zu Bernsteinsäure umgesetzt, aus der GBL synthetisiert werden kann.[5] Die jährlich in Deutschland verbrauchte Menge GBL beträgt über 1000 Tonnen, da GBL als Ausgangsstoff für viele andere Produkte dient (siehe Verwendung).
Darüber hinaus kann GBL auch durch eine innere Veresterung von γ-Hydroxybuttersäure in saurem Milieu synthetisiert werden. Umgekehrt wird γ-Hydroxybuttersäure durch die Verseifung von GBL in basischem Milieu hergestellt.
Eigenschaften
Physikalische Eigenschaften
GBL ist eine bei Raumtemperatur farblose Flüssigkeit mit schwachem Eigengeruch.
Die Schmelztemperatur von γ-Butyrolacton liegt bei −43,5 °C, der Siedepunkt bei 206 °C. Zusammen mit Wasserdampf ist GBL flüchtig bei Temperaturen, die unter dem eigentlichen Siedepunkt von GBL liegen. Der Flammpunkt und die Zündtemperatur liegen bei 100 beziehungsweise 455 °C. Die Dichte von GBL beträgt 1,128 g/cm³.
Löslich ist γ-Butyrolacton in jedem Verhältnis mit Wasser, Methanol, Ethanol, Aceton, Ether, Dichlormethan, Toluol und Propylenglycol. Allerdings ist die Löslichkeit von GBL in aliphatischen Kohlenwasserstoffen stark begrenzt.
Die Viskosität von GBL ist relativ gering und mit Wasser vergleichbar.
Chemische Eigenschaften
GBL reagiert durch partielle Hydrolyse zu 4-Hydroxybuttersäure in Wasser leicht sauer. Die Substanz wird durch wässrige Alkalien quantitativ hydrolysiert. Wasserfreie Basen können ein Proton am C2-Atom abstrahieren (C-H-acide Verbindung, Bildung des Enolats), das dadurch einem nukleophilen Angriff zugänglich wird.
GBL ist wie Ethylacetat oder Aceton ein polar aprotisches Lösungsmittel und löst viele Kunststoffe wie Polyester oder PMMA.
Verwendung
Industrie
GBL ist ein weit verbreitetes Lösungsmittel in der Industrie und wird auch als Farbentferner, Graffitientferner, Reinigungsmittel und Nagellackentferner verwendet. Es ist als Weichmacher in Weich-PVC-Folien enthalten.
Im November 2007 machte GBL Schlagzeilen als Bestandteil einer Knetmasse für Kinder. Durch Verschlucken der Knetmasse sind einzelne Kinder angeblich „in ein Koma“ gefallen, d. h., sie bekamen die Wirkung von GBL als Schlafmittel zu spüren.
Darüber hinaus dient GBL auch als Ausgangsstoff zur Herstellung von Pharmazeutika und Chemikalien für die Landwirtschaft.
Für die chemische Industrie ist GBL unersetzlich, was der wesentliche Grund dafür ist, dass es im Gegensatz zu GHB nicht als illegales Betäubungsmittel eingestuft wird. GBL findet seit dem Verbot von GHB auch als Droge Verwendung und dient zudem als Grundstoff für die Herstellung von GHB.
Droge
GBL hat einen salzig und seifen-artigen Geschmack. In geringen Mengen bewirkt GBL bei oraler Aufnahme einen Rausch, der partiell dem Alkoholrausch ähnelt. Weitere mögliche Wirkungen sind Euphorie, Schwindel, Übelkeit, Somnolenz, Mydriasis, angstlösend, antidepressiv, sexuell stimulierend, starke Entspannung der Muskeln, intensiverer Wahrnehmung der Umgebung, gesteigertes Mitteilungsbedürfnis, Bewegungsdrang und manchmal auch Kopfschmerzen. Auch Herz-Kreislauf-Probleme können sich ergeben, da GBL auf die Katecholamin-Rezeptoren im Gehirn wirkt [6]. Höhere Dosen führen zu einem narkotischen Zustandsbild. Das zu GHB metabolisierte GBL wirkt also als Schlafmittel oder Narkotikum. In geringeren Dosierungen hat es jedoch eine aufputschende Wirkung. Das hängt damit zusammen, dass mit der Aktivierung des GHB-Rezeptors Glutamat freigesetzt wird, der wichtigste erregende Neurotransmitter [7]. In größeren Mengen bewirkt es eine Aktivierung des GABAB-Rezeptors, der zu der sedativen Wirkung führt.[8] Die Wirkung von GHB auf die Dopaminfreisetzung ist zweiphasig: Niedrige Konzentrationen stimulieren die Dopaminfreisetzung über den GHB-Rezeptor [9] und höhere hemmen die Freisetzung über den GABAB-Rezeptor.[10]. Sowohl die Hemmung als auch die Ausschüttung von Dopamin wird durch Opioid-Antagonisten wie Naloxon und Naltrexon verhindert.[11] GBL kann auch je nach Dosis wie ein Neuroleptikum wirken, weil, wie eben erwähnt, durch Aktivierung der GABAB-Rezeptoren die Dopaminausschüttung gehemmt wird, was dem Haupt-Wirkmechanismus von Neuroleptika entspricht.[12][13]
GBL kann bei chronischem Abusus zu einer körperlichen und psychischen Abhängigkeit führen. Todesfälle durch Monokonsum von GBL sind bisher nur vereinzelt bei extremen Überdosierungen und bei Behandlungsfehlern vorgekommen. Besonders gefährlich ist jedoch der Mischkonsum mit zentral dämpfend wirkenden Drogen, z. B. Alkohol oder Heroin.
In Kombination mit Alkohol oder atemdepressiv wirkenden Medikamenten (z. B. Benzodiazepinen) kann es zu Übelkeit und Erbrechen kommen, was durch die narkotisierende Eigenschaft der Droge zum Erstickungstod führen kann.[14] Außerdem kann eine lebensbedrohliche Atemdepression und Bradykardie auftreten.[6]
Nach einem von GBL induzierten Schlaf wacht man nach einigen Stunden plötzlich auf, weil mit der Zeit die Konzentration von GHB unter die Schwelle der Aktivierung der GABAB-Rezeptoren sinkt und wieder in erster Linie die GHB-Rezeptoren aktiviert werden, was einen stimulierenden Effekt zur Folge hat. Wegen der einschläfernden Wirkung wird der Zustand der betroffenen Person von Sanitätern und Helfern oft falsch eingeschätzt. Meist wird eine Überdosierung von Benzodiazepinen vermutet, so dass oft eine intensivmedizinische symptomatische Behandlung (unter Umständen auch die zusätzliche Gabe von Flumazenil) vorgenommen wird. Durch den stimulierenden Effekt der GABAB-Rezeptoren wird GBL u. a. von machen Leistungssportlern und Bodybuildern als Alternative zu anabolen Steroiden als Doping-Mittel eingesetzt. Durch die Stimulierung der GABA-Rezeptoren werden die Wachstumshormone sowie der Fettstoffwechsel angeregt. Auch soll der von GBL induzierte Schlaf die Muskulatur von ihrer Beanspruchung wesentlich schneller regenerieren lassen.
Nach der oralen Einnahme setzt die Wirkung von GBL innerhalb von 5-20 Minuten ein. Dabei wird GBL komplett zu GHB hydrolysiert. Die maximale Plasmakonzentration ist innerhalb von 20-45 Minuten erreicht. Die Rauschdauer hält in der Regel zwei bis max. vier Stunden an.
GHB hat im Vergleich zu anderen Drogen wie z. B. Alkohol, Amphetamin oder Tetrahydrocannabinol eine sehr kurze Halbwertszeit. Aufgrund dieser sehr geringen Halbwertzeit ist GHB nur maximal zwölf Stunden im Urin nachweisbar. Die nötige aufwendige Messung erfolgt dabei nur in Speziallaboratorien per GC-MS (Kopplung eines Gaschromatographen (GC) mit einem Massenspektrometer (MS)).
 Stoffwechselweg von GHB, GBL und 1,4-Butandiol.
Stoffwechselweg von GHB, GBL und 1,4-Butandiol.
Pharmakokinetik
GBL wird im Blut durch die 1,4-Lactonase zu GHB hydrolysiert. GBL wird nach oraler Einnahme schneller resorbiert als GHB, so dass der Plasmaspiegel von GHB bei der Einnahme von GBL schneller ansteigt als bei Einnahme von GHB selbst. Die Plasmahalbwertszeit von GBL beträgt auf Grund rascher Metabolisierung zu GHB weniger als 60 s, das heißt, fünf Minuten nach der Einnahme von GBL sind im Körper noch etwa 3 % des Gamma-Butyrolactons vorhanden. Primär wird GHB durch Alkoholdehydrogenase (ADH)/Aldehyddehydrogenasen (ALDH) im Körper zu Bernsteinsäure metabolisiert, die ihrerseits in den Citratzyklus übergeht. Als Abbauprodukte bleiben letztlich nur Kohlenstoffdioxid und Wasser übrig. Zu geringen Teilen entstehen auch Metabolite durch β-Oxidation, welche renal ausgeschieden werden.
Schäden durch Dauerkonsum
Bei unverdünntem Konsum werden die Magenschleimhaut, die Speiseröhre und Dick- und Dünndarmzellen angegriffen und die Wundheilung ist verzögert. Unverdünntes GBL löst Calcium aus dem Zahnschmelz.
Eine weitere Gefahr stellen Verunreinigungen dar, die in dem zumeist konsumierten nicht analysenreinen Industrie-GBL enthalten sein können.
Beim Absetzen von GBL nach langfristigem, meist täglichen Gebrauch (zwei bis drei Wochen) stellen sich Entzugsbeschwerden ein, welche qualitativ denen bei Benzodiazepinen gleichen, jedoch in Intensität und Dauer (zwölf bis 96 Stunden) nicht das Ausmaß erreichen. Physisch können Charakteristisch folgende Symptome auftreten: Enormes Schwitzen, Muskelzittern,psychomotorische Unruhe bis hin zu epileptische Anfällen, begleitet mit anderen Symptomen wie zum Beispiel Durchfall oder Übelkeit. Psychisch kann es zu Schlaflosigkeit die bei entsprechender Prädisposition von akuten psychotischen Symptomen (Wahnvorstellungen, Halluzinationen, Depersonalisierung, Derealisation, teils auch Dissoziation) begleitet werden. Je nach Intensität erfordern diese Symptome klinische Hilfe.
Toxizität
Die Toxizität von GBL wurde auf Grund seiner vielfältigen Verwendung in der chemischen Industrie, unter anderem auch bei der Produktion von Lebensmitteln, recht eingehend erforscht. Tierversuche haben ergeben, dass GBL innerhalb weniger Minuten zu GHB metabolisiert wird und binnen zwei bis drei Stunden als CO2 mit der Atemluft wieder ausgeschieden wird. LD50-Werte bei einmaliger Verabreichung von GBL für Mäuse liegen im Bereich zwischen 0,5 und 1,8 g pro Kilogramm Körpergewicht. Mehrmonatige Verabreichungen an Tiere in kleineren Dosierungen sind schadlos überstanden worden. Männliche Ratten, denen über Monate GBL verabreicht wurde, hatten eine höhere Lebenserwartung im Vergleich zur Kontrollgruppe.[15] GBL ist weder gentoxisch noch krebserregend.
Sicherheitshinweise
GBL ist eine schleimhautreizende, gesundheitsschädliche Substanz. Daher müssen beim Arbeiten mit GBL eine Schutzbrille und Schutzhandschuhe getragen werden. Mit GBL verunreinigte Kleidung muss sofort entfernt werden. Zudem muss beim Arbeiten mit GBL für eine gute Belüftung gesorgt werden. Nach Hautkontakt müssen betroffene Stellen mit Seife und Wasser gründlich abgewaschen werden. Nach Augenkontakt muss das betroffene Auge mindestens 15 Minuten mit fließendem Wasser gespült werden und anschließend ein Augenarzt aufgesucht werden. Wird GBL versehentlich verschluckt, muss der Mund sofort mit Wasser gespült und reichlich Wasser nachgetrunken werden.
Brennendes GBL kann mit Wasser, Trockenlöschmitteln, Schaum und Kohlenstoffdioxid gelöscht werden, wobei Chemikalienschutzkleidung getragen werden muss. Kontaminiertes Löschwasser muss getrennt gesammelt werden und darf nicht in die Kanalisation gelangen.
GBL muss an einem gut belüfteten Ort und getrennt von Alkalien und basenbildenden Substanzen gelagert werden.
Rechtliche Situation
GBL ist nicht im Betäubungsmittelgesetz aufgeführt, doch wird die Abgabe in Europa größtenteils durch die Vertreiber überwacht (Monitoring). Der Besitz ist nicht strafbar, ist aber durch das Chemikaliengesetz und die GefStoffV geregelt. Strafbar ist der Missbrauch von GBL zur Synthese von GHB sowie die zweckentfremdete Abgabe / Verkauf zum Konsum (Arzneimittelgesetz).[16] In den letzten Jahren war auf Grund des Verbotes von GHB ein Anstieg des GBL-Konsums zu beobachten.
GBL fällt unter die Definition von § 2 Abs 1 des AMG, sobald es für die Anwendung an Mensch oder Tier bestimmt ist. Somit ist Herstellung und Verkauf einer Substanz nach dem AMG reguliert, unabhängig davon, in welcher Form die Substanz vorliegt, wenn sie in Bestimmung § 2 Abs 1 erfüllt.[17][18] Der Verkauf und die Herstellung von Arzneimitteln ohne Genehmigung ist strafbar nach ArzneimittelG § 2 Abs. 1 Nr. 5 a. F., § 2 Abs. 1 Nr. 2a n. F., § 5, § 95 Abs. 1 Nr. 1, StPO § 354a. Dies wurde in einem Urteil des Bundesgerichtshofs zu der frei verfügbaren Chemikalie GBL bestätigt, welche nach dem AMG als Arzneimittel eingestuft wird, sobald sie für den Konsum bzw. Gebrauch an Mensch oder Tier bestimmt ist.[19]'[20]
Einzelnachweise
- ↑ a b c d e f Datenblatt Butyro-1,4-lacton bei Merck, abgerufen am 19. Januar 2011.
- ↑ a b c Eintrag zu γ-Butyrolacton in der GESTIS-Stoffdatenbank des IFA, abgerufen am 21. Mai 2008 (JavaScript erforderlich).
- ↑ a b Butyro-1,4-lacton bei ChemIDplus.
- ↑ J. Vose, T. Tighe, M. Schwartz, E. Buel: Detection of gamma-butyrolactone (GBL) as a natural component in wine. In: Journal of Forensic Sciences. 46, Nr. 5, 2001, S. 1164–1167, PMID 11569560.
- ↑ Patent WO9935113.
- ↑ a b BG Chemie Toxikologische Bewertung Nr. 7 γ-Butyrolacton Ausgabe 11/00, redaktionelle Überarbeitung 01/05, ISSN 0937-4248.
- ↑ Castelli MP, Ferraro L, Mocci I, et al.: Selective gamma-hydroxybutyric acid receptor ligands increase extracellular glutamate in the hippocampus, but fail to activate G protein and to produce the sedative/hypnotic effect of gamma-hydroxybutyric acid. In: J. Neurochem.. 87, Nr. 3, November 2003, S. 722–32. doi:10.1046/j.1471-4159.2003.02037.x. PMID 14535954.
- ↑ Dimitrijevic N, Dzitoyeva S, Satta R, Imbesi M, Yildiz S, Manev H: Drosophila GABA(B) receptors are involved in behavioral effects of gamma-hydroxybutyric acid (GHB). In: Eur. J. Pharmacol.. 519, Nr. 3, September 2005, S. 246–52. doi:10.1016/j.ejphar.2005.07.016. PMID 16129424.
- ↑ Maitre M, Hechler V, Vayer P, et al.: A specific gamma-hydroxybutyrate receptor ligand possesses both antagonistic and anticonvulsant properties. In: J. Pharmacol. Exp. Ther.. 255, Nr. 2, November 1990, S. 657–63. PMID 2173754.
- ↑ Smolders I, De Klippel N, Sarre S, Ebinger G, Michotte Y: Tonic GABA-ergic modulation of striatal dopamine release studied by in vivo microdialysis in the freely moving rat. In: Eur. J. Pharmacol.. 284, Nr. 1-2, September 1995, S. 83–91. doi:10.1016/0014-2999(95)00369-V. PMID 8549640.
- ↑ Mamelak M: Gammahydroxybutyrate: an endogenous regulator of energy metabolism. In: Neurosci Biobehav Rev. 13, Nr. 4, 1989, S. 187–98. doi:10.1016/S0149-7634(89)80053-3. PMID 2691926.
- ↑ Dopamine selectively reduces GABAB transmission onto dopaminergic neurones by an unconventional presynaptic action.
- ↑ Bi-directional effects of GABA(B) receptor agonists on the mesolimbic dopamines.
- ↑ Hansjörg Lammers, Gammahydroxybuttersäure (GHB) in COmed 2004, 7, 1-3.
- ↑ NTP Study Reports TR-406 Toxicology and Carcinogenesis Studies of γ-Butyrolactone (CAS No. 96-48-0) in F344/N Rats and B6C3F1 Mice (Gavage Studies) oder Cognitive Enhancement Research Institute Discussion.
- ↑ Bundesgerichtshof, Urteil vom 8. Dezember 2009 - 1 StR 277/09.
- ↑ Erwin Deutsch, Hans-Dieter Lippert (Hrsg.): Kommentar zum Arzneimittelgesetz (AMG). Springer, 2010, S. 64–66 (Eingeschränkte Vorschau in der Google Buchsuche).
- ↑ [1] ArzneimittelG § 2 Abs. 1 Nr. 5 a. F., § 2 Abs. 1 Nr. 2a n. F., § 5, § 95 Abs. 1 Nr. 1
- ↑ [2]Strafrecht: Handel mit Gamma-Butyrolacton (GBL; liquid ecstasy) zu Konsumzwecken
- ↑ [3]BGH-Urteil vom 8. Dezember 2009 (Aktenzeichen: 1 StR 277/09), 'Das unerlaubte Inverkehrbringen von Gamma-Butyrolacton (GBL) zu Konsumzwecken ist nach dem Arzneimittelgesetz strafbar.'
Weblinks
- The Emergence of GHB Alternatives(GBL als GHB Alternative-engl.)
- The Commercial Chemistry of GHB (Zusammenhang GHB/GBL chemisch-engl.)
- Toxikologische Bewertung der BG Chemie
- Anfragen über GBL- u. GHB-Vergiftungen an das Toxzentrum der Schweiz
- Datenblatt der BASF

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- Gesundheitsschädlicher Stoff
- Butyrolacton
- Sedativum
- Synthetische Droge
- Narkotikum
Wikimedia Foundation.