- Kreuzbandriss
-
Klassifikation nach ICD-10 S83.50 Nicht näher bezeichnetes Kreuzband
Inkl.: Kreuzbandriss o.n.A.S83.53 Riss des vorderen Kreuzbandes
Inkl.: Partieller oder kompletter RissS83.54 Riss des hinteren Kreuzbandes
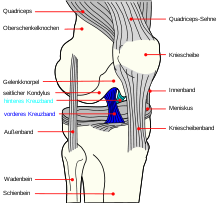
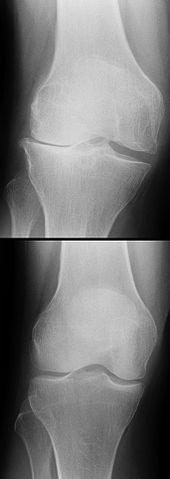
Inkl.: Partieller oder kompletter RissICD-10 online (WHO-Version 2011) Von einem Kreuzbandriss, auch Kreuzbandruptur genannt, spricht man bei einem unvollständigen (partiellen) oder vollständigen (kompletten) Riss (Ruptur) eines oder beider Kreuzbänder. In den meisten Fällen ist das vordere Kreuzband (Ligamentum cruciatum anterius) betroffen. Die Ursache für einen Kreuzbandriss ist das Überschreiten der Reißfestigkeit des Bandes.
Kreuzbandrisse entstehen meist ohne Fremdeinwirkung durch plötzliche Richtungswechsel beim Laufen oder Springen. Sie sind die häufigsten klinisch relevanten Verletzungen im Bereich des Kniegelenks. Kreuzbandrisse können anhand ihrer Symptome, der Beschreibung des Verletzungsvorgangs und mit Hilfe einfacher tastender (palpatorischer) Untersuchungen relativ sicher diagnostiziert werden. Magnetresonanztomografie und Arthroskopie können die Diagnosestellung weiter absichern. Nicht behandelte Kreuzbandrupturen können zu schweren degenerativen Schäden im Knie führen. Die Therapie kann sowohl konservativ als auch chirurgisch (minimalinvasiv mittels Arthroskopie) erfolgen. Welche Therapie, wann und in welcher Variante ausgeführt wird, ist Gegenstand kontroverser Diskussionen. Unbestritten ist dagegen, dass derzeit keine Therapieform qualitativ den ursprünglichen Zustand eines unverletzten Kreuzbandes wieder herstellen kann. Eine Langzeitfolge eines Kreuzbandrisses ist die deutlich erhöhte Wahrscheinlichkeit der Ausbildung einer Kniegelenksarthrose – unabhängig von der Art der Behandlung. Eine Vielzahl von Studien kommt zu dem Ergebnis, dass durch spezielle präventive Übungen das Risiko für einen Kreuzbandriss deutlich gesenkt werden kann.
In der anglo-amerikanischen Fachliteratur wird für Verletzungen des vorderen Kreuzbandes der Begriff anterior cruciate ligament injury verwendet. Kreuzbandriss wird korrekterweise mit cruciate ligament rupture übersetzt. Verletzungen des hinteren Kreuzbandes (Ligamentum cruciatum posterius) werden im Englischen als posterior cruciate ligament injury bezeichnet.
Arten von Kreuzbandrupturen
In den wenigsten Fällen sind Kreuzbandrisse isolierte Verletzungen. Die Rupturen werden meist von anderen Läsionen weiterer Bänder und der Menisken begleitet.[1] Es können zwei Arten von Kreuzbandrissen unterschieden werden:
- vorderer oder hinterer Kreuzbandriss mit sagittaler, das heißt von vorne nach hinten verlaufender, Instabilität und positivem Schubladenphänomen
- Kombinationsverletzung mit Schubladenphänomen in Drehstellung des Fußes nach innen oder außen:[2]
- anteromediale Rotationsinstabilität (AMRI, vorne-mittige Drehbewegungsinstabilität): vorderer Kreuzbandriss, Riss des Innenmeniskus und der mediodorsalen Kapsel, oft zusätzlich (meist zur Mitte zeigender) Riss des Innenbandes (so genannte Unhappy Triad).[3]
- anterolaterale Rotationsinstabilität (ALRI, vorne-seitliche Drehbewegungsinstabilität): Riss des hinteren Kreuzbandes, des Außenbandes und der dorsolateralen Kapsel.[4]
- posterolaterale Rotationsinstabilität (PLRI, hintere-seitliche Drehbewegungsinstabilität): Riss des Außenbandes und des hinteren Kreuzbandes bei hinterer-mittiger, beziehungsweise hinterer-seitlicher Drehbewegungsinstabilität.[5]
Verletzungsmechanismen
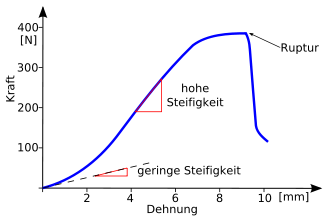 Typisches Kraft-Dehnungs-Diagramm eines menschlichen Kniebandes.[6]
Typisches Kraft-Dehnungs-Diagramm eines menschlichen Kniebandes.[6]
Bei geringer Belastung (=Kraft) verläuft die Kurve flach, da das Band ohne Zunahme der intraligamentären Kraft gedehnt wird (geringe Steifigkeit). Bei erhöhter Belastung nimmt die Steifigkeit des Bandes zu. Es stellt sich zunächst ein weitgehend linearer Anstieg ein (hohe Steifigkeit). In diesem Bereich verhalten sich die Kollagenfaserbündel des Bandes elastisch, da sie parallel ausgerichtet sind. Bei einer weiteren Krafteinwirkung finden irreversible Veränderungen im Band statt, so dass es nicht mehr zu seiner ursprünglichen Länge relaxieren kann. Nimmt die Kraft noch weiter zu, so zerreißen einzelne Faserbündel (die Kurve wird flacher). Da nicht alle Faserbündel der gleichen hohen Belastung ausgesetzt sind, kann selbst nach den ersten Rissen die Belastung weiter zunehmen (die Steifigkeit nimmt wieder ab). Ab einer bestimmten Maximalkraft zerreißt das Band schlagartig, was in einem plötzlichen Abfall der Kurve zu sehen ist.[7]Vorderes Kreuzband
Die Verletzung des vorderen Kreuzbands entsteht typischerweise durch einen Richtungswechsel. Häufig liegt eine Drehbewegungsstellung des Unterschenkels nach außen mit Valgusbeugungsstress oder eine Drehbewegungsstellung nach innen mit Varusbeugungsstress vor. Auch zu starke Streck- oder Beugebewegungen (Hyperextension beziehungsweise Hyperflexion) können ein Auslöser sein. In den überwiegenden Fällen handelt es sich um Sportverletzungen. Besonders häufig treten solche Verletzungen (Traumata) unter so genannten „Stop-and-Go“-Sportarten (z. B. Tennis oder Squash) und bei Mannschaftssportarten (z. B. Fußball, Football, Handball oder Basketball) – oft auch unter Fremdeinwirkung – auf. Auch beim Skifahren – vor allem wenn der Tal-Ski nach außen dreht, der Körper aber über dem Berg-Ski fixiert bleibt – sind Rupturen des vorderen Kreuzbandes eine häufige Art der Verletzung. Der über die Valgus- und Innenrotationsstellung laufende Verletzungsmechanismus beim Skifahren wird auch als „Phantomfuß-Mechanismus“ bezeichnet.[1][8] Ein Riss kann auch durch eine Auskugelung der Kniescheibe (Patellaluxation) mit plötzlichem Stabilitätsverlust des Kniegelenks bedingt sein.
Durch den Ausfall (Insuffizienz) des vorderen Kreuzbandes ist die Funktion eines der beiden zentralen passiven Führungselemente (primäre Stabilisatoren[9]) des Kniegelenks gestört. Daraus resultiert eine pathologische Bewegungsfreiheit des Schienbeinkopfes nach vorne (ventral), der so genannte „Tibiavorschub“. Gelenkkapsel, Seitenbänder, hinteres Kreuzband und Menisken werden vermehrt beansprucht, um den Schienbeinvorschub zu bremsen. Es kommt zu einer Überdehnung der Bandstrukturen. Bei Zunahme des Schienbeinvorschubs kommt es zu Knorpelschäden. Diese sind unter anderem dadurch bedingt, dass der Knorpel einer deutlich höheren Belastung ausgesetzt ist. Eine höhere Belastung bedeutet in so einem Fall eine frühzeitige Abnutzung mit Ausbildung einer Arthrose. Den vorderen Kreuzbandriss begleitende Verletzungen der Menisken und des Knorpels potenzieren das Risiko einer Arthrose.[10]
Hinteres Kreuzband
Risse des hinteren Kreuzbands sind seltener. Sie entstehen aufgrund des Überschreitens der maximalen Dehnungsmöglichkeit des hinteren Kreuzbands; in der Regel durch äußere Gewalteinwirkung. Von einem hinteren Kreuzbandriss ist in den meisten Fällen nicht nur das hintere Kreuzband betroffen. Die Verletzungen sind daher meist weitaus komplexer und betreffen in der Regel das gesamte Kniegelenk. Hauptursache für einen Riss des hinteren Kreuzbandes sind Verkehrsunfälle oder allgemeiner so genannte Rasanztraumata.[11] Dies ist darauf zurückzuführen, dass durch das Sitzen im PKW das Knie gebeugt ist. Durch ein Aufprallen des Unterschenkels an das Armaturenbrett reißt das hintere Kreuzband. Dieser Mechanismus wird deshalb auch dashboard injury (wörtlich aus dem engl. übersetzt: Armaturenbrett-Verletzung) genannt.[12][13] Diese Form der Verletzung ist allerdings relativ selten und ihre Häufigkeit hat im Laufe der Jahre mehr und mehr abgenommen. So fanden sich in einer in Deutschland durchgeführten Studie mit über 20 000 Unfallopfern bei Pkw-Unfällen lediglich 5 Fälle von dashboard injury.[14]
Bei körperkontaktbetonten Sportarten, wie beispielsweise American Football, kann eine von vorne-mittig einwirkende Gewalt durch eine zu starke Streckung zu einer Verletzung des hinteren Kreuzbandes führen. Häufig kommt es hierbei zu Mitverletzungen des vorderen Kreuzbandes sowie der hinteren Gelenkkapsel.[11]
Häufigkeit
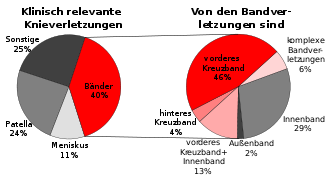 Anteil der Bänderverletzungen an den klinisch relevanten Knieverletzungen (links). Anteil der einzelnen Bänder an den Bandverletzungen (rechts).[15]
Anteil der Bänderverletzungen an den klinisch relevanten Knieverletzungen (links). Anteil der einzelnen Bänder an den Bandverletzungen (rechts).[15]
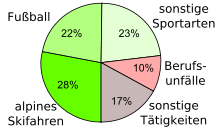 Verschiedene Ursachen und ihre Anteile an Kreuzbandrissen in der Schweiz. Der in Grün gehaltene Bereich «Sport und Spiel» kommt auf insgesamt 73%.[16]
Verschiedene Ursachen und ihre Anteile an Kreuzbandrissen in der Schweiz. Der in Grün gehaltene Bereich «Sport und Spiel» kommt auf insgesamt 73%.[16]
Der Anteil an Verletzungen der Bänder im Knie an allen klinisch relevanten Knieverletzungen liegt bei etwa 40 Prozent.[19] Von diesen 40 Prozent wiederum gehen etwa zwei Drittel der Verletzungen auf das Konto von Kreuzbandrissen – zu 46 Prozent nur das vordere Kreuzband und zu 4 Prozent nur das hintere. Mischverletzungen, beziehungsweise komplexere Verletzungen, mit Beteiligung der Kreuzbänder haben einen Anteil von 19 Prozent. Das vordere Kreuzband reißt statistisch gesehen etwa zehnmal so häufig wie das hintere. In den Vereinigten Staaten beträgt das Verhältnis von Rupturen des vorderen Kreuzbandes zum hinteren etwa 9 bis 10 : 1, in Deutschland etwa 14 : 1. Die Hauptursache für die deutlich geringere Inzidenz von Rupturen des hinteren Kreuzbandes sind zum einen dessen größerer Durchmesser und die dadurch bedingte vergleichsweise höhere Belastungsfähigkeit und zum anderen seine anders geartete Funktion.[20]
Der Riss des vorderen Kreuzbandes ist nicht nur die häufigste Bandverletzung des Knies, sondern auch die häufigste klinisch relevante Verletzung des Knies überhaupt.[15][21] Die Häufigkeit liegt bei etwa 0,5 bis 1[22] vorderen Kreuzbandrissen pro tausend Einwohner (USA, Mitteleuropa) und Jahr. In den Vereinigten Staaten kommt es pro Jahr zu etwa 80 000[23] bis 100 000[24] Rupturen des vorderen Kreuzbandes. Die Inzidenz ist im Altersintervall von 15 bis 25 Jahren am höchsten. Die dadurch entstehenden jährlichen Kosten liegen bei ungefähr 1 Milliarde Dollar.[23] In Deutschland betrugen 2002 die Krankheitskosten in den Krankenhäusern für die Behandlung der „Binnenschädigung des Kniegelenks“ – bei der Kreuzbandrisse den Hauptanteil verursachen – 359,3 Millionen Euro.[25][26] Statistisch gesehen reißt in Deutschland alle 6½ Minuten ein Kreuzband. Bei etwa jedem dritten ist zusätzlich ein Meniskus beschädigt.[27] In der Schweiz liegen die Schätzungen für die jährlichen Kosten durch Kreuzbandrupturen bei 200 bis 250 Millionen Franken. Von dieser Summe entfallen 40 Prozent auf Heilkosten, 47 Prozent auf Tagegelder, 2 Prozent auf Kapitalleistungen, wie beispielsweise Integritätsentschädigungen (ein sozialversicherungsrechtliches Schmerzensgeld), und 12 Prozent auf Invalidenrenten (Kapitalwerte). Pro Kreuzbandriss sind dies fast 21 000 Franken, mit einem durchschnittlichen Heilkostenanteil von 8350 Franken.[16]
Die Schweizerische Unfallstatistik (UVG), von der etwa die Hälfte aller Schweizer Bürger erfasst wird, meldet pro Jahr 6350 Verletzungen des vorderen Kreuzbandes (Zeitraum 1997 bis 2001). Die Hochrechnung für die Schweiz geht von 10 000 bis 12 000 Fällen aus. Von den erfassten 6350 Verletzungen werden 73 Prozent durch „Sport und Spiel“ verursacht, 10 Prozent sind Berufsunfälle und 17 Prozent entfallen auf sonstige Tätigkeiten, wie beispielsweise Wegeunfälle, Aufenthalt in Häusern oder andere Freizeitaktivitäten.[16]
Frauen haben eine zwei bis achtmal höhere Verletzungsrate als Männer, die den gleichen Sport ausüben. Verschiedene Studien zeigen, dass diese Verletzungen im Wesentlichen kontaktlos hervorgerufen werden.[28] Bei Basketballspielerinnen ist einer Studie zufolge die Wahrscheinlichkeit für eine Knieverletzung, eine Operation am Knie oder des vorderen Kreuzbandes viermal höher als bei männlichen Basketballspielern. Bei Fußballspielerinnen beträgt dieser Faktor 3,41.[29][30] Die Ursache für die erhöhte Inzidenz bei Frauen ist noch weitgehend unklar. So werden anatomische Unterschiede, wie beispielsweise ein größeres Spiel im Kniegelenk, Hormone[31] und Trainingstechniken diskutiert.[24][32][33]
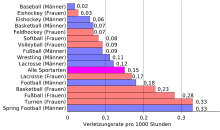
Der Anteil einzelner Sportarten an der Häufigkeit eines Kreuzbandrisses hängt sehr stark von den lokalen Präferenzen für die jeweilige Sportart ab. In den USA beispielsweise haben Basketballspieler (20 %), gefolgt von Fußball- (17 %) und American-Football-Spielern (14 %), den höchsten Anteil an Kreuzbandrissen, während in Norwegen die Reihenfolge Fußballspieler (42 %), Handballspieler (26 %) und alpine Skifahrer (10 %) ist.[34] In Deutschland treten die häufigsten Kreuzbandrisse bei den Sportarten Fußball, Handball und Skifahren (alpin) auf.[35] Danach folgen Straßenverkehrs- und Arbeitsunfälle.[36] Über 70 % der Risse des vorderen Kreuzbandes entstehen ohne Fremdeinwirkung bei der Landung nach einem Sprung, beim Abbremsen oder beim plötzlichen Richtungswechsel.[37][38]
Die Anzahl der jährlich diagnostizierten Kreuzbandrupturen nimmt seit Jahren beständig zu. Neben den verbesserten diagnostischen Möglichkeiten – mit der häufiger Kreuzbandrisse auch als solche erkannt werden – ist auch die Zunahme an sportlichen Aktivitäten in der Freizeitgesellschaft schuld an dieser Tendenz. Ohne einige bestimmte Sportarten wären Kreuzbandrupturen ein relativ seltenes Trauma.[20]
Risikofaktoren
Außer den unter der Rubrik Häufigkeit bereits beschriebenen Faktoren Sportart und Geschlecht spielen noch andere Risikofaktoren beim Kreuzbandriss eine Rolle. Aufgrund der Häufigkeit der Verletzung liegen umfassende statistische Daten und eine Vielzahl daraus abgeleiteter Studien vor. Die Ätiologie des vorderen Kreuzbandrisses ohne Fremdeinwirkung ist sehr vielschichtig und eine Reihe von teilweise sehr unterschiedlichen Faktoren beeinflussen das Risiko einer Ruptur. Es ist bis heute noch nicht vollständig zu erklären, warum einzelne Personen ein höheres Risiko für diese Verletzung haben als andere.[39] Beispielsweise ist ungeklärt, warum nach der Verletzung des vorderen Kreuzbands eines Knies eine erhöhte Wahrscheinlichkeit für dieselbe Verletzung des anderen Knies innerhalb der nächsten Jahre gegeben ist.[40][41][42][43][44][45] So haben deutsche Fußballspielerinnen, die bereits einen Kreuzbandriss hatten, eine über fünf mal höhere Wahrscheinlichkeit für eine erneute Kreuzbandruptur, als Spielerinnen, die bisher von dieser Verletzungsart verschont waren.[46] Bei den Risikofaktoren wird zwischen intrinsischen (personenbezogenen) und extrinsischen (äußeren) Faktoren unterschieden. Zu den intrinsischen Faktoren gehören beispielsweise die genetische Prädisposition beziehungsweise Anatomie, Trainingszustand (Fitness), neuromuskuläre Effekte oder hormonelle Faktoren. Dagegen sind beispielsweise die Bodenbeschaffenheit, das Wetter oder die Sportschuhe extrinsische Risikofaktoren.
Die Kenntnis der Risikofaktoren für Kreuzbandrisse ist ein wichtiger Ansatzpunkt für präventive Maßnahmen.
Intrinsische Risikofaktoren
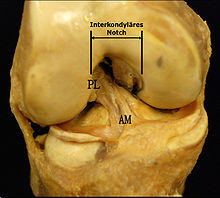
Anatomische Faktoren gehören zu den schon länger vermuteten Risikofaktoren. Die Reißfestigkeit eines Kreuzbandes hängt unmittelbar mit dessen Breite zusammen, die wiederum von Mensch zu Mensch unterschiedlich sein kann. In einer anthropometrischen Studie wurden die vorderen Kreuzbänder des unverletzten kontralateralen Knies von Patienten mit einer Kreuzbandruptur mit denen einer Kontrollgruppe mit gleicher mittlerer Körpermasse verglichen. Die Volumina der Kreuzbänder wurden mittels Magnetresonanztomografie ermittelt. In der Gruppe mit Kreuzbandrissen betrug das Volumen des kontralateralen Kreuzbandes durchschnittlich 1921 mm³, während es bei der Kontrollgruppe bei 2151 mm³ lag. Die Autoren der Studie schließen daraus, dass anthropometrische Unterschiede im Volumen – und daraus abgeleitet der Breite – des Kreuzbandes, einen direkten Einfluss auf die Wahrscheinlichkeit eines Kreuzbandrisses ohne Fremdeinwirkung haben.[47] Schon in früheren Studien wurde eine Korrelation von einer schmalen Kreuzbandhöhle (interkondyläres Notch), die wiederum im Zusammenhang mit einem schmaleren Kreuzband steht, mit einem erhöhten Risiko für einen Kreuzbandriss festgestellt.[48][49][50][51][52][53] Allerdings herrscht darüber kein wissenschaftlicher Konsens, da andere Studien zu anderen Ergebnissen kommen.[41][54][55] Frauen haben gegenüber Männern eine schmalere Kreuzbandhöhle, weshalb dieser anatomische Unterschied ein Erklärungsmodell für die höhere Inzidenz von Kreuzbandrupturen bei Frauen ist.[56][57]
Defizite in der Propriozeption,[58] das heißt der Wahrnehmung der eigenen Körperbewegung und -lage im Raum, werden ebenso wie neuromuskuläre Ermüdungserscheinungen in den unteren Extremitäten[59] und zentrale Ermüdungserscheinungen bei der Landung nach einem Sprung[60] als Risikofaktoren für eine vordere Kreuzbandruptur gesehen.[41] In einer Studie wurde festgestellt, dass die Patienten mit einem Kreuzbandriss signifikante Defizite bei neurokognitiven Fähigkeiten hatten.[61]
Extrinsische Risikofaktoren
Der Reibungskoeffizient zwischen Sportschuh und Untergrund ist ein Faktor bei der Ätiologie des Kreuzbandrisses. Ein hoher Reibungskoeffizient korreliert mit einem erhöhten Verletzungsrisiko.[62] In einer Studie über zwei Spielzeiten in den oberen drei norwegischen Handballigen spielte bei 55 Prozent der Kreuzbandrisse der Reibungskoeffizient Sportschuh/Bodenbelag eine Rolle.[63] In kälteren Monaten werden im American Football weniger Spieler durch Kreuzbandrisse verletzt, als in den Sommermonaten. Eine dabei diskutierte Ursache ist die in den kühleren Monaten reduzierte Bodenhaftung.[64]
In einer Studie über Kreuzbandrisse bei Australian Football wurde ebenfalls ein Zusammenhang mit den Wetterbedingungen und der Verletzungsrate festgestellt. So war die Verletzungsrate auf trockenen Spielfeldern signifikant höher als auf feuchten.[43] Als Ursache wird ein weicherer Untergrund nach Niederschlägen vermutet, der die Kraftübertragung zwischen Schuh und Oberfläche reduziert.[65]
Ebenfalls in Australien wurde ein Zusammenhang mit der Bodenbeschaffenheit festgestellt. So rissen in der Australian Football League auf Weidelgras weniger Kreuzbänder, als auf Hundszahngras. Hier wird als Ursache eine reduzierte Haftung der Sportschuhe in Wechselwirkung mit dem Weidelgras vermutet, wodurch die für das Kreuzband destruktive Kraftübertragung geringer ist, als auf dem Hundszahngras mit höherer Haftung.[66]
Symptomatik
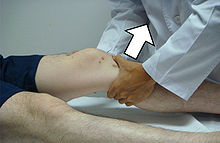
Wenn ein Kreuzband gerissen ist, führt dies meist zu einer deutlichen Schwellung des Kniegelenks und in Folge zu Schmerzhaftigkeit aufgrund der Kapseldehnung des Gelenkes. Ein blutiger Gelenkerguss (Hämarthros) ist der Normalfall bei einem Kreuzbandriss. Er tritt in 95 % der Fälle auf und schränkt sehr schnell die Beweglichkeit des Kniegelenks ein. Zusammen mit der Instabilität des Kniegelenks ist ein Hämarthros ein Leitsymptom für eine Kreuzbandruptur.[67] Umgekehrt ist ein Kreuzbandriss für etwa 50 bis über 75 % aller Hämarthrosen verantwortlich.[68] Diese Symptomatik wurde bereits im Jahre 1879 von dem Franzosen Paul Ferdinand Segond (1851–1912) beschrieben: Heftiger Schmerz im Knie-Inneren und rasches Einbluten mit entsprechender Schwellung des Gelenkes.[69] Ursache für diese Symptome sind die im Kreuzband verlaufenden Nervenfasern und Blutgefäße. Erstere lösen beim Zerreißen den Schmerz aus und letztere sorgen für die Einblutung in das Gelenk.
Oft ist das Zerreißen mit einem hörbaren Knall („Plopp“) verbunden.[70] Auf das Zerreißen folgt ein kurzer Schmerz. Die Instabiltiät im Knie bemerkt der Betroffene schon unmittelbar, wenn sich der erste Schmerz gelegt hat. Der Gelenkerguss stellt sich meist erst im Laufe des Tages ein. In der Regel muss der ausgeübte Sport abgebrochen werden. Eine Ausnahme sind Skifahrer, die oft noch die Abfahrt bewerkstelligen können – allerdings unter erheblichen Schmerzen. Treffen all diese Symptome zu, so handelt es sich mit 90%iger Sicherheit um einen Riss des vorderen Kreuzbandes (oder beider). Das Knie lässt sich meist nicht mehr ganz strecken und wird in leichter Beugestellung gehalten (Schonhaltung). In dieser Beugestellung kann man den Unterschenkelknochen mit der Hand gegen den Oberschenkelknochen um etwa 5–10 mm nach vorne ziehen ohne einen Anschlag zu spüren, während beim gesunden Knie nur wenige Millimeter (2–3 mm) möglich sind und man dann einen Anschlag verspürt (positiver Lachman-Test).
Nach etwa einer Woche klingen die Symptome bei einem vorderen Kreuzbandriss wieder ab. Manche Patienten beginnen bereits nach zwei Wochen wieder mit Sport. Der Grad der Instabilität des Kniegelenkes ist stark abhängig von den sekundären Kniegelenks-Stabilisatoren beziehungsweise deren Trainingszustand. Sekundäre Kniegelenks-Stabilisatoren sind andere periphere Bänder und Muskelsehnen.[9] Sie können teilweise die Funktion des vorderen Kreuzbandes zur Stabilisierung des Kniegelenkes übernehmen. Viele Patienten sind dann drei bis sechs Monate weitgehend beschwerdefrei. Danach können die sekundären Stabilisatoren die auf das Kniegelenk einwirkenden Kräfte aber meist nicht mehr abfangen. Schäden an den Menisken und Seitenbändern sowie ein vermehrtes Auftreten von giving way sind die Folge.[71]
Begleitverletzungen
Isolierte vordere Kreuzbandrisse sind eher die Ausnahme. Bis zu 80 % aller Kreuzbandrisse werden von anderen Verletzungen begleitet.[36] Verletzungen der Menisken sind dabei ausgesprochen häufig. In einer umfangreichen Studie wurde bei akuten Kreuzbandrissen in 42 % der Fälle ein Riss des Innenmeniskus und zu 62 % ein Riss des Außenmeniskus diagnostiziert. In einer anderen Studie wurde bei Kreuzbandrissen im chronischen Intervall (bei der Durchführung einer Bandplastik) bei 60 % der Patienten ein Riss des Innenmeniskus und bei 49 % einer des Außenmeniskus festgestellt.[72] Wird der verletzte Meniskus entfernt, so steigt die Instabilität des betroffenen Knies weiter an. Die stark eingeschränkte Stoßdämpfung führt des Weiteren zu einer verstärkten Häufigkeit sekundärer Arthrosen.[10][73] Unversehrte Menisken wirken sich positiv auf das Ergebnis einer Kreuzbandplastik aus.[74] Aus diesem Grund empfiehlt sich – wenn es der Riss des Meniskus zulässt – eine Refixation[75] des selbigen durchzuführen. Idealerweise erfolgt dies zusammen mit der Rekonstruktion des Kreuzbandes.[76][77]
Eine weitere häufige Begleitverletzung ist der Riss des Innen- und/oder Außenbandes des Kniegelenks. Sind Innenband, Innenmeniskus und vorderes Kreuzband betroffen, so spricht man von einer Unhappy Triad. Eher selten ist der anterolaterale (vorn und seitlich) knöcherne Kapselausriss am Schienbeinplateau, die sogenannte Segond-Fraktur.[1]
Verletzungen des Gelenkknorpels (traumatische Chondropathien) sind an 16 bis 46 % aller Rupturen des vorderen Kreuzbandes beteiligt.[78]
Seltener, aber meist unerkannt, ist der Riss der hinteren, äußeren Kapselschale, vor allem der Sehne des Popliteusmuskels (tiefer Wadenmuskel). Unbehandelt führt diese Verletzung zu einer erheblichen Kniegelenksinstabilität mit sichtbar gestörtem Gang.
Diagnostik
Die Diagnosestellung erfolgt in vielen Fällen mit einer erheblichen zeitlichen Verzögerung, auch wenn die Patienten unmittelbar nach der Verletzung einen Arzt aufgesucht haben. Einige Studien geben einen mittleren Zeitraum von 2[79] bis 21 Monaten[80] an, der zwischen dem Zeitpunkt der Verletzung und der korrekten Diagnosestellung vergeht. In vielen Fällen ist zudem der Besuch mehrerer Ärzte notwendig, bis die richtige Diagnose gestellt ist. Typische Falschdiagnosen sind vor allem Meniskusriss und „Verstauchung“.[81] Es wird deshalb davon ausgegangen, dass Kreuzbandrupturen unterdiagnostiziert werden. Das heißt, dass sie tatsächlich häufiger auftreten, als dass sie korrekt diagnostiziert werden.[80]
Klinische Befundung
- → siehe Hauptartikel Schubladentest, Lachman-Test und Pivot-Shift-Test
Bei einem Riss des vorderen Kreuzbands kommt es zum so genannten vorderen Schubladenphänomen: Bei gebeugtem Knie kann der Unterschenkel von hinten nach vorne geschoben werden. Ist dagegen das hintere Kreuzband gerissen, so kommt es zum hinteren Schubladenphänomen: Bei gebeugtem Knie kann der Unterschenkel von vorne nach hinten geschoben werden.
Die initiale Diagnose wird mittels Schubladen- und Lachman-Test (seltener Pivot-Shift-Test) durchgeführt. Aufgrund der Anatomie des vorderen Kreuzbandes (zwei Bandanteile = Faszikelbündel) ist eine klinische Diagnose oft erschwert, wenn nur ein Bündel gerissen ist. Hier ergibt sich dann beispielsweise ein negatives Schubladenphänomen in 90°-Beugung des Kniegelenkes, aber ein positiver Lachman-Test in 15°-Beugung.
Ein Ausfall (Insuffizienz) des hinteren Kreuzbandes kann in einigen Fällen durch eine Beobachtung (Inspektion) des in 90° gebeugten Kniegelenks von der Seite beim liegenden Patienten beurteilt werden. Bei zurückgesunkenem Schienbeinkopf sollte eine Verletzung des Bandes in Erwägung gezogen werden. Durch zusätzliches Anspannen der so genannten ischiocruralen Muskulatur (hintere Oberschenkelmuskulatur) kann dieses Phänomen verstärkt werden. Durch nachfolgende Quadrizepsmuskel-Anspannung (Kontraktion) wird die hintere Schublade aufgehoben.
Der Stabilitätsverlust tritt mit zunehmender Beugung im Kniegelenk ein und ist bei Streckung nicht vorhanden. Dadurch erklären sich die erstaunlich geringen Beschwerden bei isolierten Rissen. Beschwerden werden vor allem beim Treppensteigen oder beim Heben von Gewichten hinter der Kniescheibe (retropatellar) angegeben (erhöhter Druck des Oberschenkelknochens auf die Kniescheibe).
Die Instabilität, die durch einen Kreuzbandriss entsteht, sorgt für eine Überbelastung von Knorpel, Innen- und Außenmeniskus. Wird die Instabilität nicht durch die Muskulatur kompensiert oder durch eine Operation beseitigt, kommt es häufig zu einem Meniskusriss und/oder einer Knorpelschädigung mit Arthrose.
Bildgebende Verfahren
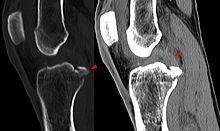 Knöcherner Ausriss des hinteren Kreuzbandes in der Computertomographie im Knochen- und Weichteilfenster.
Knöcherner Ausriss des hinteren Kreuzbandes in der Computertomographie im Knochen- und Weichteilfenster.
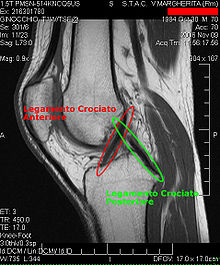
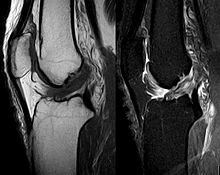
Die Diagnose kann mit bildgebenden Verfahren – namentlich der Magnetresonanztomographie (MRT, „Kernspin“) – bestätigt werden. Dabei ist allerdings zu beachten, dass die Interpretation der MRT in der Diagnostik eines Kreuzbandrisses zu 20 Prozent falsche Diagnosen liefert. Hier kommt es auf die so genannten Schnittbilder und die geeignete Positionierung des Kniegelenkes bei der MRT-Untersuchung an. Der Radiologe sollte die genaue Vorgeschichte kennen, die zur Verletzung führte, und auch Erfahrung in der Untersuchung eines verletzten Gelenkes haben, um Fehlbeurteilungen zu vermeiden. Im Vergleich zur MRT liegt die Fehlerquote bei dem erheblich einfacher durchzuführenden Lachman-Test bei nur 10 Prozent.[82][83][84][85] Die MRT ist daher in der Regel zur Diagnose eines vorderen Kreuzbandrisses weniger sensitiv und weniger spezifisch als die klinische Befundung durch einen qualifizierten Orthopäden.[86] Das Ergebnis einer MRT hat nur relativ selten einen Einfluss auf die klinische Entscheidungsfindung[87] und sollte keinen Ersatz für eine sorgfältige Anamnese und Palpation darstellen.[15] Mehrere Studien kommen zu dem Schluss, dass eine MRT nur bei komplizierteren unklaren Knieverletzungen – und dabei eher zum Erstellen einer Ausschlussdiagnose[88] – sinnvoll ist.[89][90]
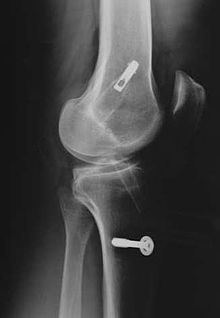
Röntgenaufnahmen leisten keinen unmittelbaren Beitrag zur Diagnosestellung einer Kreuzbandruptur. Beide Kreuzbänder sind – ob gerissen oder nicht – im Röntgenbild nicht sichtbar. Wird dennoch geröntgt, so kann dies der Diagnosestellung von möglichen knöchernen Begleitverletzungen dienen.
Diagnostische Arthroskopie
- → siehe Hauptartikel Arthroskopie
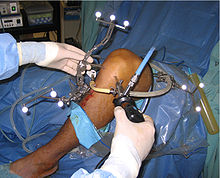
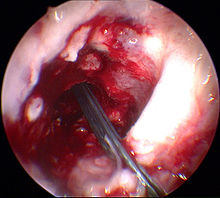
Die höchste diagnostische Sicherheit bietet die diagnostische Arthroskopie (Gelenkspiegelung). Dieses Verfahren stellt für die Diagnosestellung des Kreuzbandrisses den Goldstandard dar. Das Verfahren ist zwar minimal-invasiv, stellt aber in jedem Fall einen mit gewissen Risiken behafteten chirurgischen Eingriff in das Knie des Patienten dar.[91] Da jedoch die operative Behandlung eines Kreuzbandrisses in der Regel arthroskopisch (therapeutische Arthroskopie) durchgeführt wird, ergibt sich die Möglichkeit die Therapie, beispielsweise in Form einer Kreuzbandteilresektion (bei Anriss) oder einer Refixation des ausgerissenen Bandes, unmittelbar nach der diagnostischen Arthroskopie durchzuführen. Mit der zunehmenden Verbreitung von Kernspintomographen hat die Anzahl der rein diagnostischen Arthroskopien in den letzten Jahren deutlich abgenommen.[92][93] Die diagnostische Arthroskopie ist aber nach wie vor zur sicheren Abklärung der Diagnose einer Kreuzbandruptur – bei unklarer klinischer Befundung und unklarer MRT – das Mittel der Wahl.[91]
Späte Zeichen eines nicht diagnostizierten vorderen Kreuzbandrisses
Wird ein Kreuzbandriss nicht diagnostiziert und folglich auch nicht behandelt, so kann es zum so genannten giving way kommen. Dies bedeutet, dass das Kniegelenk instabil ist. Der Patient hat den Eindruck, dass z. B. beim Treppabwärtsgehen der Unterschenkel nicht unter Kontrolle steht.[71] Sportliche Belastungen mit Drehbewegungen des Kniegelenkes sind nicht möglich oder werden vermieden. Rezidivierende Schwellneigungen durch Gelenkergüsse können auftreten.
Therapiemöglichkeiten
Im Gegensatz zu Rupturen der Außen- und Innenbänder findet bei gerissenen Kreuzbändern – auch bei Ruhigstellung des Knies – keine Heilung durch Vernarbung („Zusammenwachsen“) statt. Es gibt keine intrinsische Heilung.[94] Eine Kreuzbandruptur sollte in jedem Fall nach erstellter Diagnose behandelt werden. Eine nicht therapierte Ruptur kann zu einer Degeneration des hyalinen Gelenkknorpels und so zu Meniskusschäden führen.[95][96] In einer Vielzahl von Studien konnte gezeigt werden, dass ein Ausbleiben therapeutischer Interventionen zu einer progressiven Zerstörung der Gelenkstrukturen führt und ein hohes Wiederverletzungsrisiko besteht.[97]
Die Behandlungsmöglichkeiten lassen sich in zwei Gruppen einteilen: in die chirurgische Therapie (Operation) und in die konservative Therapie. Welche Form der Behandlung zur Anwendung kommt, wird üblicherweise individuell mit dem Patienten auf dessen Bedürfnisse abgestimmt.[35] Für beide Formen gibt es verschiedene Ansätze und Behandlungskonzepte, die zum Teil kontrovers diskutiert werden. Grundsätzlich ist der Verlauf eines chronischen Kreuzbandschadens individuell sehr unterschiedlich. Es ist allgemein akzeptiert, dass nicht jeder Patient eine operative Behandlung zur Rekonstruktion des Kreuzbandes benötigt.[98][99][100][101] Jüngere, sportlich aktive Patienten profitieren einigen Studien zufolge von der Rekonstruktion des Kreuzbandes.[102][103][104][105][106][107]
Die Basis der konservativen Therapie ist ein physiotherapeutischer Muskelaufbau, der der externen Stabilisierung des Kniegelenkes dienen soll. Das Ziel der chirurgischen Therapien ist die anatomische und biomechanische Rekonstruktion des gerissenen Kreuzbandes, das heißt, die bestmögliche Wiederherstellung der Funktion des Kreuzbandes.[108]
Den ursprünglichen Zustand des Knies kann weder die konservative noch die operative Behandlung eines Kreuzbandrisses wiederherstellen – eine Ausnahme ist die Healing-Response-Technik, über die noch keine Langzeitstudien vorliegen.[98][109][110]
Konservative Behandlung
Nicht jedes gerissene Kreuzband muss operiert werden. In jedem Fall wird individuell, in Abhängigkeit von Lebensalter, Aktivität, Sportfähigkeit, Bereitschaft und Alltagsfähigkeit (Morbidität) des Patienten entschieden. Daher bedarf die Therapieentscheidung eines eingehenden Gespräches mit dem Patienten. Die konservative Behandlung ist vor allem für Patienten mit einem vorderen Kreuzbandriss ohne Begleitverletzungen, einer eingeschränkten sportlichen Aktivität und einem höheren Lebensalter eine Alternative zur Operation.[111][112] Bei sportlich aktiven, konservativ behandelten Patienten wurde eine erhöhte Häufigkeit von Arthrosen – im Vergleich zu operierten Patienten – festgestellt.[10] Mehrere Studien belegen einen signifikanten Vorteil der chirurgischen Intervention,[113][114][115][116][117] vor allem bei Sportlern, die Sportarten wie beispielsweise Fußball, Handball oder Basketball ausüben – also Sportarten mit hoher Rotations- und Hyperextension-Belastung des Kniegelenkes.[108][118] Es gibt einige ältere Studien, die zu dem Ergebnis kommen, dass die konservative Behandlung eines Kreuzbandrisses – auch bei Sportlern – keine negative Auswirkungen hat.[109][119][120][121]
In der konservativen Therapie wird über eine frühfunktionelle Bewegungsbehandlung versucht, die Kniegelenksinstabilität durch ein konsequentes Muskelaufbautraining zu kompensieren und so die fehlende Stabilität wieder herzustellen. Ein weiteres Ziel ist die Verbesserung der propriozeptiven Fähigkeiten der um das Kniegelenk herum gelegenen (periartikulären) Elemente.[122][123][124] Häufig wird durch eine Schienung des Kniegelenks in einer Orthese (Knie-Brace) für sechs Wochen und begleitende Physiotherapie eine ausreichende Stabilität erreicht.
Durch eine gezielte und sachgerechte orthopädische Behandlung kann prinzipiell ein Großteil von Patienten mit einer Ruptur des vorderen Kreuzbandes ihre sportliche und berufliche Tätigkeit uneingeschränkt wieder aufnehmen. Die so behandelten Patienten sind nach durchschnittlich sieben Wochen wieder arbeitsfähig und können nach etwa elf Wochen ein normales Leben führen. Diese Zeiten sind in der Regel kürzer als bei einem chirurgischen Eingriff.[125] Etwa 80 Prozent der Patienten kann nach vier Monaten wieder sportlich aktiv sein. Allerdings beschränkt sich dies im Wesentlichen auf Sportarten ohne direkten Körperkontakt und ohne das Knie belastende Schwenkbewegungen. Bei vielen Patienten mit konservativer Behandlung des Kreuzbandrisses stellt sich ein Angstgefühl beim Sport in den Situationen ein, die zur ursprünglichen Verletzung führten. Der für den Betroffenen spürbare Stabilitätsverlust des Knies ist dafür eine der Hauptursachen. Diese Unsicherheit verspüren 18 Monate nach der Verletzung etwa 30 Prozent der Patienten und nach vier Jahren nahezu 80 Prozent. Im täglichen Leben stört es dagegen nur etwa 10 Prozent. Im Alltagsleben sind die meisten Patienten schmerzfrei. In bestimmten Situationen, beispielsweise nach längeren Phasen ohne Bewegung oder Änderungen der Luftfeuchtigkeit, klagt etwa die Hälfte nach vier Jahren über Schmerzen. Bei bis zu 30 Prozent der Patienten ist nach vier Jahren ein Gelenkerguss, oft zusammen mit einer Meniskusläsion, diagnostizierbar. Letzteres ist meist eine Folge von Unfällen, die durch der Instabilität des Gelenkes resultieren.[109][121] Zur frühzeitigen Erkennung von möglichen Komplikationen ist bei der konservativen Therapie eine regelmäßige Überwachung des betroffenen Kniegelenks notwendig. Eine chirurgische Behandlung ist dann jederzeit möglich.
Bei komplexen Kniebandverletzungen (z. B. Unhappy Triad), knöchernen Ausrissen des vorderen Kreuzbands, zusätzlichen Läsionen im Meniskus, fehlender muskulärer Kompensation nach intensiver Physiotherapie, sowie bei jüngeren leistungsorientierten Sportlern wird normalerweise eine operative Behandlung durchgeführt.
Healing-Response-Technik
Die sogenannte Healing-Response-Technik wurde zu Beginn der 1990er Jahre von dem US-amerikanischen Chirurgen Richard Steadman entwickelt.[126][127][128] Dieses Therapieverfahren ist nur bei frischen vorderen Kreuzbandrissen, mit Abriss am Oberschenkelknochen oder bei einem Riss im Synovialüberzug, möglich. Bei 80 Prozent aller Rupturen des vorderen Kreuzbandes erfolgt der Abriss am Oberschenkelknochen.[129]
Undifferenzierte Stammzellen können sich bei entsprechender mechanischer Beanspruchung – gemäß dem Wolffschen Gesetz – zu Tendinozyten (Flügelzellen) ausdifferenzieren. Dies ist das therapeutische Konzept der Healing-Response-Technik. Mittels Arthroskopie werden zunächst eventuelle Begleitverletzungen behandelt. Anschließend wird mit einer Ahle das Knochenmark im Bereich des Kreuzbandes an bis zu zehn Stellen geöffnet, damit Stammzellen aus dem Mark austreten können. Ein ausreichender hoher Austritt von Blut aus dem Knochenmark ist wichtig. Danach wird das Kreuzband an seine Ansatzstelle in das Koagulum wieder reponiert und das Kniegelenk gestreckt. Die Behandlung wird stationär durchgeführt. Der Klinikaufenthalt dauert dabei typischerweise zwei Tage.[129] Ohne Drainage wird das Kniegelenk mit einer Schiene für etwa vier bis sechs Wochen in einer 10°-Beugung fixiert. Danach erfolgt ein intensives Training.[130] Nach durchschnittlich drei Monaten ist der so behandelte Patient wieder fähig Leistungssport auszuüben. Der Eingriff muss innerhalb von wenigen Tagen nach der Verletzung erfolgen. Die Erfolgsrate liegt bei über 80 Prozent. Misserfolge können mittels Kreuzbandplastik behandelt werden.[131] Das Verfahren ist möglicherweise auch zur Behandlung von Rissen des hinteren Kreuzbandes geeignet.[132]
Operative Behandlung
In den 1970er bis 1980er Jahren lag die Altersgrenze für Operationen zur Rekonstruktion des vorderen Kreuzbandes bei etwa 35 Jahren. Dies lag an den noch eingeschränkten operativen Möglichkeiten im Zusammenhang mit der mäßigen Blutversorgung und schlechten Heilungstendenz der Kreuzbänder. Heute gibt es keine Altersgrenze mehr.[133] Der Zustand des betroffenen Knies, die Ansprüche des Patienten und seine Motivation sind die wesentlichen Einflussgrößen für die Entscheidung für oder gegen eine operative Behandlung. In den meisten Fällen besteht aus medizinischer Sicht bei einem Kreuzbandriss kein unmittelbarer Bedarf für eine sofortige chirurgische Intervention. Eine frische Ruptur wird idealerweise nach einem Physiotherapiezyklus – das sind in der Regel etwa sechs bis acht Wochen nach der Verletzung – operiert. Das Knie ist dann normalerweise wieder vollständig abgeschwollen.[134] In vielen Fällen erfolgt eine operative Behandlung mehrere Monate oder gar Jahre nach der Kreuzbandruptur. Beispielsweise dann, wenn eine zunächst nur geringe Instabilität des betroffenen Knies bei Patienten zu Beschwerden führt.[134] In den skandinavischen Ländern Norwegen, Dänemark und Schweden beträgt die Zeit zwischen Ruptur und Operation im Mittel sieben, neun und zehn Monate,[135] in den Vereinigten Staaten dagegen 2,4 Monate. Der Inter-Quartilsabstand geht dabei in den USA von 1,2 bis 7,2 Monate und in Norwegen von 4,2 bis 17,8 Monate.[34]
Einige neuere Studien kommen zu dem Ergebnis, dass bereits sechs Monate nach einer Kreuzbandruptur ohne operative Intervention degenerative Erscheinungen an den Menisken der betroffenen Knie zu beobachten sind, so dass die Autoren zur Reduzierung der Risiken eine Rekonstruktion innerhalb eines Jahres empfehlen.[136][137][138]
Absolute Indikation für eine Operation ist die Instabilität des Kniegelenkes. Diese führt ohne Stabilisationsoperation zu Meniskusschäden und letztendlich zu einer sekundären Arthrose des Gelenkes. Es sind vorwiegend sportlich aktive Menschen in jüngeren Altersstufen betroffen, wobei auch in den letzten Jahren die Generation der über 50-jährigen einen Anstieg an Kreuzband-Sportverletzungen in Deutschland zu verzeichnen hatte. Besteht ferner für die Betroffenen eine berufliche Einschränkung (z. B. Handwerksberufe), so ist auch hier die Operation notwendig.
Die nachfolgenden Techniken beziehen sich alle auf die Rekonstruktion des vorderen Kreuzbandes. Rekonstruktionen des hinteren Kreuzbandes sind vergleichsweise selten. Sie werden am Ende dieses Absatzes aufgeführt.
Kreuzbandnaht
- →siehe auch Absatz Medizingeschichtliches
Bis in die 1980er Jahren wurde das Verfahren der Primärnaht, beispielsweise bei intraligamentären Rissen, bevorzugt. Bei der Primärnaht werden die durchtrennten Enden des Kreuzbandes im Sinn einer Reparatur wieder zusammengenäht. Dieser Therapieansatz wurde erstmals 1895 durchgeführt. 1976 erschien eine Studie über die Primärnaht von Kreuzbandrissen, deren Langzeitergebnisse ausgesprochen schlecht waren.[139] Die Versagerquote dieser Methode lag in den ersten fünf Jahren nach der Operation bei 40 bis 50 Prozent.[107] In der Folgezeit wurde die primäre Naht des Kreuzbandes ohne Augmentation als Therapie mehr und mehr zugunsten der Rekonstruktion des vorderen Kreuzbandes aufgegeben.[140] Auch nachfolgende Langzeitstudien[141][142][143] belegen die progressive Verschlechterung der Resultate über längere Zeiträume, weshalb die primäre Naht heute obsolet ist und keine Therapieoption mehr darstellt.[144][145][146][147][148][149] Ursache für die schlechten Langzeitergebnisse ist das biomechanisch unzulängliche Narbengewebe, das bei der Primärnaht entsteht und zu einer erneuten Instabilität im Knie führt.[108][150][151][152]
Eine Variante der Kreuzbandnaht ist die Verstärkung des heilenden Kreuzbandes durch eine so genannte Augmentation. Für die Augmentation können verschiedene synthetische Bandmaterialien oder auch körpereigenes Gewebe verwendet werden. Die Verstärkung kann intraartikulär (innerhalb des Gelenkes)[153][154][155][156][157][158] oder auch extraartikulär (außerhalb des Gelenkes) [159][160][161][162][163] erfolgen. Auch diese Verfahren werden allgemein als überholt angesehen. Ihre Anwendung ist heute nicht mehr zu rechtfertigen.[99][107]
Sonderfall knöcherner Ausriss
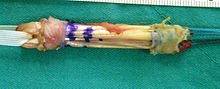
Der knöcherne Ab- oder Ausriss am vorderen Kreuzband ist wesentlich seltener als seine intraligamentäre Ruptur[164] und ist kein Kreuzbandriss. Dieser Sonderfall tritt häufiger bei Kindern, vor allem im Bereich der Eminentia intercondylica auf und hat durch Refixierung des Ausrisses – beispielsweise mit Schrauben oder Drahtnaht – im Allgemeinen gute Chancen wieder vollständig einzuheilen.
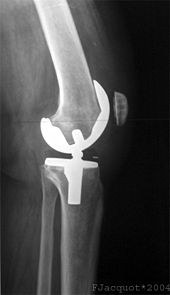
Kreuzbandplastik
Alle aktuell verwendeten Operationstechniken sehen die Rekonstruktion des gerissenen Kreuzbandes vor. Die Reste des durchtrennten Bandes werden dazu vollständig entfernt und durch ein neues Band ersetzt. Das neue Band kann aus körpereigenem Gewebe (autolog) oder aus dem Gewebe von Verstorbenen (allogen) oder einer anderen Spezies (xenogen) sein.[16]
Während noch in den 1980er Jahren meist sofort oder zumindest kurzfristig nach der Verletzung eine Operation durchgeführt wurde, wird seit den 1990er Jahren das „zweizeitige“ Vorgehen bevorzugt. Nach klinischer Untersuchung, oft gestützt durch den Befund einer Magnetresonanztomographie (MRT), wird die Arthroskopie mit Resektion des gerissenen Kreuzbandes und Versorgung von allfälligen Meniskusverletzungen als Vorbereitung für die zweite Operation (Kreuzbandplastik) vorgenommen. Nach der Arthroskopie folgt eine physiotherapeutische Behandlung zur Abschwellung des Knies und Kräftigung der Muskulatur. Nach Abklingen der Symptomatik wird zirka sechs Wochen nach Erstarthroskopie die eigentliche Kreuzband-Operation durchgeführt.
Diese zweizeitige Methode wird bis heute von vielen Operateuren bevorzugt, da man bei den „Sofortoperationen“ eine höhere Rate an Arthrofibrosen und damit massive Bewegungseinschränkungen nach der Operation beobachtete.
In den letzten Jahren wird allerdings – dank besser standardisierter Methoden, aber auch zwecks möglicher Abkürzung des Behandlungsverfahrens – wieder vermehrt „einzeitig“ operiert. Dabei werden die Stümpfe des gerissenen Kreuzbandes meist nur noch partiell entfernt; oft gerade so viel, dass ein Einklemmen der Stümpfe im Gelenk verhindert wird. Klinisch gesicherte Kreuzbandverletzungen können – insbesondere bei Hochleistungs- und Profisportlern – unmittelbar nach der Verletzung auch sofort versorgt werden, soweit das Knie noch weitgehend entzündungsfrei ist.[165]
Bei allen Rekonstruktionstechniken wird versucht, die Eigenschaften des ursprünglichen Kreuzbandes so gut wie möglich wieder herzustellen. Das vordere Kreuzband hat eine multiaxiale Faserstruktur. Keines der derzeit verwendeten Transplantate erreicht diese Struktur. Allen Rekonstruktionen fehlt zudem die Propriozeption. Ein gesundes Kreuzband hat Mechanorezeptoren, die den Transplantaten fehlen. Über die Mechanorezptoren können afferente Signale zum Rückenmark geleitet und Motoneuronen über die γ-Spindelschleife entladen werden. Dieser Regelkreis beeinflusst den Bewegungs-, Kraft-, und Stellungssinn des Kniegelenkes und ist ein wichtiger Faktor für dessen Stabilität. Die gesamte Propriozeption des betroffenen Knies ist durch den Verlust der Sensorik deutlich verschlechtert.[166][167] Deshalb erreicht keine derzeit bekannte Operationstechnik nach der Rekonstruktion des Kreuzbandes die Qualität des unverletzten Bandes. Darüber, welche Technik beziehungsweise welches Transplantat den Eigenschaften eines unverletzten Kreuzbandes am nächsten kommt, wird kontrovers diskutiert.[108]
Transplantatauswahl
Bei den verwendeten Transplantatmaterialen, die das gerissene vordere Kreuzband ersetzen sollen, haben sich seit den 1980er Jahren im Wesentlichen körpereigene (autologe) Transplantate durchgesetzt. Zurzeit kommen hauptsächlich das Kniescheibenband, die Quadrizepssehne und die Semitendinosussehne zum Einsatz. Die Transplantatwahl ist in Fachkreisen das seit Jahren am meisten diskutierte Thema der Kniechirurgie.[107][168][169]
Kaum verwendet werden Streifen aus dem Tractus iliotibialis oder der Faszie des Musculus gastrocnemius.[107] Aufgrund der Morbidität und Invasivität bei den körpereigenen Sehnentransplantaten sind synthetische Bandersatzmaterialien oder Leichen-Transplantate eine naheliegende Alternative. Die Leitlinien der Deutschen Gesellschaft für Unfallchirurgie empfehlen freie mehrsträngige Sehnentransplantate aus der Pes-anserinus-Gruppe (Semitendinosussehne oder Semitendinosus- und Gracilissehne) sowie aus der Patellasehne und seiner Knochenansätze.[170]
In den Vereinigten Staaten wurden im Jahr 2006 einer Studie zufolge etwa 46 Prozent aller vorderen Kreuzbandplastiken mittels BTB-Technik, 32 Prozent mittels Hamstring und 22 Prozent per Allograft realisiert.[171] In Deutschland bevorzugte, nach einer Umfrage aus dem Jahr 2004, ein etwas höherer Anteil der Operateure die Kniescheibensehne als Transplantat gegenüber den Hamstrings.[172] Die meisten Chirurgen im Bundesgebiet haben sich auf eine Operationstechnik spezialisiert.[166]
Kniescheibensehne
Bei der Kniescheibensehne (fachsprachlich: Patella(r)sehne, Ligamentum patellae) handelt es sich um eine sehr große und starke Sehne, sie stellt daher in vielen Fällen das Mittel der Wahl dar. Sie ist aber nur halb so elastisch wie das natürliche eigene Kreuzband. Bei der Rekonstruktion des Kreuzbandes mittels autologer Transplantation der Kniescheibensehne wird diese mit anhängenden Knochenteilen (engl.: bone tendon bone = Knochen-Sehne-Knochen; BTB-Technik) entnommen und durch verbreiterte Kanäle (8–10 mm Durchmesser) im Schienbein beziehungsweise Oberschenkelknochen gezogen. Die Länge des oberen und unteren Knochenblocks beträgt jeweils etwa 20 mm. Die stabilste Verankerung der Knochenenden des autologen Transplantats (engl.: graft = Transplantate ohne Blutversorgung, weshalb sowohl hier als auch bei der im folgenden Abschnitt näher erläuterten Semitendinosustechnik von autograft gesprochen wird, mit griechisch αὐτός = selbst) wird durch die Fixation mit so genannten Interferenzschrauben erreicht. Diese ist besonders wichtig im Hinblick auf eine frühe funktionelle Mobilisierung.Die Unterstützung nach der Operation mittels einer orthopädietechnischen Schiene (Orthese) ist häufig nicht nötig, so dass die Gefahr der Muskelatrophie geringer ist als bei anderen Verfahren. Dieser Vorteil ist insbesondere für Sportler interessant, die eine frühzeitige Rückkehr zu alter Leistung wünschen.
Da die Kniescheibensehne nur halb so dehnbar ist, wie das eigentliche Kreuzband, kann es bis zu 18 Monate dauern, bis wieder an so genannten „Stop-and-go“-Sportarten teilgenommen werden kann.
Semitendinosussehne
Der halbsehnige Muskel (Musculus semitendinosus) zieht an der zur Mitte zeigenden Seite vom Kniegelenk zum Oberschenkelknochen und ist Bestandteil des so genannten „Gänsefußes“ Pes anserinus superficialis, der zusätzlich aus den Sehnen des Musculus gracilis und Musculus sartorius gebildet wird.
Die Sehne (Transplantat) wird durch einen mittleren Schnitt auf dem Schienbein, knapp unterhalb des Knies, mittels eines so genannten tendon stripper oder ring stripper (Sehnenschneider, engl. auch harvester von to harvest = ‚ernten‘) entnommen. Je nach Länge wird die Sehne drei- oder vierfach mit einer bestimmten Fadentechnik zusammengelegt, verdrillt, fixiert und durch eine Bohrung durch den Unterschenkel zum Oberschenkel geführt und dort ebenfalls befestigt. Seit Begin des 21. Jahrhunderts ist eine minimal-invasive Technik zur leichteren und schnelleren Entnahme der Sehne aus der Kniekehle, bei besseren kosmetischen Resultaten, vorhanden.[173]
Die Semitendinosussehne ist vierfach gelegt stärker als die Kniescheibensehne. Diese Technik war der Kniescheibensehnentechnik bis etwa zum Jahre 2003 ebenbürtig. Seitdem etabliert sich diese Technik als so genannter „Goldstandard“, da vor allem die Entnahmestelle weniger schmerzhaft verheilt. Wenn die Semitendinosussehne zu kurz oder zu dünn ist, wird zusätzlich die Gracilissehne entnommen (STG-Technik; Semitendinosus- und Gracilissehne). Das Transplantat wird dadurch aber nicht belastbarer. Manche Operateure entnehmen immer beide Sehnen. Insbesondere für die Plastik des hinteren Kreuzbandes werden sowohl Semitendinosus- als auch Gracillissehne benötigt, was besonders im Fall einer zusätzlich zu versorgenden Außenbandinstabilität die Entnahme von der Gegenseite notwendig macht.
Die modernste OP-Technik ist die Doppel-Bündel-Technik (double bundle technique). Dabei werden mittels vier Knochenkanälen zwei Bündel (anteriomedial und posterolateral) in das Knie eingesetzt. Durch die bessere Nachahmung der Anatomie ergeben sich stabilere Ergebnisse. Dieses Verfahren ist allerdings technisch anspruchsvoll und wird derzeit (2010) nur in spezialisierten Zentren durchgeführt. Die Fixation der beiden Transplantate erfolgt ausschließlich extraartikulär durch Endobuttons.[174]
Quadrizepssehne
Dem oben genannten Prinzip folgend wird oberhalb der Kniescheibe ein Teil der Sehne des vierbäuchigen Oberschenkelmuskels einschließlich eines Kniescheiben-Knochenzylinders entnommen und in oben gezeigter Weise als Kreuzband implantiert.[175] Als sogenannte Press-fit-Methode wird sie ohne zusätzliche Verschraubung angewandt. Vorteil sind die im Vergleich zur Gracilissehne stärkeren Sehnen. Im Vergleich zur Patellasehne bestehen deutlich geringere Schmerzen beim Knien, da der Druck nicht auf der Narbe lastet. Nachteilig ist, dass nach der Operation häufig ein Muskelschwund des Musculus quadriceps femoris auftritt. Die Quadrizepssehne wird bisher nur von relativ wenigen Chirurgen zur Rekonstruktion des Kreuzbandes verwendet.[107]Allograft
Bei einem so genannten Allograft handelt es sich um ein Leichen-Transplantat. Hierfür kommen neben den drei zuvor genannten Sehnen, auch präparierte Achillessehnen und die Tibialis-anterior-Sehne in Frage. Ein positiver Effekt bei der Verwendung eines Allografts ist, dass es zu keiner Entnahmemorbidität kommen kann. Weitere Vorteile sind die kürzere Operationszeit, kleinere Operationsnarben und Reduzierung der postoperativen Schmerzen.[176] Ursprünglich wurden Allografts nur bei Revisionseingriffen und für die Rekonstruktion des hinteren Kreuzbandes verwendet. Mittlerweile kommen Allografts vermehrt auch zur primären Rekonstruktion des vorderen Kreuzbandes zum Einsatz.[107]Verwendet werden unbehandelte tiefgefrorene Transplantate. Die ursprünglich angewandten Verfahren zur Sterilisation (γ-Strahlung oder Ethylenoxid) schädigten das Transplantat in seinen biomechanischen Eigenschaften oder führten zu Abstoßungsreaktionen.[177][178][179][180] Bei den unbehandelten Transplantaten ergibt sich jedoch die HIV-Problematik. Die in Deutschland transplantierten Allografts stammen im Wesentlichen aus klinikeigenen Beständen oder von Eurotransplant, da Handel und Vertrieb von Organteilen in Deutschland gesetzlich verboten sind. Die hirntoten Lebendspender werden unter anderem auf das HI-Virus hin untersucht. Das Risiko einer Infektion des Empfängers beschränkt sich somit auf den Zeitraum der „diagnostischen Lücke“ und wird als sehr gering eingestuft.[107]
Die tiefgefrorenen Allografts lösen keine Abstoßungsreaktion aus.[181][182] Eine Reihe von Studien bescheinigt den Allografts ähnliche Werte wie den autologen Transplantaten, sowohl in der Kurz-[183] als auch Langzeitbetrachtung.[184][185] Qualitativ stehen Allografts autologen Transplantaten in nichts nach.[186] Ob ein autologes oder ein allogenes Transplantat zur Rekonstruktion ein Kreuzbandes verwendet wird, ist letztlich eine Entscheidung von Arzt und Patient.[187] Ein wesentliches Problem ist dabei, dass es viel zu wenige Spender für Allografts gibt, um den Bedarf auch nur annähernd decken zu können.[107]
Synthetische Rekonstruktionsmaterialien
Synthetische Kreuzbandprothesen, das heißt Implantate beispielsweise aus Kohlenstofffasern, Polyester, Polypropylen, Gore-Tex oder Rinderkollagen, wurden vor allem in der 1980er Jahren verwendet. Sie werden wegen der unzureichenden biomechanischen Eigenschaften und einer erhöhten Anzahl von intraartikulären Komplikationen nicht mehr verwendet.[168] Bei diesen Komplikationen handelte es sich meist um Gelenkergüsse und reaktive Synovitiden (Entzündungen der inneren Schicht der Gelenkkapsel).[188][189] Die Komplikationen wurden vor allem durch Abriebpartikel hervorgerufen, die im Gelenk zu Fremdkörperreaktionen führen.[190] [191][192] Die Versagerquote lag bei diesen synthetischen Kreuzbandprothesen zwischen 40 und 78 Prozent.[99][108]Befestigung des Transplantats
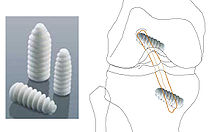 Autoresorbierbare Interferenzschrauben und ihre Positionierung bei der Rekonstruktion des vorderen Kreuzbandes.[193]
Autoresorbierbare Interferenzschrauben und ihre Positionierung bei der Rekonstruktion des vorderen Kreuzbandes.[193]
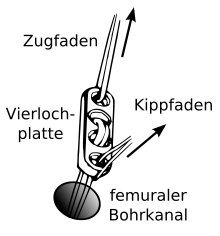
In den frühen 1990er Jahren wurden die Kniescheibensehnen-Transplantate mit so genannten Titan-Interferenzschrauben als Fixation an beiden Enden des Transplantates, teilweise auch nur einseitig verschraubt und am Oberschenkelknochen mit einem so genannten Endobutton, der durch das Transplantat „gefädelt“ wird, befestigt. Der Endobutton besteht aus einer Schlaufe aus einem nichtresorbierbarem Fadenmaterial mit einem Titan-Kipp-Knopf (Vierlochplatte), der nach der Durchführung durch den Knochenkanal verkippt wird.[194] Später wurden die Titanschrauben durch die heute verwendeten so genannten Bio-Screws („Bio-Schrauben“, das sind autobioresorbierbare Interferenzschrauben) ersetzt,[195] die einen erneuten Eingriff zur Materialentfernung unnötig machen. Diese Schrauben bestehen aus abbaubaren Polymeren, wie beispielsweise Poly-L-Lactid (PLLA) oder Poly-(L-co-D/L-Lactid) (PLDLLA). Ebenso kann eine Hybridtechnik aus Bio-Schraube (als intraartikuläre Fixation) und femorale/tibialen Endobuttons (als extraartikuläre Fixation) durchgeführt werden. Bei der so genannten „Press-Fit-Technik-Fixation“, die um das Jahr 1995 aufkam, kann auf die Schraubenfixation bei der BTB-Technik (Knochen-Sehne-Knochen-Technik) völlig verzichtet werden. Hierbei werden die Knochenenden konisch zugerichtet, sodass ein festes Verkanten in den Bohrkanälen gewährleistet ist. Ab 1996 kamen operative Verfahren mittels robotergesteuerten Bohrkanaldiamantfräsen auf, welche sich in letzter Zeit aufgrund hoher Kosten (personal- und apparateintensiv) nicht durchsetzen konnten und keine eindeutig besseren operativen Ergebnisse hervorbrachten.
Bei Semitendinosus- und Gracilistransplantaten (STG) werden meist Bio-Screws für die Befestigung genommen. Seit Ende der 1990er Jahre ist auch hier eine implantatfreie Fixation möglich.[196] Bei dieser Technik wird in das Semitendinosus- und Gracilissehnen-Transplantat am Ende geknotet und der femurale Kanal in Richtung Gelenk etwa 4 mm schmaler aufgebohrt, als an der gelenkfernen Stelle. Das Transplantat wird über die femurale Bohrung in das Gelenk eingesetzt. Dabei sitzt der Knoten des Transplantates vor dem schmaleren Teil des Kanals auf. Messungen ergaben, dass die Gelenksteifigkeit und die maximale Last ähnliche Werte wie bei anderen Techniken erreicht. Durch die Knotung der Sehnenenden sind Interferenzschrauben (Implantate) überflüssig. Die Protagonisten der implantatfreien Fixation sehen darin einen Kostenvorteil. Da keine Implantate verwendet werden, können auch keine Probleme mit diesen Materialien auftreten.[196] Nachteilig ist jedoch der erheblich größere Kanal im Oberschenkelknochen.[1]
Bei der Fixierung der Transplantate mit Interferenzschrauben ist es zur Vermeidung des sogenannten „Bungee-Effektes“ und des „Scheibenwischer-Effektes“ wichtig, dass die Fixierung nahe an den Gelenkflächen erfolgt.[1]
Morbidität und Invasivität der Transplantatentnahme
Die Qualität und Technik der rekonstruierten Kreuzbänder wurde seit der ersten Kreuzbandplastik 1917 stetig verbessert und weist heute sehr hohe Erfolgsraten auf. Die hohen Erfolgsraten im Bereich von etwa 90 Prozent verändern die Anspruchshaltung der Patienten. Ein Nebenaspekt der autologen Transplantate gewinnt daher zunehmend an Bedeutung: die Morbidität und Invasivität der Transplantatentnahme. Sie hat mittlerweile einen erheblichen Einfluss auf die Zufriedenheit der Patienten, die im Wesentlichen durch Schmerzen und Beweglichkeit bestimmt wird.[107][197]
 Sagittalschnitt des Kniegelenks mit Darstellung des Hoffa-Fettkörpers (Corpus adiposum infrapatellare, oben rechts). Verletzungen des Hoffa-Fettkörpers können bei der Entnahme der Kniescheibensehne zu Komplikationen führen.
Sagittalschnitt des Kniegelenks mit Darstellung des Hoffa-Fettkörpers (Corpus adiposum infrapatellare, oben rechts). Verletzungen des Hoffa-Fettkörpers können bei der Entnahme der Kniescheibensehne zu Komplikationen führen.
Die Entnahme der Kniescheibensehne ist häufig schmerzhafter ist als die der anderen autologen Sehnen. Bis zu 60 Prozent der Patienten klagen über Schmerzen beim Knien. Für Patienten mit häufigen knienden Tätigkeiten wird deshalb meist vom Patellasehnen-Transplantat abgeraten. Den Schmerz im Knie verursachen das Patellaspitzensyndrom, Patellatendinitis, patellofemorale Krepitation[198] und infrapatelläre Kontrakturen.[199][200][201] Die Häufigkeit dieser Symptome variiert und liegt je nach Studie zwischen 4 und 40 Prozent der Patienten.[107][201][202][203][204] Eine wesentliche Ursache für die Komplikationen sind offenbar Verletzungen des Hoffa-Fettkörpers, die zu einer narbigen Kontraktur (Verkürzung der Patellasehne) und einer Fibrose führen können. Dies führt wiederum zu einer eingeschränkten Beweglichkeit der Patellasehne und ihrem Festsitzen an der Vorderkante des Schienbeinknochens. Dass sich die Patellasehne nach der Entnahme des Transplantates verkürzt, wird in einer Reihe von Studien beschrieben.[191][205][206] Die Verkürzung kann im Bereich zwischen 2 und 7 mm liegen. Eine zu starke Verkürzung der Patellasehne kann zu einer patellofemoralen Arthrose führen.[107][207] In Einzelfällen sind Fissuren der Kniescheibe beobachtet worden, die unter hoher Belastung zum Knochenbruch (Fraktur) derselben führen können. Das Risiko für eine Patellafraktur liegt im Bereich von 0,1 bis 3 Prozent. Durch eine sorgfältige Entnahme des Transplantates lässt es sich weiter minimieren. Wird bei der Entnahme des patellären Knochenblocks beispielsweise eine Hohlfräse verwendet, so wird auch das Risiko der Bildung von Sollbruchstellen vermieden. Die Wahrscheinlichkeit einer Patellasehnenruptur ist durch die Entnahme der Kniescheibensehne erhöht.[107]
Auch die Entnahme einer Semitendinosussehne (Hamstring) zur Rekonstruktion des vorderen Kreuzbandes kann zu Komplikationen führen. So wird beispielsweise die Beugekraft der ischiokruralen Muskulatur in den ersten Monaten nach der Entnahme der Sehne reduziert.[208][209][210] Auch das Auftreten von patellofemoralen Schmerzen wird von einigen Patienten bei dieser Transplantationsmethode beklagt.[203][208] Die Ursachen für die Schmerzen sind offensichtlich ein gestörter patellofemoraler Bewegungsablauf im betroffenen Knie,[211] sowie die Verkürzung der Quadrizepsmuskulatur durch die Entnahme des Hamstrings.[107] Durch die Entnahme der Semitendinosussehne entstehende Schmerzen sind eher selten und dann auch nur von kurzer Dauer.[210] Die gleichzeitige Entnahme von Semitendinosus- und Grazilissehne kann die Innenrotation des Kniegelenkes längerfristig stören.[212] Die Hamstrings regenerieren sich nach der Entnahme des Transplantates weitgehend vollständig. Sie verändern aber meist ihre Lage und sind dann etwas näher zum Körper gelegen (proximal).[107][213][214][215][216][217]
Der Anteil an Operationen bei denen die Quadrizepssehne zur Rekonstruktion des Kreuzbandes verwendet wird, ist bisher noch recht gering. Entsprechend schlecht ist die Datenlage zur Morbidität der Entnahme dieser Sehne. In den vorhandenen Studien sind die Ergebnisse zum Teil sehr widersprüchlich. Einige Autoren berichten im Vergleich zur Entnahme der Patellasehne von einer deutlich geringeren Entnahmemorbidität[107], während andere von einer Funktionseinschränkung und deutlichen Schmerzen schreiben.[218]
Typischer Ablauf einer Rekonstruktion des vorderen Kreuzbandes
In diesem Beispiel wird der Ablauf der Rekonstruktion des vorderen Kreuzbandes durch Transplantation einer autologen Semitendinosus- und Gracilissehne beschrieben. In den 1980er Jahren wurde die klassische offene Kreuzbandoperation über den Payr-Zugang zunächst durch die Miniarthrotomie abgelöst.[150] Mittlerweile werden nahezu alle Kreuzbandrekonstruktionen minimalinvasiv mittels Arthroskopie durchgeführt.[219] Nur in Ausnahmefällen, beispielsweise bei sehr komplexen Knieverletzungen, erfolgt eine offene Operation.
Anästhesie
Der Eingriff kann unter Allgemeinanästhesie (Vollnarkose) oder unter Regionalanästhesie erfolgen. Beide Verfahren haben für den Patienten Vor- und Nachteile. Als regionale Verfahren kommen die Spinalanästhesie, die Periduralanästhesie (PDA, Rückenmarksnarkose) und die kombinierte Spinal- und Epiduralanästhesie (CSE) infrage. Eine andere, häufig zusätzlich zu den genannten Anästhesieformen angewandte Form der Regionalanästhesie ist der Femoraliskatheter. Damit können vor allem die Schmerzen im betroffenen Knie nach der Operation (postoperativ) unterdrückt werden (Nervus-femoralis-Blockade). Dazu wird ein Lokalanästhetikum mit Hilfe eines Katheters in die Nähe des schmerzleitenden Nervs, des Nervus femoralis, gebracht. Eine vollständige Blockade des Knies ist damit alleine jedoch nicht möglich.[9] Die Fasern des N. femoralis verlaufen von der Lendenwirbelsäule aus kommend bis zum Kniegelenk. Ein haarfeiner Schlauch transportiert über eine kleine Dosiereinheit das Schmerzmittel in der Leistengegend an den N. femoralis. Durch die Blockade des N. femoralis wird nicht nur der Schmerz betäubt, sondern auch Gefühl, Kraft und Beweglichkeit des Beins eingeschränkt. Drei bis fünf Tage nach der Operation wird der Katheter entfernt.[220]
Arthroskopie
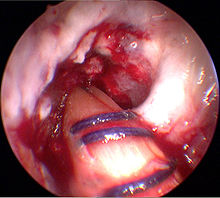
Der eigentliche Eingriff beginnt mit der Einführung des Arthroskops in das Knie des Patienten. Die Diagnose »Kreuzbandriss« kann so nochmals bestätigt werden. Andere Verletzungen, insbesondere des Meniskus, können vor der Rekonstruktion des Kreuzbandes versorgt werden.Entnahme der Sehne
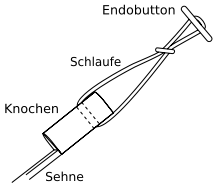
Als erster operativer Eingriff erfolgt die Entnahme der Transplantatsehne. Ein etwa 4 cm langer Hautschnitt am inneren Schienbeinkopf, oberhalb des Pes anserinus, ermöglicht nacheinander die Entnahme der körpereigenen (autologen) Semitendinosus- und Gracilissehne. Die beiden Sehnen werden mit einem so genannten „Sehnenstripper“ entnommen und haben eine Länge von etwa 28 cm. Die Sehnen werden auf einer Spezialvorrichtung vorgespannt und als Mehrfachstrang, beispielsweise „Quadruple“, miteinander vernäht. Die Länge des Transplantates beträgt dann noch etwa 7 cm und hat einen Durchmesser von etwa 7 mm. Das Transplantat wird mittels eines Spezialfadens an den beiden inneren Öffnungen einer ovalen Vier-Loch-Scheibe (Endobutton) befestigt. Der Spezialfaden ist nicht bioresorbierbar.Entfernung der Kreuzbandreste und Bohren der Knochenkanäle
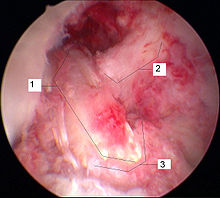
Arthroskopisch werden die Reste des gerissenen vorderen Kreuzbandes entfernt. Dazu wird ein motorgetriebenes Saug-Schneid-Werkzeug verwendet. Mit Hilfe eines Zielgerätes wird die Position zur Bohrung eines Kanals durch den Kopf des Schienbeins anvisiert und anschließend gebohrt. Der Durchmesser des Bohrkanals ist dem Durchmesser des Transplantates angepasst. Durch Kanal des Schienbeins hindurch wird ein Zielgerät für die Bohrung des Oberschenkelknochens angebracht. Mit Unterstützung dieses Zielgeräts wird ein Kanal in den Oberschenkelknochen gebohrt. Dieser Kanal verjüngt sich nach oben und hat eine Länge von etwa 35 mm. Der breitere Teil des Kanals ist für die Aufnahme des Transplantates, der schmälere für den Durchzug der Transplantataufhängung.Einziehen des Transplantates
Mit zwei Zugfäden wird das Transplantat von unten nach oben in die Bohrkanäle eingezogen. Mit Hilfe einer Hohlschraube (Transfix-Schraube) wird das Transplantat am Oberschenkelknochen befestigt. Das aus dem Ende des Schienbeinkanals herausragende Ende wird vorgespannt und mit einer Interferenzschraube (Delta-Schraube) durch Verklemmung fixiert. Abschließend werden die Wunden vernäht. Die Operationsdauer liegt typischerweise im Bereich von 45 bis 90 Minuten.Nach der Operation
Entscheidend für die definitive Funktion ist eine Lagerung direkt postoperativ in Streckposition. Diese sollte 24 Stunden eingehalten werden. Durch diese Lagerung wird ein postoperatives Streckdefizit verhindert, das sich sonst oft ausbildet und zu dessen Beseitigung wochenlange physiotherapeutische Bemühungen notwendig werden können. Am Tag nach der Operation werden üblicherweise die Drainagen aus den Wunden am Knie entfernt. Das operierte Bein darf bis zur fünften Woche nach der Operation nur teilbelastet werden, da das Transplantat in den Bohrkanälen in die Knochen einwachsen muss. Um das in dieser Zeit empfindliche Transplantat zu schützen, wird eine Knieorthese verwendet. Die Rehabilitation kann üblicherweise nach der fünften Woche beginnen.Mögliche Komplikationen nach Rekonstruktionen des vorderen Kreuzbandes
Wie bei jedem chirurgische Eingriff kann es auch bei der Rekonstruktion der Kreuzbänder mit den beiden heute üblichen Transplantaten (Patellasehne und Hamstring) zu Komplikationen kommen. Zu den allgemeinen Risiken bei Operationen, wie beispielsweise Blutungen, Wundinfektionen, Störungen der Wundheilung, Thrombosen, Verletzungen von Gefäßen oder Nerven, addieren sich spezifische Komplikationen. Je nach Autor werden unterschiedliche Komplikationsraten von bis zu 26 Prozent angegeben. Die häufigsten Komplikationen sind dabei das Versagen des Transplantates, beispielsweise durch Ausriss, Re-Ruptur oder Lockerung, und vor allem Bewegungseinschränkungen des Kniegelenks.[221]
Zu den Komplikationen kann auch die zuvor gezeigte Morbidität der Transplantatentnahme gerechnet werden.
- Bewegungseinbuße
- → siehe Hauptartikel Arthrofibrose
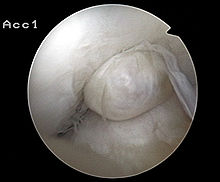 Arthroskopische Aufnahme eines Zyklops im Knie eines Patienten.
Arthroskopische Aufnahme eines Zyklops im Knie eines Patienten.
Ein Zyklops ist eine sekundäre Arthrofibrose und eine mögliche Komplikation einer Kreuzbandrekonstruktion. Bei etwa 2 Prozent aller Patienten ist nach einer Kreuzbandrekonstruktion ein Zyklops die Ursache für eine Einbuße der Beweglichkeit bei der Streckung des Kniegelenks.[222]Bewegungseinbuße ist eine schwer wiegende Komplikation nach der Rekonstruktion des vorderen Kreuzbandes. Sie liegt definitionsgemäß dann vor, wenn bei der Streckung des Beines ein Winkel von 10° nicht unterschritten und bei der Beugung ein Winkel von 125° nicht überschritten werden kann.[223] Der Verlust der Streckfähigkeit des Gelenkes ist häufiger als der der Beugefähigkeit und zudem für den Patienten auch schwerwiegender.[224] Die Ursache für Bewegungseinbußen ist meist eine entzündungsbedingte Vermehrung von Bindegewebe – einer Fibrose; genauer gesagt einer Arthrofibrose.[225]
Transplantatversagen
Die Inzidenz für Transplantatversager liegt bei etwa 4,3 %.[226] Die Ursachen für ein Versagen eines Transplantates lassen sich in drei Gruppen einteilen:[108][227]- chirurgische Fehler,
- biologisches Versagen, bedingt durch mangelhaftes Einheilen des Transplantates und
- erneute Kreuzbandruptur.
In einer Studie waren 52 Prozent der Fälle von Transplantatversagen iatrogen, das heißt durch den Arzt verursachte chirurgische Fehler. Bei 25 Prozent der Fälle führte ein erneuter Riss des Kreuzbandes, bei 8 Prozent eine mangelhafte Inkorporation des Transplantates, bei 3 Prozent eine Bewegungseinschränkung und bei ebenfalls 3 Prozent die verwendeten synthetischen Implantate zum Ausfall. Bei 9 Prozent der Fälle von Transplantatversagen konnte die Ursache nicht genau zugeordnet werden.[228] Generell ist das chirurgische Können des Operateurs für den Erfolg einer Rekonstruktion des vorderen Kreuzbandes von großer Wichtigkeit. Typische chirurgische Fehler sind beispielsweise eine falsche Platzierung des Bohrkanals, eine unzureichende Fixierung des Transplantates, eine ungenügende Spannung des Transplantates und eine unzureichende Notch-Plastik mit konsekutivem Impingement.[108][227]
Die erneute Ruptur des Kreuzbandes kann unter anderem durch eine zu aggressive Rehabilitation, mangelnde Komplianz des Patienten oder zu frühe Wiederaufnahme einer sportlichen Tätigkeit mit zu hoher Belastung für das Implantat verursacht werden.[45]
- Septische Arthrithis
- → siehe Hauptartikel Arthritis
Eine septische Arthritis (bakterielle Arthritis) ist eine relativ seltene, allerdings sehr schwerwiegende Komplikation einer Kreuzbandrekonstruktion. Die Inzidenzraten liegen im Bereich von 0,3 bis 1,7 Prozent.[229][230][231][232][233][234][235] Die septische Arthritis ist mit einer hohen Morbidität, einem meist langwierigen Krankenhausaufenthalt und häufig mit einem schlechten klinischen Ergebnis verbunden.[236]
In einer Studie in den Vereinigten Staaten lag die Rate an schwerwiegenden Infektionen nach einer Kreuzbandrekonstruktion bei 0,75 Prozent. Die Rate lag bei Autografts bei 1,2 und bei Allografts bei 0,6 Prozent.[237] Die Gabe von Antibiotika ist nach postoperativen Infektionen obligat.[238]
In Deutschland werden bei 62 Prozent aller Arthroskopien den Patienten prophylaktisch Antibiotika verordnet, um Infektionen – wie beispielsweise eine septische Arthritis – zu vermeiden.[239]
Andere Komplikationen
Postoperative Thrombosen haben eine Inzidenz von 1,2 Prozent.[226] Außerst selten sind maligne Neoplasien (bösartige Tumore), die sich nach einer Kreuzbandplastik bilden. In der Literatur sind bisher (Stand Juni 2010) lediglich drei Fälle beschrieben.[240][241][242]Therapieperspektiven
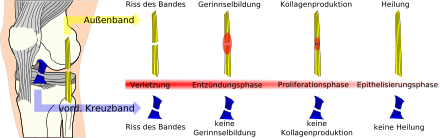 Vergleich des Heilungsprozesses bei einer Innenbandruptur (oben), mit der Nicht-Heilung einer Ruptur des vorderen Kreuzbandes.[94]
Vergleich des Heilungsprozesses bei einer Innenbandruptur (oben), mit der Nicht-Heilung einer Ruptur des vorderen Kreuzbandes.[94]
Die beiden Kreuzbänder sind im Gegensatz zum Innen- und Außenband nicht in der Lage, nach einem Riss durch Ruhigstellung wieder von alleine zusammenzuwachsen. Bei einem Innenbandriss genügt beispielsweise ein Stützband, das etwa sechs Wochen getragen werden muss, damit die beiden Enden vernarben können und der Riss so verheilt. Bei den beiden im Inneren des Knies gelegenen Kreuzbändern ist dies nicht der Fall. Die Ursache hierfür ist nicht genau bekannt. Mehrere Faktoren werden diskutiert. So ist die Synovialflüssigkeit, die die Kreuzbänder umgibt, möglicherweise ein Medium, das einen solchen Heilungsprozess verhindert.[243][244] Ebenso werden Veränderungen des Zellstoffwechsels nach der Verletzung[245][246] und intrinische Defizite, wie beispielsweise in der Genexpression der die Kreuzbänder formenden Zellen, für diesen Effekt verantwortlich gemacht.[247][248][249][250][251][252][253]
Zukünftige Therapiekonzepte setzen daran an, in den Zellen der gerissenen Kreuzbändern die gleichen Fähigkeiten, wie beispielsweise bei den Zellen des Außen- und Innenbands, zu aktivieren.[94] Prinzipiell sind die Zellen der Kreuzbänder, wie beispielsweise die Zellen des Innenbandes, in der Lage nach einer Ruptur zu proliferieren und zu revaskularisieren. Dies wurde histologisch und immunhistochemisch nachgewiesen.[243][254][255] Auch ein Jahr nach der Ruptur sind die Zellen in der Lage, innerhalb der Bandfragmente Kollagen zu produzieren.[256] Auch die Fähigkeit zur Zellmigration in den Wundbereich ist nachgewiesen.[257][258] Dennoch bildet sich im Knie keine Stützstruktur (Scaffold) für den Gewebeaufbau, das die gerissenen Kollagenfaserbündel des Kreuzbandes wieder miteinander verbindet. Die Enden des gerissenen Kreuzbandes wogen ziellos in der Synovialflüssigkeit hin und her.[254] Eine Hypothese geht davon aus, dass das Fehlen von für den Aufbau der Stützstruktur essentiellen extrazellulären Matrixproteinen und Zytokinen im Bereich der Wunde die Selbstheilung verhindert. Ein Indiz hierfür ist, dass beim Heilungsprozess des Innenbandes erhebliche Mengen an Fibrinogen, Fibronektin, Platelet-Derived Growth Factor A (PDGF-A), TGF-β1, Fibroblasten-Wachstumsfaktor (FGF) und Von-Willebrand-Faktor (vWF) nachweisbar sind, die beim Kreuzbandriss fehlen.[259] Trotz der Einblutung bei einem Kreuzbandriss sind keine Fibrin-Plättchen in der Nähe der Verletzung nachweisbar.[260] Eine mögliche Ursache ist die Anwesenheit höherer Konzentrationen des Enzyms Plasmin. Plasmin ist in der Lage die Spaltung von Fibrin (Fibrinolyse) zu katalysieren. Es entsteht durch die verstärkte Expression des Enzyms Urokinase, das wiederum die Umwandlung von Plasminogen in Plasmin katalysiert.[94][261]
Die biologische Stimulation des Aufbaus einer Stützstruktur, die einen Heilungsprozess des gerissenen Kreuzbandes im Knie ermöglicht, ist ein potenzielles zukünftiges Therapiekonzept. Die Gabe von Wachstumsfaktoren wie PDGF, TGF-β und FGF konnte in vitro die Proliferation und Migration, wie auch die Produktion von Kollagen hochregulieren. Im Modellorganismus Kaninchen konnte durch die Injektion von Hyaluronsäure eine erhöhte Gefäßneubildung und eine verstärkte Produktion von Kollagen Typ III beobachtet werden.[262] Im Tiermodell Hausschwein bewirkt die Injektion eines kollagenreichen Hydrogels bei einem genähten Kreuzband einen verbesserten Heilungsprozess, mit einer signifikant erhöhten Bandfestigkeit.[94][263]
Alle diesbezüglichen Konzepte des Tissue Engineerings befinden sich noch in einer präklinischen Phase. Bis zu einer zugelassenen Therapie beim Menschen vergehen erfahrungsgemäß noch über zehn Jahre.
Hintere Kreuzbandrupturen
Die Operation des hinteren Kreuzbandes gestaltet sich erheblich schwieriger als die des vorderen und ist eher die Ausnahme. Die Heilungstendenz ist zudem bei einer konservativen Therapie recht hoch. Ein operativer Eingriff ist meist nur bei komplexen Bandverletzungen des Knies indiziert.[264] Gegenwärtig sind drei konkurrierende operative Verfahren beim hinteren Kreuzbandriss etabliert. Dies sind:[130]
- Die anatomische Rekonstruktion des anterolateralen Hauptbündels in Single-incision-Technik unter Verwendung von Hamstring-Sehnen, wie beispielsweise Musculus semitendinosus[265]
- Die anatomische Rekonstruktion beider Bündel
- Die Tibial-Inlay-Technik[266]
Physiotherapie zur Rehabilitation nach einer Operation
Ziel der Therapie sollte nicht die alleinige Wiederherstellung der Stabilität sein, sondern vielmehr die Erhaltung der gesamten Gelenkfunktion. Das heißt Stabilität, inklusive des Gefühls eines stabilen Kniegelenks, freie Gelenkbewegung und Beschwerdefreiheit.
Nach der Operation wird frühfunktionell beübt (teilweise passiv mittels Motorbewegungsschiene) und die Mobilität des Patienten mit Unterarmgehstützen und unter Umständen mit einer Kniegelenksorthese hergestellt. Im Anschluss erfolgt eine physiotherapeutische Behandlung, die je nach Operationstyp und Schule nach etwa zwei Wochen zur Vollbelastung des operierten Knies führen soll. Es wird empfohlen Anspannungsübungen durchzuführen. Dies soll die Muskelgruppen aktivieren. Etwa ab der dritten Woche kann man mit leichtem Fahrrad fahren beginnen. Nach etwa sechs Wochen können Übungen auf dem Sportkreisel oder Minitrampolin unter Anleitung durchgeführt werden. Sportfähigkeit für leichtes Lauftraining besteht ab zirka dem dritten Monat nach der Operation. Nach etwa sechs Monaten können Belastungen wie beispielsweise Springen hinzukommen.[267] Insgesamt dauert die Rehabilitationsphase im Durchschnitt sechs bis neun Monate, bevor die volle Sportfähigkeit erreicht ist. Die vollständige Einheilung (Remodellisierungsphase) des vorderen Kreuzbands ist erst nach einem Jahr abgeschlossen.[26]
Die Nachbehandlung nach der Operation unterscheidet sich im Wesentlichen nur marginal. Es existieren feste Standards in der physiotherapeutischen Behandlung, die nur unwesentlich differenzieren. Hier sollten auch klare Nachbehandlungsschemata je nach Operationsmethode ihren Niederschlag in der Behandlung finden. Die Erfahrung und Arbeit des Physiotherapeuten ist somit in der Folge für den Heilungsprozess von entscheidender Bedeutung.
Prognose
Auch nach einer optimalen Therapie kann im betroffenen Kniegelenk eine funktionelle Instabilität verbleiben. Diese Instabilität kann zu einer Fehlbelastung des Gelenkkörpers führen und so Folgeschäden verursachen. Typische Folgeschäden sind sekundäre Knorpelschäden, eine Degeneration des Hinterhorns des Innenmeniskus und ein signifikant erhöhtes Risiko einer Kniegelenksarthrose (Gonarthrose).[26][268][269]
Mehrere Studien zeigen, dass nach einem Riss des vorderen Kreuzbandes die Wahrscheinlichkeit zur Ausbildung einer Kniegelenksarthrose deutlich erhöht ist. Etwa 50 bis 70 % der Patienten mit einem Kreuzbandriss zeigen nach 15 bis 20 Jahren radiographische Veränderungen im Knie. Kommen zu dem Kreuzbandriss noch Begleitverletzungen im Knie – wie beispielsweise ein Meniskusriss – hinzu, so steigt die Wahrscheinlichkeit für eine Gonarthrose weiter an.[270][271][272] In diesem Zeitraum hat die Gonarthrose einen Ahlbäck-Grad von I bis II erreicht und ist üblicherweise noch ohne klinische Symptome. Die Progression ist meist relativ langsam. Ältere Studien gehen davon aus, dass in den meisten Fällen vermutlich erst 30 und mehr Jahre nach dem Riss des vorderen Kreuzbandes die Gonarthrose klinisch relevant wird.[273] Andere Studien berichten davon, dass es bereits im Zeitraum 10 bis 20 Jahre nach dem Riss des Kreuzbandes zu funktionellen Einschränkungen des Kniegelenkes, verbunden mit Schmerzen, bedingt durch arthrotische Prozesse im Knie kommen kann. Die Prognose ist aber generell stark abhängig von Alter, Geschlecht, Genetik, Körpergewicht, Muskelstärke,[274] körperlicher Aktivität und möglichen erneuten Verletzungen im Knie.[275][276]
Bei nicht operativ behandelten Kreuzbandrupturen liegt das Risiko für eine Kniegelenksarthrose nach 20 Jahren, über mehrere Studien betrachtet, bei 60 bis 100 %. Im Vergleich dazu haben Patienten mit einer Rekonstruktion des vorderen Kreuzbandes ein 14 bis 16%iges Risiko und bei zusätzlicher Meniskektomie eines von 37 % für eine Gonarthrose.[277]
Bei der Langzeitbetrachtung einer kleinen Kohorte von 19 Spitzensportlern mit Kreuzbandriss hatten nach 35 Jahren 8 der Athleten (=42 %) eine Knieprothese.[277]
Prävention
Ein Kreuzbandriss hat für den Betroffenen erhebliche ernste Konsequenzen. Diese Art der Verletzung ist daher eine der am meisten von Sportlern gefürchteten.[278] Für Berufs- und Leistungssportler bedeutet ein Kreuzbandriss – trotz immer weiter verbesserter Behandlungsmöglichkeiten – eine langwierige Trainings- und Wettkampfpause. Bis in die 1990er Jahre führte ein Kreuzbandriss meist zum Karriereende.[279] Für Berufssportler, sowie ihre Vereine und Sponsoren, sind nach wie vor beträchtliche Einnahmeeinbußen die Folge. In der Regel dauert es nach Wiederherstellung der Bänder und Wiederbeginn der Wettkampftätigkeit weitere Monate, bis das ursprüngliche Leistungsniveau des Sportlers wieder erreicht wird. Im Amateur- und Hobbybereich des Sports entstehen für die Gesellschaft durch Arbeitsausfallzeiten, Behandlung und Rehabilitationsmaßnahmen erhebliche Kosten, zu denen sich noch die langfristig entstehenden Kosten durch vorzeitige Kniegelenksarthrosen addieren.
Der Prävention, also der Vermeidung, eines Kreuzbandrisses kommt daher eine immer bedeutendere Rolle zu. Grundsätzlich erscheint es als möglich, dass durch bestimmte Trainingsmethoden die Wahrscheinlichkeit eines Kreuzbandrisses gesenkt werden kann. Da eine Reihe von Pathomechanismen, die einen Kreuzbandriss begünstigen, aber noch nicht ausreichend verstanden ist, ist noch weitgehend unklar, welche Übungen einen präventiven Charakter haben oder gar warum sie das Verletzungsrisiko senken.[280] Es werden daher mittlerweile in vielen Ländern große Forschungsanstrengungen unternommen, um zum einen die Risikofaktoren und Pathomechanismen eines Kreuzbandrisses aufzuklären und zum anderen daraus abgeleitet mit geeigneten Maßnahmen dieser Verletzungsart begegnen zu können.[39][281]
Spezielle Übungen
Beispiel für einen Sportkreisel. Normalweise wird dieses Trainingsgerät barfuß benutzt.
Bisher gibt es keine standardisierten Übungen, um Kreuzbandrissen ohne Fremdeinwirkung vorzubeugen. In einigen Studien zeigte es sich, dass vielseitigere Übungsprogramme einen größeren positiven Effekt zeigen als einzelne Übungen. Plyometrische Übungen für die unteren Extremitäten, Dehngymnastik (Stretching), zur gezielten Beherrschung des Rumpfes, zur gestärken Wahrnehmung der Körperbewegung (Propriozeption) und zur verbesserten Entscheidungsfindung, scheinen positive Effekte in der Prävention zu haben. Dadurch werden die Kräfte bei der Landung des Sportlers nach einem Sprung ebenso reduziert wie die Momente, die bei Varus/Valgus einwirken. Zudem werden Muskeln aktiviert, die Kraftmomente, die auf das Knie einwirken, teilweise mit abfangen können.[281]
In einer Studie mit über 1400 Fußballspielerinnen konnte ein positiver Effekt durch spezielles Aufwärmen (warm-up) erreicht werden. Gegenüber der Kontrollgruppe nahm die Anzahl an vorderen Kreuzbandrissen insgesamt um den Faktor 1,7 ab. Betrachtet man nur die Kreuzbandrisse ohne Fremdeinwirkung, so lag in der Gruppe mit dem speziellen Aufwärmprogramm die Häufigkeit sogar um den Faktor 3,3 niedriger. Der Schwerpunkt der Aufwärmübung liegt auf der neuromuskulären Kontrolle des Kniegelenkes.[282][283] In anderen Studien konnte elektromyografisch nachgewiesen werden, dass neuromuskuläre Übungen positive Effekte auf den Musculus semitendinosus vor Absprung und Landung eines Sportlers haben.[284][285][286]
Zu ähnlich positiven Ergebnissen kommt eine Studie aus Italien. Mitte der 1990er Jahre nahmen insgesamt 600 Fußballspieler aus 40 Mannschaften des Halbprofi- beziehungsweise Amateurbereichs teil. Die Hälfte der Mannschaften trainierte jeden Tag zusätzlich 20 Minuten nach einem speziellen sensomotorischen Trainingsprogramm, das propriozeptive Elemente enthielt.[287] Die Übungen wurden beispielsweise mit einem Balance-Board durchgeführt. Über drei Spielsaisons wurde die Häufigkeit von Verletzungen der vorderen Kreuzbänder beobachtet. Bei den Teilnehmern an dem speziellen Trainingsprogramm war die Inzidenz einer Kreuzbandverletzung signifikant niedriger als in der Kontrollgruppe.[288] Einige Autoren sehen in dieser Studie den Beweis für einen prophylaktischen Effekt des koordinativen Trainings.[289][290] Übliche propriorezeptive Trainingsmittel sind beispielsweise „Wackelbretter“ und „Sportkreisel“. Diese geben dem Trainierenden einen instabilen Untergrund, wodurch dieser ständig gezwungen ist, seinen Körper im Gleichgewicht zu halten.[289]
Eine andere evidenzbasierte Studie aus Norwegen, mit über 1800 Handballspielern im Alter von 15 bis 17 Jahren, zeigt ebenfalls, dass durch ein strukturiertes Aufwärmprogramm mit neuromuskulären Übungselementen die Inzidenz von Kreuzbandrissen um über 50 % gesenkt werden kann. Zum Einsatz kamen hierbei unter anderem Balancematten.[291] Eine 2005 von der Universität Münster veröffentlichte Studie mit über 250 deutschen Handballspielerinnen kommt ebenfalls zu dem Ergebnis, dass propriozeptive und neuromuskuläre Übungen die Häufigkeit von Kreuzbandrupturen erheblich reduzieren können.[292]
Eine Reihe von Sportwissenschaftlern plädiert dafür, dass solche präventiven Übungselemente integraler Bestandteil von Trainingseinheiten in Sportarten mit erhöhter Inzidenz für Kreuzbandrupturen werden.[291][293][294]
Andere Präventionsmaßnahmen
Eine Regeländerung zu Beginn der Saison 2005 bewirkte in der Australian Football League, dass die Häufigkeit für einen hinteren Kreuzbandriss um mehr als den Faktor zwei gesenkt werden konnte. Die Regeländerung bestand darin, den Anlauf des Ruckman auf das Anstoßquadrat zu begrenzen.[295]
Tiermedizin
- → siehe Hauptartikel Kreuzbandruptur bei Kleintieren
Von den Haustieren ist insbesondere der Haushund häufig von Rupturen des vorderen Kreuzbandes betroffen. Allerdings spielen hier andere, nicht traumatische, Pathomechanismen eine große Rolle. Seltener sind Kreuzbandrisse bei Hauskatzen.
Medizingeschichtliches
Hippokrates von Kos beschrieb eine Subluxation des Knies, die er auf eine Bandverletzung im Knie zurückführte. Galenos beschrieb detailliert die Wichtigkeit der Bänder zur Stabilisierung des Knies und für einen normalen Bewegungsablauf beim Gehen. Zuvor meinte man noch, dass es sich bei den Kreuzbändern um „Nervenstrukturen“ handelt. Auf Galenos geht auch der heute noch gültige Name genu cruciata, mit dem er die das Knie stabilisierenden Strukturen bezeichnete, zurück.[140]
Bis in das 19. Jahrhundert hinein wurden zwar ausführlich die Luxationen des Knies und ihre Behandlung beschrieben, die Funktion der Bänder im Knie wurde aber in dem Sammelbegriff Dérangement intern völlig unterbewertet.[296] Die Wittenberger Brüder Wilhelm Eduard und Eduard Friedrich Weber beschrieben 1835 in ihrem Werk Mechanik der menschlichen Gehwerkzeuge[297] ausführlich die biomechanischen Zusammenhänge der Komponenten innerhalb des Knies und in seiner Peripherie. Bei ihren Forschungsarbeiten untersuchten sie die abnorme Bewegung des Schienbeins in einem Knie ohne Kreuzbänder. Sie beschrieben so als Erste den durch einen Kreuzbandriss entstehenden abnormalen Bewegungsablauf beim Gehen.[298]
Der Franzose Amédée Bonnet beschrieb 1845 in seiner 1300 Seiten umfassenden Monographie Traité des maladies des articulations[299] (deutscher Titel von 1851: Zur Behandlung von Gelenkerkrankungen) seine an Leichen vorgenommenen Studien. Er stellte unter anderem fest, dass das vordere Kreuzband in den meisten Fällen an seiner femoralen (am Oberschenkel) Insertion reißt und die Ruptur von einem krachenden Geräusch begleitet wird. Das mediale Seitenband würde durch Valgusbeugungsstress auch an seinem femoralen Ansatz reißen. Bonnet erkannte auch, dass ein blutiger Gelenkerguss (Hämarthros) und der Schmerz wichtige Symptome des vorderen Kreuzbandrisses sind. Die Ursache der Schmerzen sah er in der Dehnung der Ligamentnerven. Über die Inzidenz schrieb er, dass „Rupturen der Ligamente viel häufiger sind als allgemein angenommen.“. Bonnet erwähnte auch als Erster das Phänomen der Subluxation („… des déplacements qui font croire à une luxation incomplète”), das erst wieder zu Beginn der 1970er Jahre von R. D. Galway und D. L. MacIntosh als Pivot Shift aufgegriffen wurde.[300][301][302] In seinem 1853 veröffentlichten Buch Traité de thérapeutique des maladies articulaires[303] schrieb Bonnet, dass eine zu lange Ruhigstellung des betroffenen Knies sich negativ auf den Heilungsprozess auswirke. Gegen die knorpelschädigende Wirkung einer Immobilisierung entwickelte er erste Geräte zur aktiven Bewegung.[140] In seinen Ausführungen zur Behandlung akuter Verletzungen war er der damaligen Zeit weit voraus. So schlug Bonnet beispielsweise kalte Packungen zur Erstversorgung der Verletzung und eine baldige, leichte Bewegung vor.[298] Im gleichen Buch beschreibt Bonnet eine Orthese mit zwei Scharnieren für Patienten mit Riss des vorderen Kreuzbandes.[140][304][305]
Die Verletzung des vorderen Kreuzbandes wurde erstmals 1850 von dem Briten J. Stark auf konservative Weise mittels eines Gipsverbandes behandelt.[144][306][307]
Der knöcherne Ausriss des vorderen Kreuzbandes, bei dem die ligamentären Strukturen unverletzt sind, wurde 1875 von französischen Chirurgen Poncet beschrieben.[164] Poncet obduzierte die Leiche eines durch einen Fenstersturz aus dem dritten Stock Verunglückten.[308]
Der Engländer Arthur Mayo Robson (1853–1933)[309] führte 1895 an einem 41-jährigen Minenarbeiter aus Featherstone – Mayo Robson nennt ihn in seiner Veröffentlichung acht Jahre später „J. B.“ – erstmals eine Kreuzbandnaht durch. Der Patient hatte sich 36 Wochen zuvor bei einem Unfall in einer Kohlengrube am Knie verletzt. Am 21. November 1895 öffnete Mayo Robson das Knie von J. B.. Dabei stellte er fest, dass beide Bänder vollständig abgerissen waren und fixierte sie mit Catgut („Katzendarm“). Das vordere Kreuzband nähte er dabei an die Gelenkinnenhaut und an Gewebe der inneren Seite des äußeren Kondylus. Das hintere Kreuzband befand er als zu kurz, weshalb er es aufteilte, um eine ausreichende Länge zu erhalten. Dann fixierte er es an der Gelenkinnenhaut und am Knorpelgewebe der äußeren Seite des inneren Kondylus. Anschließend schloss er die Wunde mit Catgut und die Oberfläche mit Seidendarm. Knapp sechs Jahre später, am 24. Oktober 1901, besuchte ein Mitarbeiter von Mayo Robson den Patienten, der sein operiertes Bein als perfectly strong beschrieb und seinen alten Beruf wieder voll ausüben konnte. Schmerzen hatte er nur, wenn er das Knie bei der Arbeit zu sehr belastete. Der Umfang beider Knie war identisch.[310] Auch andere Veröffentlichungen empfahlen im Fall einer akuten Ruptur die primäre Kreuzbandnaht. Der Berliner Arzt H. Goetjes veröffentlichte 1913 die erste Sammelstatistik über 30 Fälle mit primärer Kreuzbandnaht, die zu einem positiven Ergebnis kam.[311][312] Eine erste Kritik am Nähen der Bänder kam bereits 1916 durch Robert Jones, einen britischen Militärorthopäden. Jones hielt das Nähen der Bänder für völlig nutzlos und sah in der natürlichen Vernarbung die einzige verlässliche Reparatur.[144][313] Ungeachtet dieser Kritik sollte sich die primäre Kreuzbandnaht noch über 60 weitere Jahre halten, wurde sie doch von zahlreichen Autoren bestätigt und empfohlen.[314][315][316][317][318]
1976 veröffentlichten John A. Feagin und Walton W. Curl das Ergebnis einer fünfjährigen Langzeitstudie, die sie über Soldaten an der Militärakademie West Point anfertigten.[139] 64 Kadetten hatten sich während ihrer Collegezeit einer Naht des vorderen Kreuzbandes unterzogen. Die Langzeitergebnisse waren ausgesprochen negativ, so dass in der Folgezeit die primäre Naht des Kreuzbandes ohne Augmentation als Therapie mehr und mehr zugunsten der Rekonstruktion des vorderen Kreuzbandes aufgegeben wurde.[140][145][146][147][148][149] Spätere Studien bestätigten die Ergebnisse dieser Studie.Der aus Australien stammende Chirurg James Hogarth Pringle beschrieb 1907 an der Glasgow Royal Infirmary erstmals eine Reposition an einem Lebenden, die er 1903 durchgeführt hatte: „The joint was then opened into, the blood and fluid in it washed out, and it was at once seen that the anterior crucial ligament still attached to its bone insertion had been torn off the tibia and taken the spine with it; with a little trouble this was sutured, and the wound closed.“[30][319]
Ebenfalls 1903 verwendet der Münchener Fritz Lange Seidenfäden, zur Verstärkung beziehungsweise als Ersatz des vorderen Kreuzbandes.[320] Der Schweizer Eugen Bircher führte 1921 im Kantonsspital Aarau die erste Arthroskopie durch.
Die erste Rekonstruktion eines vorderen Kreuzbandes beim Menschen wurde vermutlich 1914 von dem russischen Chirurgen Grekow vorgenommen. Nach der Beschreibung von Erich Hesse verwendete Grekow freie Streifen von Fascia lata, einer Bindegewebshülle des Oberschenkels.[321] Drei Jahre später verwendete der britische Chirurg Ernest William Hey Groves (1872–1944) einen gestielten Streifen des Tractus iliotibialis zur Kreuzbandrekonstruktion. Den Streifen führte er dabei durch zwei Bohrkanäle, die vom Epicondylus zur Fossa intercondylica, sowie vom Schienbein zur Eminentia intercondylica reichten. Damit legte er den Grundstein für die moderne Bandchirurgie.[322][323][324][325]
Der erste Ersatz eines Kreuzbandes durch ein Patellasehnen-Transplantat erfolgte 1935 durch den Deutschen A. Wittek,[326] nachdem drei Jahre zuvor der Marinechirurg zur Verth dies auf dem Kongress der Deutschen Orthopädischen Gesellschaft in Mannheim vorschlug.[327]
1926 beschrieb Edwards, dass eine Rekonstruktion mit den Sehnen des M. semitendinosus und des M. gracilis möglich sei.[328] Lindemann führte 1950 dann erstmals eine Kreuzbandrekonstruktion mit diesen Sehnen durch.[316]
Kenneth Jones verwendete 1963 als Erster ein distal gestieltes Transplantat des mittleren Drittels der Patellasehne. Dieses präparierte er zusammen mit dem Knochenblock in ganzer Länge aus der Patella. Das Transplantat zog er distal ohne Bohrkanal unter dem Hoffa-Fettkörper hindurch. Auf der proximalen Seite zog er es durch einen Bohrkanal im Bereich der Kreuzbandhöhle hindurch.[329] Die erste Beschreibung eines BTB-Transplantates stammt vermutlich von dem deutschen Arzt Helmut Brückner aus dem Jahr 1966.[330] Die Arbeiten von Jones und Brückner bilden die Grundlagen der heutigen Kreuzbandchirurgie. Im deutschen Sprachraum spricht man daher oft auch von einer Brückner- oder Brückner-Jones-Plastik.
Weiterführende Literatur
Fachbücher
- W. Petersen und T. Zantop: Das vordere Kreuzband: Grundlagen und aktuelle Praxis der operativen Therapie. Deutscher Ärzteverlag, 2009, ISBN 3-769-10562-1 Eingeschränkte Vorschau in der Google Buchsuche
- M. J. Strobel und A. Weiler: Hinteres Kreuzband. Anatomie, Diagnostik und Operationstechnik. 1. Auflage, Endo Press, 2008, ISBN 3-89756-719-9
- N. P. Südkamp und A. Weiler: Ligamentäre Kniegelenksverletzungen und Meniskusverletzungen. In: Praxis der Unfallchirurgie W. Mutschler und N. P. Haas (Herausgeber), 2. Auflage, Thieme, 2007, S. 466–467. ISBN 3-13-101151-3
- A. Hüter-Becker: Lehrbuch zum neuen Denkmodell der Physiotherapie – Band 1 Bewegungssystem. 2. Auflage, Thieme Verlag, 2006, ISBN 3-13-130142-2 Eingeschränkte Vorschau in der Google Buchsuche
- A. Wilcke: Vordere Kreuzbandläsion. Verlag Birkhäuser, 2004, ISBN 3-7985-1404-6 Eingeschränkte Vorschau in der Google Buchsuche
- J. Jerosch und J. Heisel: Das Kniegelenk – Rehabilitation nach Verletzungen und operativen Eingriffen. Pflaum Verlag, 2004, ISBN 3-7905-0911-6
- M. J. Strobel: Arthroskopische Chirurgie. 1. Auflage, Springer, 1998, ISBN 978-3-540-63571-0 Eingeschränkte Vorschau in der Google Buchsuche
Übersichtsartikel (Reviews)
- O. Gorschewsky: Das Vordere Kreuzband.
- H. J. Eichhorn und W. Birkner: Aktuelle Trends zur Rekonstruktion des vorderen Kreuzbandes. (PDF)
- P. Renström und J. Kelm: Vorderes Kreuzband – Operation und Rehabilitation. In: Deutsche Zeitschrift für Sportmedizin 58, 2007, S. 392–394.
- M. M. Murray: Current status and potential of primary ACL repair. In: Clin Sports Med 28, 2009, S. 51–61. PMID 19064165
- Y. Shimokochi und S. J. Shultz: Mechanisms of noncontact anterior cruciate ligament injury. In: J Athl Train 43, 2008, S. 396–408. PMID 18668173
- T. E. Hewett u. a.: Dynamic neuromuscular analysis training for preventing anterior cruciate ligament injury in female athletes. In: Instr Course Lect 56, 2007, S. 397–406. PMID 17472323
- C. D. Harner u. a.: Anterior and posterior cruciate ligament reconstruction in the new millennium: a global perspective. In: Knee Surg Sports Traumatol Arthrosc 9, 2001, S. 330–336. PMID 11734868
Weblinks
-
 Commons: Kreuzbandriss – Sammlung von Bildern, Videos und Audiodateien
Commons: Kreuzbandriss – Sammlung von Bildern, Videos und Audiodateien - Leitlinie Vordere Kreuzbandruptur . In: AWMF online
- Übersicht: Die vordere Kreuzbandruptur (Ärztemagazin)
- Diashow einer Kreuzbandrekonstruktion
Einzelnachweise
- ↑ a b c d e W. Petersen und T. Zantop: Das vordere Kreuzband: Grundlagen und aktuelle Praxis der operativen Therapie. Verlag Deutscher Ärzteverlag, 2009, ISBN 3-769-10562-1 Eingeschränkte Vorschau in der Google Buchsuche
- ↑ J. C. Hughston u. a.: Classification of knee ligament instabilities. Part I. The medial compartment and cruciate ligaments. In: J Bone Joint Surg Am 58, 1976, S. 159–172. PMID 1254619
- ↑ medrapid.info: anteromediale Rotationsinstabilität im Kniegelenk. Abgerufen am 30. März 2010
- ↑ medrapid.info: anterolaterale Rotationsinstabilität im Kniegelenk. Abgerufen am 30. März 2010
- ↑ medrapid.info: posterolaterale Rotationsinstabilität im Kniegelenk. Abgerufen am 30. März 2010
- ↑ G. L. Lucas u. a.: A primer of biomechanics. Verlag Springer, 1999, ISBN 0-387-98456-9
- ↑ E. Luciani: Eine in-vitro-Studie über die Zugkräfte im vorderen Kreuzband und vorderen Kreuzband-Ersatz (Ligamentum patellae- und Semitendinosus-Plastik). Dissertation, LMU München, 2003
- ↑ C. F. Ettlinger u. a.: A method to help reduce the risk of serious knee sprains incurred in alpine skiing. In: Am J Sports Med 23, 1995, S. 531–537. PMID 8526266
- ↑ a b c C. J. Wirth u. a.: Orthopädie und orthopädische Chirurgie. Knie. Georg Thieme Verlag, 2005, ISBN 3-131-26231-1 Seite. 153f.Eingeschränkte Vorschau in der Google Buchsuche
- ↑ a b c C. Fink u. a.: Arthroseentwicklung nach Ruptur des vorderen Kreuzbandes. In: Der Unfallchirurg 97, 1994, S. 357–361. PMID 7939737
- ↑ a b P. Hochstein u. a.: Diagnostik und Inzidenz der Verletzungen des hinteren Kreuzbandes. In: Der Unfallchirurg 102, 1999, S. 753–762. doi:10.1007/s001130050477 PMID 10525618
- ↑ H. Monma und T. Sugita: Is the mechanism of traumatic posterior dislocation of the hip a brake pedal injury rather than a dashboard injury? In: Injury 32, 2002, S. 221–222. PMID 11240298
- ↑ A. T. Janousek u. a.: Posterior cruciate ligament injuries of the knee joint. In: Sports Med 28, 1999, S. 429–441. PMID 10623985 (Review)
- ↑ C. Haasper u. a.: Knee injuries in restrained car drivers in German road traffic accidents. In: J Trauma 65, 2008, S. 136–141. PMID 18580510
- ↑ a b c S. Bollen: Epidemiology of knee injuries: diagnosis and triage. In: Br J Sports Med 34, 2000, S. 227–228. doi:10.1136/bjsm.34.3.227-a PMID 10854030
- ↑ a b c d Gesundheitsdirektion des Kantons Zürich: Ruptur des vorderen Kreuzbandes: operative oder konservative Behandlung? Bericht vom 30. Juni 2009
- ↑ J. M. Hootman u. a.: Epidemiology of collegiate injuries for 15 sports: summary and recommendations for injury prevention initiatives. In: J Athl Train 42, 2007, S. 311–319. PMID 17710181 (Review)
- ↑ D. Gehring: Kniegelenkskontrolle bei dynamischen Bewegungen - Einfluss von Geschlecht, Ermüdung und Equipment Dissertation, Albert-Ludwigs-Universität Freiburg i. Br., 2009
- ↑ J. P. Nicholl u. a.: Injuries in sport and exercise. Verlag Sports Council, 1991, ISBN 1-872158-71-4
- ↑ a b A. Wilcke: Vordere Kreuzbandläsion. Verlag Birkhäuser, 2004, ISBN 3-7985-1404-6 S. 37. Eingeschränkte Vorschau in der Google Buchsuche
- ↑ K. Miyasaka u. a.: The incidence of knee ligament injuries in the general population. In: Am J Knee Surg 4, 1991, S. 3–8.
- ↑ S. Rupp und D. Kohn: Vorderes Kreuzband im Mittelpunkt des Interesses. In: Orthopäde 31, 2002. S. 701. doi:10.1007/s001320200000 PMID 12426747
- ↑ a b L. Y. Griffin u. a. Noncontact anterior cruciate ligament injuries: risk factors and prevention strategies. In: J Am Acad Orthop Surg 8, 2000, S. 141–150. PMID 10874221 (Review)
- ↑ a b L. J. Huston u. a.: Anterior cruciate ligament injuries in the female athlete. Potential risk factors. In: Clin Orthop Relat Res 372, 2000, S. 50–63. PMID 10738414 (Review)
- ↑ Statistisches Bundesamt, Zweigstelle Bonn, Krankheitskostenrechnung: Krankheitskosten 2002 für die Diagnose M23 (Binnenschädigung des Kniegelenkes) in der Einrichtung Krankenhaus nach Geschlecht und Alter.
- ↑ a b c M. B. Gothner: Der Einfluss der Ruptur des vorderen Kreuzbandes auf die RHCL. Dissertation, Universität Ulm, 2006
- ↑ B. Wagner: Kreuzbandriss: Auf wackligen Knien. In: Der Stern vom 13. April 2006
- ↑ E. Arendt und R. Dick: Knee injury patterns among men and women in collegiate basketball and soccer: NCAA data and review of literature. In: Am J Sports Med 23, 1995, S. 694–701. PMID 8600737 (Review)
- ↑ J. W. Powell und K. D. Barber-Foss: Sex-related injury patterns among selected high school sports. In: Am J Sports Med 28, 2000, S. 385–391. PMID 10843133
- ↑ a b C. Becker: Biomechanische Untersuchungen unterschiedlicher Fixationsmethoden zur tibialen Reinsertion knöcherner Ausrisse des vorderen Kreuzbandes. Dissertation, Westfälische Wilhelms-Universität Münster, 2005.
- ↑ T. E. Hewett u. a.: Effects of the menstrual cycle on anterior cruciate ligament injury risk: a systematic review. In: Am J Sports Med 35, 2007, S. 659–668. PMID 17293469 (Review)
- ↑ S. D. Barber-Westin u. a.: Reducing the risk of noncontact anterior cruciate ligament injuries in the female athlete. In: Phys Sportsmed 37, 2009, S. 49–61. PMID 20048528 (Review)
- ↑ T. E. Hewitt: Predisposition to ACL Injuries in Female Athletes Versus Male Athletes. In: Orthopedics 31, 2008, S. 26–28. PMID 18269164
- ↑ a b R. A. Magnussen u. a.: Cross-cultural comparison of patients undergoing ACL reconstruction in the United States and Norway. In: Knee Surg Sports Traumatol Arthrosc 18, 2010, S. 98–105. PMID 19784630
- ↑ a b S. Kesting: Patellarsehne versus Semitendinosus-/Gracilis-Sehne als Ersatz zur Rekonstruktion des vorderen Kreuzbandes – 5-Jahres-Ergebnisse eines randomisierten Patientenkollektivs – eine klinische Studie. Dissertation, Universitätsklinikum Münster, 2008
- ↑ a b A. Wilcke: Vordere Kreuzbandläsion. Verlag Birkhäuser, 2004, ISBN 3-7985-1404-6 S. 38. Eingeschränkte Vorschau in der Google Buchsuche
- ↑ M. H. Lam u. a.: Knee stability assessment on anterior cruciate ligament injury: Clinical and biomechanical approaches. In: Sports Med Arthrosc Rehabil Ther Technol 1, 2009, 20. PMID 19712449 (Review im Open Access)
- ↑ G. Hughes und J. Watkins: A risk-factor model for anterior cruciate ligament injury. In: Sports Med 36, 2006, S. 411–428. PMID 16646629 (Review)
- ↑ a b E. Alentorn-Geli u. a.: Prevention of non-contact anterior cruciate ligament injuries in soccer players. Part 1: Mechanisms of injury and underlying risk factors. In: Knee Surg Sports Traumatol Arthrosc 17, 2009, S. 705–729. PMID 19452139 (Review)
- ↑ M. Waldén u. a.: High risk of new knee injury in elite footballers with previous anterior cruciate ligament injury. In: Br J Sports Med 40, 2006, S. 158–162. PMID 16432004
- ↑ a b c P. Swärd u. a.: Risk factors for a contralateral anterior cruciate ligament injury. In: Knee Surg Sports Traumatol Arthrosc 18, 2010, S. 277–291. PMID 20062970 (Review)
- ↑ O. Faude u. a.: Injuries in female soccer players: a prospective study in the German national league. In: Am J Sports Med 33, 2005, S. 1694–1700. PMID 16093546
- ↑ a b J. Orchard u. a.: Intrinsic and extrinsic risk factors for anterior cruciate ligament injury in Australian footballers. In: Am J Sports Med 29, 2001, S. 196–200. PMID 11292045
- ↑ N. Pujol u. a.: The incidence of anterior cruciate ligament injuries among competitive Alpine skiers: a 25-year investigation. In: Am J Sports Med 35, 2007, S. 1070–1074. PMID 17468379
- ↑ a b L. Salmon u. a.: Incidence and risk factors for graft rupture and contralateral rupture after anterior cruciate ligament reconstruction. In: Arthroscopy 21, 2005, S. 948–957. PMID 16084292
- ↑ O. Faude u. a.: Risk factors for injuries in elite female soccer players. In: Br J Sports Med 40, 2006, S. 785–790. PMID 16825269
- ↑ A. M. Chaudhari u. a.: Anterior cruciate ligament-injured subjects have smaller anterior cruciate ligaments than matched controls: a magnetic resonance imaging study. In: Am J Sports Med 37, 2009, S. 1282–1287. PMID 19307330
- ↑ E. J. Comerford u. a.: Distal femoral intercondylar notch dimensions and their relationship to composition and metabolism of the canine anterior cruciate ligament. In: Osteoarthritis Cartilage 14, 2006, S. 273–278. PMID 16242971
- ↑ K. D. Shelbourne u. a.: The relationship between intercondylar notch width of the femur and the incidence of anterior cruciate ligament tears. A prospective study. In: Am J Sports Med 26, 1998, S. 402–408. PMID 9617403
- ↑ H. Lund-Hanssen u. a.: Intercondylar notch width and the risk for anterior cruciate ligament rupture. A case-control study in 46 female handball players. In: Acta Orthop Scand 65, 1994, S. 529–532. PMID 7801756
- ↑ J. M. Uhorchak u. a.: Risk factors associated with noncontact injury of the anterior cruciate ligament: a prospective four-year evaluation of 859 West Point cadets. In: Am J Sports Med 31, 2003, S. 831–842. PMID 14623646
- ↑ T. O. Souryal und T. R. Freeman: Intercondylar notch size and anterior cruciate ligament injuries in athletes. A prospective study. In: Am J Sports Med 21, 1993, S. 535–539. PMID 8368414
- ↑ K. D. Shelbourne u. a.: Radiographic and intraoperative intercondylar notch width measurements in men and women with unilateral and bilateral anterior cruciate ligament tears. In: Knee Surg Sports Traumatol Arthrosc 5, 1997, S. 229–233. PMID 9430572
- ↑ S. Lombardo u. a.: Intercondylar notch stenosis is not a risk factor for anterior cruciate ligament tears in professional male basketball players: an 11-year prospective study. In: Am J Sports Med 33, 2005, S. 29–34. PMID 15610996
- ↑ M. S. Schickendantz und G. G. Weiker: The predictive value of radiographs in the evaluation of unilateral and bilateral anterior cruciate ligament injuries. In: Am J Sports Med 21, 1993, S. 110–113. PMID 8427350
- ↑ T. J. Davis u. a.: Correlation of the intercondylar notch width of the femur to the width of the anterior and posterior cruciate ligaments. In: Knee Surg Sports Traumatol Arthrosc 7, 1999, S. 209–214. PMID 10462209
- ↑ M. Dienst u. a.: Correlation of intercondylar notch cross sections to the ACL size: a high resolution MR tomographic in vivo analysis. In: Arch Orthop Trauma Surg 127, 2007, S. 253–260. PMID 16807752
- ↑ T. Friden u. a.: Review of knee proprioception and the relation to extremity function after an anterior cruciate ligament rupture. In: J Orthop Sports Phys Ther 31, 2001, S. 567–576. PMID 11665744 (Review)
- ↑ A. C. Thomas, R. M. Palmieri-Smith, S. G. McLean: Isolated hip and ankle fatigue are unlikely risk factors for anterior cruciate ligament injury. In: Scand J Med Sci Sports [elektronische Veröffentlichung vor dem Druck], 2010, PMID 20136750.
- ↑ S. G. McLean und J. E. Samorezov: Fatigue-induced ACL injury risk stems from a degradation in central control. In: Med Sci Sports Exerc 41, 2009, S. 1661–1672. PMID 19568192
- ↑ C. B. Swanik u. a.: The relationship between neurocognitive function and noncontact anterior cruciate ligament injuries. In: Am J Sports Med 35, 2007, S. 943–948. PMID 17369562
- ↑ A. V. Dowling u. a.: Shoe-surface friction influences movement strategies during a sidestep cutting task: implications for anterior cruciate ligament injury risk. In: Am J Sports Med 38, 2010, S. 478–485. PMID 9338947
- ↑ G. Myklebust u. a.: Registration of cruciate ligament injuries in Norwegian top level team handball. A prospective study covering two seasons. In: Scand J Med Sci Sports 7, 1997, S. 289–292. PMID 9338947
- ↑ J. W. Orchard und J. W. Powell: Risk of knee and ankle sprains under various weather conditions in American football. In: Med Sci Sports Exerc 35, 2003, S. 1118–1123. PMID 12840631
- ↑ J. Orchard u. a.: Rainfall, evaporation and the risk of non-contact anterior cruciate ligament injury in the Australian Football League. In: Med J Aust 170, 1999, S. 304–306. PMID 10327970
- ↑ J. W. Orchard u. a.: Rye grass is associated with fewer non-contact anterior cruciate ligament injuries than bermuda grass. In: Br J Sports Med 39, 2005, S. 704–709. PMID 16183765
- ↑ J. Löhnert und J. Raunest: Arthroskopische Chirurgie des Kniegelenkes. Wissenschaftliche Verlagsgesellschaft Regensberg & Biermann, 1985, ISBN 3-924469-10-5
- ↑ A. Wilcke: Vordere Kreuzbandläsion. Verlag Birkhäuser, 2004, ISBN 3-7985-1404-6 S. 75. Eingeschränkte Vorschau in der Google Buchsuche
- ↑ P. Segond: Recherches cliniques et expérimentales sur les épanchements sanguins du genou par entorse. In: Prog Med 16, 1879, S. 297–299, 320–321, 340–341, 379–381, 400–401, 419–421.
- ↑ F. Adam: Knie. In: Orthopädie und orthopädische Chirurgie. D. Kohn (Herausgeber), Georg Thieme Verlag, 2005, ISBN 3-13-126231-1 S. 62. Eingeschränkte Vorschau in der Google Buchsuche
- ↑ a b C. Elliger-Wimber: Objektive Scores bei Ersatz des vorderen Kreuzbandes mit Patellar-Sehne oder Semitendinosus-Gracilis-Sehne. Dissertation, Westfälische Wilhelms-Universität zu Münster, 2003
- ↑ K. D. Shelbourne und T. Gray: Anterior cruciate ligament reconstruction with autogenous patellar tendon graft followed by accelerated rehabilitation. A two- to nine-year followup. In: Am J Sports Med 25, 1997, S. 786–795. PMID 9397266
- ↑ P. Aglietti u. a.: Arthroscopic partial meniscectomy in the anterior cruciate deficient knee. In: Am J Sports Med 16, 1988, S. 597–602. PMID 3071151 (Review)
- ↑ V. J. Cooley u. a.: Quadrupled semitendinosus anterior cruciate ligament reconstruction: 5-year results in patients without meniscus loss. In: Arthroscopy 17, 2001, S. 795–800. PMID 11600975
- ↑ F. Escalas u. a.: T-Fix anchor sutures for arthroscopic meniscal repair. In: Knee Surg Sports Traumatol Arthrosc 5, 1997, S. 72–76. PMID 9228311
- ↑ W. D. Cannon und J. M. Vittori: The incidence of healing in arthroscopic meniscal repairs in anterior cruciate ligament-reconstructed knees versus stable knees. In: Am J Sports Med 20, 1992, S. 176–181. PMID 1558246
- ↑ F. R. Noyes und S. D. Barber-Westin: Arthroscopic repair of meniscus tears extending into the avascular zone with or without anterior cruciate ligament reconstruction in patients 40 years of age and older. In: Arthroscopy 16, 2000, S. 822–829. PMID 11078538
- ↑ R. H. Brophy u. a.: Anterior cruciate ligament reconstruction and concomitant articular cartilage injury: incidence and treatment. In: Arthroscopy 26, 2010, S. 112–120. PMID 20117635
- ↑ N. Hartnett und R. J. Tregonning: Delay in diagnosis of anterior cruciate ligament injury in sport. In: N Z Med J 114, 2001, S. 11–13. PMID 11243663
- ↑ a b S. R. Bollen und B. W. Scott: Anterior cruciate ligament rupture: a quiet epidemic? In: Injury 27, 1996, S. 407–409. PMID 8881137
- ↑ F. R. Noyes u. a.: Knee sprains and acute knee hemarthrosis: misdiagnosis of anterior cruciate ligament tears. In: Phys Ther 60, 1980, S. 1596–1601. PMID 7454786
- ↑ K. D. Shelbourne und D. A. Foulk: Treatment of anterior Cruciate Ligament injuries. Prinicples and practice of orthopaedic Sport Medicine. W. E. Garrett u. a. (Editors), Lippincott Williams & Wilkins, Philadelphia, 2000, ISBN 0-7817-2578-X S. 743–761.
- ↑ S. J. Kim und H. K. Kim: Reliability of the anterior drawer test, the pivot shift test and the Lachman test. In: Clin Orthop Relat Res 317, 1995, S. 237–242. PMID
- ↑ D. P. König u. a.: Diagnosis of anterior knee instability. Comparison between the Lachman test, the KT-1000 arthrometer and the ultrasound Lachman test. In: Unfallchirurg 101, 1998, S. 209–213. PMID 9577218
- ↑ W. Schwarz u. a.: Manual ultrasound of the knee joint. A general practice method for diagnosis of fresh rupture of the anterior cruciate ligament. In: Unfallchirurg 100, 1997, S. 280–285. PMID 9229778
- ↑ K. J. O’Shea u. a.: The Diagnostic accuracy of history, physical examination, and radiographs in the evaluation of traumatic knee disorders. In: Am J Sports Med 24, 1996, S. 164–167. PMID 8775114
- ↑ H. J. Gelb u. a.: Magnetic resonance imaging of knee disorders: clinical value and cost effectiveness in a sports medicine practice. In: Am J Sports Med 24, 1996, S. 99–103. PMID 8638763
- ↑ F. Rayan: Clinical, MRI, and arthroscopic correlation in meniscal and anterior cruciate ligament injuries. In: Int Orthop 33, 2009, S. 129–132. PMID 18297284
- ↑ Y. Kocabey u. a.: The value of clinical examination versus magnetic resonance imaging in the diagnosis of meniscal tears and anterior cruciate ligament rupture. In: Arthroscopy 10, 2004, S. 696–700. PMID 15346110
- ↑ S. Thomas u. a.: The value of magnetic resonance imaging in our current management of ACL and meniscal injuries. In: Knee Surg Sports Traumatol Arthrosc 15, 2007, S. 533–536. PMID 17225179
- ↑ a b R. Crawford u. a.: Magnetic resonance imaging versus arthroscopy in the diagnosis of knee pathology, concentrating on meniscal lesions and ACL tears: a systematic review. In: Br Med Bull 84, 2007, S. 5–23. PMID 17785279 (Review)
- ↑ N. Glynn u. a.: Trends in utilization: has extremity MR imaging replaced diagnostic arthroscopy? In: Skelet Radiol 33, 2004, S. 272–276. doi:10.1007/s00256-004-0750-5
- ↑ K. Wörtler: MRT des Kniegelenks. In: Der Radiologe 47, 2007, S. 1131–1143. doi:10.1007/s00117-007-1581-x PMID 17992501
- ↑ a b c d e M. M. Murray: Current status and potential of primary ACL repair. In: Clin Sports Med 28, 2009, S. 51–61. PMID 19064165 (Review)
- ↑ G. A. Murell u. a.: The effects of time course after anterior cruciate ligament injury in correlation with meniscal and cartilage loss. In: Am J Sports Med 29, 2001, S. 9–14. PMID 11206263
- ↑ H. Ross u. a.: Osteoarthritis of the knee after injury to the anterior cruciate ligament and meniscus: the influence of time and age. In: Osteoarthritis Cartil 3, 1995, S. 261–267. PMID 8689461
- ↑ C. Fink u. a.: Langzeitergebnisse nach konservativer oder operativer Therapie der vorderen Kreuzbandruptur. In: Der Unfallchirurg 99, 1996, S. 964–969. doi:10.1007/s001130050081
- ↑ a b P. P. Casteleyn und F. Handelberg: Non-operative management of the anterior cruciate ligament injuries in the general population. In: Bone It Surg 78, 1996, S. 446–451. PMID 8636184
- ↑ a b c C. B. Frank und D. W. Jackson: The science of reconstruction of the anterior cruciate ligament. In: J Bone Joint Surg Am 79, 1997, S. 1556–1576. PMID 9378743 (Review)
- ↑ R. Johnson u. a.: The treatment of injuries of the anterior cruciate ligament. In: J Bone Joint Surg 74, 1992, S. 140–151. PMID 1734005 (Review)
- ↑ F. Noyes u. a.: The variable functional disability of the anterior cruciate ligament-deficient knee. In: Orthop Clin N Am 16, 1985, S. 47–67. PMID 3881716 (Review)
- ↑ C. Andersson u. a.: Knee function after surgical and nonsurgical treatment of acute rupture of the anterior cruciate ligament: A randomized study with a long-term follow-up period. In: Clin Orthop 264, 1991, S. 255–263. PMID 1997243
- ↑ W. Clancy u. a.: Acute tears of the anterior cruciate ligament. Surgical versus conservative treatment. In: J Bone Joint Surg 70, 1988, S. 1483–1488. PMID 3198673
- ↑ P. Neyret u. a.: Partial meniscectomy and anterior cruciate ligament rupture in soccer players. A study with a minimum 20-year followup. In: Am J Sports Med 21, 1993, S. 455–460. PMID 8346763
- ↑ H. Roos u. a.: Soccer after anterior cruciate ligament injury – an incompatible combination? A national survey of incidence and risk factors and a 7-year follow-up of 310 players. In: Acta Orthop Scand 66, 1995, S. 107–112. PMID 7740937
- ↑ L. Rosenberg und M. Sherman: Meniscal injury in the anterior cruciate-deficient knee. A rational for clinical decision-making. In: Sports Med 13, 1992, S. 423–432. PMID 1615259
- ↑ a b c d e f g h i j k l m n o p A. Weiler: Anatomische „Hamstringsehnen“ Verankerung mit Interferenzschrauben beim Kreuzbandersatz. Habilitationsschrift, Humboldt-Universität zu Berlin, 2002
- ↑ a b c d e f g M. Schettle: Vergleich der vorderen Kreuzbandplastik durch das mittlere Patellarsehnendrittel Allograft mit dem mittleren Patellarsehnendrittel Autograft bei Revisionseingriffen. Dissertation, LMU München, 2008
- ↑ a b c G. Gremion u. a.: Konservative Behandlung bei einem vorderen Kreuzbandriss – Ergebnisse. In: Orthopädie Technik 1, 2002, S. 99–101.
- ↑ W. J. McDaniel und T. B. Dameron: The untreated anterior cruciate ligament rupture. In: Clin Orthop Relat Res 172, 1983, S. 158–163. PMID 6821986
- ↑ B. D. Beynnon u. a.: Treatment of anterior cruciate ligament injuries, part I. In: Am J Sports Med 33, 2005, S. 1579–1602. PMID 16199611 (Review)
- ↑ B. D. Beynnon u. a.: Treatment of anterior cruciate ligament injuries, part II. In: Am J Sports Med 33, 2005, S. 1751–1761. PMID 16230470 (Review)
- ↑ S. Hinterwimmer u. a.: Operative vs. konservative Therapie der vorderen Kreuzbandruptur: eine systematische Literaturübersicht. In: Der Unfallchirurg 106, 2003, S. 374–379. doi:10.1007/s00113-003-0596-7 (Review)
- ↑ R. H. Wittenberg u. a.: A comparison of conservative and delayed surgical treatment of anterior cruciate ligament ruptures. A matched pair analysis. In: Int Orthop 22, 1998, S. 145–148. PMID 9728304
- ↑ H. Seitz u. a.: Langzeitergebnisse nach vorderem Kreuzbandersatz im Vergleich zur konservativen Therapie. In: Chirurg 65, 1994, S. 992–998. PMID 7821082
- ↑ C. Andersson u. a.: Knee function after surgical or nonsurgical treatment of acute rupture of the anterior cruciate ligament: a randomized study with a long-term follow-up period. In: Clin Orthop Relat Res 264, 1991, S. 255–263. PMID 1997243
- ↑ E. Linko u. a.: Surgical versus conservative interventions for anterior cruciate ligament ruptures in adults. In: Cochrane Database Syst Rev 2005, CD001356. PMID 15846618
- ↑ C. Fink u. a.: Long-term outcome of operative or nonoperative treatment of anterior cruciate ligament rupture - is sports activity a determining variable? In: Int J Sports Med 22, 2001, S. 304–309. PMID 11414676
- ↑ P. J. Fowler und W. D. Regan: The patient with symptomatic chronic anterior cruciate ligament insufficiency. In: Am J Sports Med 15, 1987, S. 321–325. PMID 3661812
- ↑ T. P. Giove u. a.: Non-operative treatment of the torn anterior cruciate ligament. In: J Bone Jt Surg 65, 1985, S. 184–192. PMID 6822581
- ↑ a b R. J. Hawkins u. a.: Follow up of the acute nonoperated isolated anterior cruciate ligament tear. In: Am J Sports Med 14, 1986, S. 205–210. PMID 3752360
- ↑ D. J. Beard u. a.: Proprioception enhancement for anterior cruciate deficiency. A prospective trial of two physiotherapy regimes. In: Bone Surg 76, 1994, S. 654–659. PMID 8027158
- ↑ H. Ihara und A. Nakayama: Dynamic joint control training for knee ligament injuries. In: Am J Sports Med 14, 1986, S. 309–315. PMID 3728783
- ↑ P. Kannus und M. Jarvinen: Conservatively treated tears of the anterior cruciate ligament. In: J Bone Joint Surg Am 69, 1987, S. 1007–1012. PMID 3654691
- ↑ R. Sandberg u. a.: Operative vervus non-operative treatment of recent injuries. A prospective randomized Study. In: J Bone Jt Surg 69, 1987, S. 1120–1126. PMID 3312204
- ↑ J. R. Steadman u. a.: A minimally invasive technique ("healing response") to treat proximal ACL injuries in skeletally immature athletes. In: J Knee Surg 19, 2006, S. 8–13. PMID 16468488
- ↑ R. Steadman u. a.: Healing-response treatment for ACL injuries. In: Orthop Technol Rev 3, 2002, 3
- ↑ K. Fehske u. a.: Die Healing Response Technik – eine suffiziente Therapieoption bei Partialrupturen des vorderen Kreuzbandes? 9/2009, Leipzig, Arbeitsgemeinschaft für Arthroskopie, S. 24.
- ↑ a b Franziskus Krankenhaus Linz am Rhein: Vorderer Kreuzbandriss / Kreuzbandinsuffiz. Abgerufen am 12. März 2010
- ↑ a b D. Altmann: Operativer Standard bei frischen Kreuzbandverletzungen. In: Trauma und Berufskrankheit 8, 2006, S. S150–S154. doi:10.1007/s10039-006-1156-5
- ↑ Universitätsklinikum Gießen und Marburg: Neueste Behandlungsoptionen beim vorderen Kreuzbandriss. In: Newsletter vom 6. Mai 2006
- ↑ W. G. Rodkey u. a.: Healing of a surgically created partial detachment of the posterior cruciate ligament using marrow stimulation: an experimental study in dogs. In: J Knee Surg 19, 2006, S. 14–18. PMID 16468489
- ↑ M. J. Blyth u. a.: Anterior cruciate ligament reconstruction in patients over the age of 50 years: 2- to 8-year follow-up. In: Knee Surg Sports Traumatol Arthrosc 11, 2003, S. 204–211. PMID 12761610
- ↑ a b F. Dirisamer: Patienteninformation: Diagnose Kreuzbandriß. Abgerufen am 4. Februar 2010
- ↑ L. P. Granan u. a.: The Scandinavian ACL registries 2004-2007: baseline epidemiology. In: Acta Orthop 80, 2009, S. 563–567. PMID 19916690
- ↑ J. Kennedy u. a.: Timing of reconstruction of the anterior cruciate ligament in athletes and the incidence of secondary pathology within the knee. In: J Bone Joint Surg Br 92, 2010, S. 362–366. PMID 20190306
- ↑ J. C. Yoo u. a.: Increasing incidence of medial meniscal tears in nonoperatively treated anterior cruciate ligament insufficiency patients documented by serial magnetic resonance imaging studies. In: Am J Sports Med 37, 2009, S. 1478–1483. PMID 19359417
- ↑ P. J. Millett u. a.: Associated injuries in pediatric and adolescent anterior cruciate ligament tears: does a delay in treatment increase the risk of meniscal tear? In: Arthroscopy 18, 2002, S. 955–959. PMID 12426537 (Review)
- ↑ a b J. Feagin und W. Curl: Isolated tear of the anterior cruciate ligament. 5-year follow-up study. In: Am J Sports Med 4, 1976, S. 95–100. PMID 984289
- ↑ a b c d e H. H. Pässler und A. Driessen: Die Geschichte der Kreuzbandchirurgie. In: ATOSNews 11, 2008, S. 50–61.
- ↑ N. Kaplan u. a.: Primary surgical treatment of anterior cruciate ligament ruptures. A long-term follow-up study. In: Am J Sports Med 18, 1999, S. 354–358. PMID 2206080
- ↑ M. Odensten u. a.: Suture of fresh ruptures of anterior cruciate ligament. A 5-year follow-up. In: Acta Orthop Scand 55, 1984, S. 270–272. PMID 6377805
- ↑ K. Sommerlath u. a.: The long-term course after treatment of acute anterior cruciate ligament ruptures. A 9-to 16-year follow-up. In: Am J Sports Med 19, 1991, S. 156–162. PMID 2039067
- ↑ a b c C. Eberhardt u. a.: Geschichte der Chirurgie des vorderen Kreuzbandes. In: Orthopäde 31, 2002, S. 702–709, doi:10.1007/s00132-002-0329-6.
- ↑ a b C. Fink u. a.: Langzeitergebnisse nach konservativer oder operativer Therapie der vorderen Kreuzbandruptur. In: Unfallchirurg 99, 1996, S. 964–969, doi:10.1007/s001130050081
- ↑ a b T. Grøntvedt et al.: A prospective randomized study of three operations for acute rupture of the anterior cruciate ligament. Five-year follow-up of one hundred and thirty-one patients. In: J Bone Joint Surg Am 78, 1996, S. 159–168. PMID 8609105
- ↑ a b P. Hertel: Frische und alte Kniebandverletzungen. In: Unfallchirurg 99, 1996, S. 686–700. ISSN 0177-5537
- ↑ a b H. Seiler und H. R. Frank: Naht am vorderen Kreuzband – was ist die Methode tatsächlich wert? In: Unfallchirurg 96, 1993, S. 443–450, PMID 8235679.
- ↑ a b F. Schmid und W. Bandi: Die Verletzung des medialen Seitenbandes (MSB) und des vorderen Kreuzbandes (VKB) am Kniegelenk und ihre operativ-funktionelle Behandlung nach Lemaire. In: European Journal of Trauma 14, 1988, S. 124–129, doi:10.1007/BF02806640.
- ↑ a b R. Becker u. a.: Die vordere Kreuzbandplastik – Transplantatwahl und Verankerungstechniken. In: Zentralbl Chir 127, 2002, S. 842–849. doi:10.1055/s-2002-35128 PMID 12410449
- ↑ N. Kaplan u. a.: Primary surgical treatment of anterior cruciate ligament ruptures. A long-term follow-up study. In: Am J Sports Med 18, 1990, S. 354–358. PMID 2206080
- ↑ T. Strand u. a.: Long-term follow-up after primary repair of the anterior cruciate ligament: clinical and radiological evaluation 15-23 years postoperatively. In: Arch Orthop Trauma Surg 125, 2005, S. 217–221. PMID 15875231
- ↑ T. Gomez u. a.: Semitendinosus repair augmentation of acute anterior cruciate ligament rupture. In: Can J Sports Sci 15, 1990, S. 137–142. PMID 2383818
- ↑ G. Hehl u. a.: Clinical experience with PDS II augmentation for operative treatment of acute proximal ACL reptures - 2-year follow-up. In: Knee Surg Sports Traumatol Arthrosc 7, 1999, S. 102–106. PMID 10223532
- ↑ W. Holzmüller u. a.: Mechanische Eigenschaften PDS-augmentier- ter Patellarsehnentransplantate zur. Rekonstruktion des vorderen Kreuzbandes. In: Unfallchirurg 95, 1992, S. 306–310. PMID 1636112
- ↑ W. Holzmüller u. a.: Histologische Untersuchungen zum Ersatz des vorderen Kreuzbands mit PDS-augmentierten Patellarsehnentransplantaten. In: Unfallchirurg 97, 1994, S. 144–150. PMID 8178182
- ↑ R. Kdolsky u. a.: Synthetic augmented repair of proximal ruptures of the anterior cruciate ligament. Long-term results of of 66 patients. In: Clin Orthop 295, 1993, S. 183–189. PMID 8403646
- ↑ K. E. Rehm und K. H. Schultheis: Bandersatz mit Polydioxanon (PDS) In: Unfallchirurgie 11, 1985, S. 264–273. PMID 3934825
- ↑ J. Amirault u. a.: Chronic anterior cruciate ligament deficiency. Long-term results of MacIntohs’s lateral substitution reconstruction. In: J Bone Joint Surg 70, 1988, S. 622–624. PMID 3403611
- ↑ R. Bray u. a.: Reconstruction for chronic anterior cruciate instability. A comparison of two methods after six years. In: J Bone Joint Surg 70, 1988, S. 100–105. PMID 3339039
- ↑ C. Frank und D. Jackson: Lateral substitution for chronic isolated anterior cruciate ligament deficiency. In: J Bone Joint Surg 70, 1988, S. 407–411. PMID 3372561
- ↑ J. Reid u. a.: The Ellison iliotibial-band transfer for a torn anterior cruciate ligament of the knee: Long-term follow-up. In: J Bone Joint Surg 74, 1992, S. 1392–1402. PMID 1429795
- ↑ T. Vail u. a.: Long-term functional results in patients with anterolateral rotatory instability treated by iliotibial band transfer. In: Am J Sports Med 20, 1992, S. 274–282. PMID 1636857
- ↑ a b T. Engel u. a.: Interligamentäre Ruptur und knöcherner Ausriß des vorderen Kreuzbands. In: Arthroskopie 13, 2000, S. 66–68, doi:10.1007/s001420050122.
- ↑ M. Krüger-Franke u. a.: Die arthroskopische vordere Kreuzbandrekonstruktion – was ist gesichert 2009? In: Sport-Orthopädie - Sport-Traumatologie 25, 2009, S. 206–211. doi:10.1016/j.orthtr.2009.06.002
- ↑ a b M. Schuhmacher: Veränderungen ausgewählter Parameter der Kniegelenkmechanik vor und nach operativem Ersatz des vorderen Kreuzbandes bei unterschiedlichen Operationstechniken. Dissertation, Deutsche Sporthochschule Köln, 2007
- ↑ M. Quante und E. Hille: Propriozeption: Eine kritische Analyse zum Stellenwert in der Sportmedizin. In: Dtsch Z Sportmed 50, 1999, S. 306–310.
- ↑ a b J. Höher und T. Tiling: Differenzierte Transplantatauswahl in der Kreuzbandchirurgie. In: Chirurg 71, 2000, S. 1045–1054. doi:10.1007/s001040051180 PMID 11043122
- ↑ J. Brand u. a.: Current concepts: Graft fixation in cruciate ligament surgery. In: Am J Sports Med 28, 2000, S. 761–774. PMID 11032238 (Review)
- ↑ Leitlinien der Deutschen Gesellschaft für Unfallchirurgie: Vordere Kreuzbandruptur. Stand der letzten Aktualisierung: 5/2008
- ↑ T. R. Duquin u. a.: Current trends in anterior cruciate ligament reconstruction. In: J Knee Surg 22, 2009, S. 7–12. PMID 19216345
- ↑ C. Lüring u. a.: Therapie der vorderen Kreuzbandruptur des Kniegelenks. In: Sportverl Sportschad 18, 2004, S. 119–124. doi:10.1055/s-2004-813174
- ↑ W. Franz und J. Ulbrich: Eine neue Technik zur Entnahme der Semitendinosussehne für den Kreuzbandersatz. In: Arthroskopie 17, 2004, S. 104–107. doi:10.1007/s00142-004-0255-1
- ↑ H. Steckel u. a.: The double-bundle technique for anterior cruciate ligament reconstruction: a systematic overview. In: Scand J Med Sci Sports 17, 2007, S. 99–108. PMID 17076829 (Review)
- ↑ C. Chen u. a.: Arthroscopic anterior cruciate ligament reconstruction with quadriceps tendon-patellar bone autograft. In: J Trauma 46, S. 1999, S. 678–682. PMID 10217233
- ↑ P. Reich: Patellasehnendrittel Autograft versus Allograft beim Ersatz des Vorderen Kreuzbandes. Dissertation, Ludwigs-Maximilians-Universität München, 2007
- ↑ D. Drez u. a.: Anterior cruciate ligament reconstruction using bone-patellar tendon-bone allografts. A biological and biomechanical evaluation in goats. In: Am J Sports Med 19, 1991, S. 256–263. PMID 1714244
- ↑ B. M. Fideler u. a.: Gamma irradiation: effect on biomechanical properties of human bone-patellar tendon-bone allografts. In: Am J Sports Med 23, 1995, S. 643–646. PMID 8526284
- ↑ D. Jackson u. a.: Intraartikular reactions associated with the use of freeze-dried, ethylene oxid-sterilized bone-patellar tendon-bone allografts in the reconstruction of the anterior cruciate ligament. In: Am J Sports Med 18, 1990, S. 1–11. PMID
- ↑ T. S. Roberts u. a.: Anterior cruciate ligament reconstruction using freeze-dried, ethylen oxide-sterilized bone-patellar tendon-bone allografts. In: Am J Sports Med 19, 1991, S. 35–41. PMID 2301680
- ↑ D. Jackson u. a.: A comparison of patellar tendon autograft and allograft used for anterior cruciate ligament reconstruction in the goat model. In: Am J Sports Med 21, 1993, S. 176–185. PMID
- ↑ P. Nikolaou u. a.: Anterior cruciate ligament allograft transplantation: Long-term function, histology, revsacularization and operative technique. In: Am J Sports Med 14, 1986, S. 348–360. PMID
- ↑ J. L. Carey u. a.: A systematic review of anterior cruciate ligament reconstruction with autograft compared with allograft. In: J Bone Joint Surg Am 91, 2009, S. 2242–2250. PMID 19724004 (Review)
- ↑ K. F. Almqvist u. a.: A long-term study of anterior cruciate ligament allograft reconstruction. In: Knee Surg Sports Traumatol Arthrosc 17, 2009, S. 818–822. PMID 19421736
- ↑ K. Sun u. a.: Anterior cruciate ligament reconstruction with bone-patellar tendon-bone autograft versus allograft. In: Arthroscopy 25, 2009, S. 750–759.
- ↑ D. A. McGuire und S. D. Hendricks: Allograft tissue in ACL reconstruction. In: Sports Med Arthrosc 17, 2009, S. 224–233. PMID 19910780 (Review)
- ↑ F. Fu u. a.: Graft selection for anterior cruciate ligament reconstruction. In: Instr Course Lect 58, 2009, S. 337–354. PMID 19385547
- ↑ K. Kumar und N. Maffulli: The ligament augmentation device: an historical perspective. In: Arthroscopy 15, 1999, S. 422–432. PMID 10355719 (Review)
- ↑ L. E. Paulos u. a.: The GORE-TEX anterior cruciate ligament prosthesis. A long-term followup. In: Am J Sports Med 20, 1992, S. 246–252. PMID 1636852
- ↑ L. Claes u. a.: Biological response to ligament wear particles. In: J Appl Biomater 6, 1995, S. 35–41. PMID 7703536
- ↑ a b K. Jenson und W. Klein: Probleme und Komplikationen beim künstlichen Kreuzbandersatz. In: Arthroskopie 3, 1990, S. 15–23.
- ↑ W. Klein und K. Jenson: Synovitis and artificial ligaments. In: Arthroscopy 8, 1992, S. 116–124. PMID 1532312
- ↑ D. Stengel u. a.: Resorbable screws versus pins for optimal transplant fixation (SPOT) in anterior cruciate ligament replacement with autologous hamstring grafts: rationale and design of a randomized, controlled, patient and investigator blinded trial (ISRCTN17384369). In: BMC Surgery 5, 2005, 1. doi:10.1186/1471-2482-5-1 PMID 15723704 (Open Access)
- ↑ S. Fromm: Rekonstruktion des vorderen Kreuzbands (VKB) mit Knochen-Sehnen-Knochen-Transplantat unter Verwendung des ENDOBUTTON CL BTB-Fixationssystems. Broschüre der Smith & Nephew GmbH
- ↑ S. Konan und F. S. Haddad: A clinical review of bioabsorbable interference screws and their adverse effects in anterior cruciate ligament reconstruction surgery. In: The Knee 16, 2009, S. 6–13. PMID 18639461 (Review)
- ↑ a b H. H. Paessler und D. S. Mastrokalos: Anterior cruciate ligament reconstruction using semitendinosus and gracilis tendons, bone patellar tendon, or quadriceps tendon-graft with press-fit fixation without hardware. A new and innovative procedure. In: Orthop Clin North Am 34, 2003, S. 49–64. PMID 12735201 (Review)
- ↑ N. P. Südkamp und N. P. Haas: Neue Wege in der Kreuzbandchirurgie. In: Der Chirurg 71, 2000, S. 1024–1033. doi:10.1007/s001040051178 PMID 11043120
- ↑ P. Aglietti u. a.: Patellofemoral problems after intraarticular anterior cruciate ligament reconstruction. In: Clin Orthop 288, 1993, S. 195–204. PMID 8458134
- ↑ L. Paulos u. a.: Infrapatellar contracture syndrom: An unrecognizedcause of knee stiffness with patella entrapment and patella infera. In: Am J Sports Med 15, 1987, S. 331–341. PMID 3661814
- ↑ J. Kartus u. a. Complications following arthroscopic anterior cruciate ligament reconstruction. A 2–5 year follow-up of 604 patients with special emphasis on anterior knee pain. In: Knee Surg Sports Traumatol Arthrosc 7, 1999, S. 2–8. PMID 10024955
- ↑ a b J. Rosenberg u.a.: Extensor mechanism function after patellar tendon graft harvest for anterior cruciate ligament reconstruction. In: Am J Sports Med 18, 1990, S. 560–565. PMID 1443318
- ↑ R. Bartlett u. a.: Graft selection in reconstruction of the anterior cruciate ligament. In: J Bone Joint Surg 83, 2001, S. 625–634. PMID 11476294
- ↑ a b I. Corry u. a.: Arthroscopic reconstruction of the anterior cruciate ligament: A comparison of patellar tendon autograft and four-strand hamstring tendon autograft. In: Am J Sports Med 27, 1999, S. 444–454. PMID 10424213
- ↑ J. Kartus u. a.: Factors affecting donor-site morbidity after anterior cruciate ligament reconstruction using bone-patellar tendon-bone autografts. In: Knee Surg Sports Traumatol Arthrosc 5, 1997, S. 222–228. PMID 9430571
- ↑ T. Muellner u. a.: Shortening of the patella tendon after anterior cruciate ligament reconstruction. In: Arthroscopy 14, 1998, S. 444–454. PMID 9754477
- ↑ B. Shaffer und J. Tibone: Patellar tendon length change after anterior cruciate ligament reconstruction using the midthird patellar tendon. In: Am J Sports Med 21, 1993, S. 633–646. PMID 8346762
- ↑ T. Järvelä u. a.: The incidence of patellofemoral osteoarthritis and associated findings 7 years after anterior cruciate ligament reconstruction with a bone-patellar tendon-bone autograft. In: Am J Sports Med 29, 2001, S. 18–24. PMID 11206250
- ↑ a b J. Feller u. a.: Early post-operative morbidity following anterior cruciate ligament reconstruction: patellar tendon versus hamstring graft. In: Knee Surg Sports Traumatol Arthrosc 9, 2001, S. 260–266. PMID 11685356
- ↑ A. Lipscomb u. a.: Evaluation of hamstring strength following use of semitendinosus and gracilis tendons to reconstruct the anterior cruciate ligament. In: Am J Sports Med 10, 1982, S. 340–342. PMID 7180953
- ↑ a b K. Yasuda u. a.: Graft site morbidity with autogenous semitendinosus and gracilis tendons. In: Am J Sports Med 23, 1995, S. 706–714. PMID 8600739
- ↑ Y. Hsieh u. a.: The effects of removal and reconstruction of the anterior cruciate ligament on patellofemoral kinematics. In: Am J Sports Med 26, 1998, S. 201–209. PMID 9548113
- ↑ R. Viola u. a.: Internal and external tibial rotation strength after anterior cruciate ligament reconstruction using ipsilateral semidentinosus and gracilis tendon autograft. In: Am J Sports Med 28, 2000, S. 552–555. PMID 10921649
- ↑ K. Eriksson u. a.: The semitendinosus tendon regenerates after resection: a morphologic and MRI analysis in 6 patients after resection for anterior crucaite ligament reconstrcution. In: Acta Orthop Scand 72, 2001, S. 379–384. PMID 11580127
- ↑ K. Eriksson u. a.: Semitendinosus tendon regeneration after harvesting for ACL reconstruction. A prospective MRI study. In: Knee Surg Sports Traumatol Arthrosc 7, 1999, S. 220–225. PMID 10462211
- ↑ P. Papandrea u. a.: Regeneration of the semitendinosus tendon harvested for anterior cruciate ligament reconstruction. Evaluation using ultrasonography. In: Am J Sports Med 28, 2000, S. 556–561. PMID 10921650
- ↑ D. M. Rispoldi u. a.: Magnetic resonance imaging at different time periods following hamstring harvest for anterior cruciate ligament reconstruction. In: Arthroscopy 17, 2001, S. 2–8. PMID 11154359
- ↑ P. Simonian u. a.: Assessment of morbidity of semitendinosus and gracilis tendon harvest for ACL reconstruction. In: Am J Knee Surg 10, 19997, S. 54–59. PMID 9131234
- ↑ A. Comley und J. Krishnan: Donor site morbidity after quadriceps tendon harvest for rotator cuff repair. In: Aust N Z J Surg 69, 1999, S. 808–810. PMID 10553971
- ↑ W. Konermann und R. Haaker: Navigation und Robotic in der Gelenk- und Wirbelsäulenchirurgie. Verlag Springer, 2002, ISBN 3-540-43305-8 Eingeschränkte Vorschau in der Google Buchsuche
- ↑ T. Frietsch und A. Weiler-Lorentz (Herausgeber): Anästhesie in der Traumatologie und Orthopädie. Verlag Elsevier, Urban&Fischer, 2009, ISBN 3-437-24450-7 S. 44. Eingeschränkte Vorschau in der Google Buchsuche
- ↑ P. Lobenhoffer und J. D. Agneskirchner: Vorderes Kreuzband – was ist gesichert? In: Arthroskopie 18, 2005, S. 11–14. doi:10.1007/s00142-004-0290-y
- ↑ J. Wang und Y. Ao: Analysis of different kinds of cyclops lesions with or without extension loss. In: Arthroscopy 25, 2009, S. 626–631. PMID 19501293
- ↑ C. D. Harner u. a.: Loss of motion after anterior cruciate ligament reconstruction. In: Am J Sports Med 20, 1992, S. 499–506. PMID 1443315
- ↑ J. M. Marzo u. a.: Intraarticular fibrous nodule as a cause of loss of extension following anterior cruciate ligament reconstruction. In: Arthroscopy 8, 1992, S. 10–18. PMID 1550639
- ↑ K. E. DeHaven u. a.: Arthrofibrosis of the knee following ligament surgery. In: Instr Course Lect 52, 2003, S. 369–381. PMID 12690864 (Review)
- ↑ a b T. Weig: Bewegungseinschränkung nach vorderer Kreuzbandrekonstruktion (Ursachenanalyse, Therapieergebnisse). Dissertation, LMU München, 2002
- ↑ a b M. Fagelman und K. B. Freedman: Revision reconstruction of the anterior cruciate ligament: evaluation and management. In: Am J Orthop 34, 2005, S. 319–328. PMID 16130349 (Review)
- ↑ E. W. Carson u. a.: Revision anterior cruciate ligament reconstruction: etiology of failures and clinical results. In: J Knee Surg 17, 2004, S. 127–132. PMID 15366266
- ↑ R. T. Burks u. a.: Treatment of postoperative anterior cruciate ligament infections with graft removal and early reimplantation. In: Am J Sports Med 31, 2003, S. 414–418. PMID 12750136
- ↑ S. Y. Fong und J. L. Tan: Septic arthritis after arthroscopic anterior cruciate ligament reconstruction. In: Ann Acad Med Singap 33, 2004, S. 228–234. PMID 15098639
- ↑ P. F. Indelli u. a.: Septic arthritis in postoperative anterior cruciate ligament reconstruction. In: Clin Orthop Rel Res 398, 2002, S. 182–188. PMID 11964649
- ↑ D. R. McAllister u. a.: Outcomes of postoperative septic arthritis after anterior cruciate ligament reconstruction. In: Am J Sports Med 27, 1999, S. 562–570. PMID 10496570
- ↑ R. Viola u. a.: An unusual epidemic of Staphylococcus-negative infections involving anterior cruciate ligament reconstruction with salvage of the graft and function. In: Arthroscopy 16, 2000, S. 173–177. PMID 10705329
- ↑ R. J. Williams u. a.: Septic arthritis after arthroscopic anterior cruciate ligament reconstruction: diagnosis and management. In: Am J Sports Med 25, 1997, S. 261–267. PMID 9079185
- ↑ C. Wang u. a.: Septic arthritis after arthroscopic anterior cruciate ligament reconstruction: a retrospective analysis of incidence, presentation, treatment, and cause. In: Arthroscopy 25, 2009, S. 243–249. PMID 19245985
- ↑ G. Mouzopoulos u. a.: Septic knee arthritis following ACL reconstruction: a systematic review. In: Knee Surg Sports Traumatol Arthrosc 17, 2009, S. 1033–1042. PMID 19381611 (Review)
- ↑ L. M. Katz u. a.: A retrospective comparison of the incidence of bacterial infection following anterior cruciate ligament reconstruction with autograft versus allograft. In: Arthroscopy 24, 2008, S. 1330–1335. PMID 19038702
- ↑ D. Judd u. a.: Infections following arthroscopic anterior cruciate ligament reconstruction. In: Arthroscopy 22, 2006, S. 375–384. PMID 16581449
- ↑ R. Müller-Rath, E. Ingenhoven, T. Mumme, M. Schumacher, O. Miltner: Perioperative management in outpatient arthroscopy of the knee joint. In: Z Orthop Unfall 148, 2010, S. 282–287 PMID 20135619.
- ↑ T. Efe u. a.: Malignant fibrous histiocytoma of the distal femur after an arthroscopic anterior cruciate ligament reconstruction: A case report and a review of the literature. In: BMC Cancer 10, 2010, 264 doi:10.1186/1471-2407-10-264 (Open Access)
- ↑ F. Sirveaux u. a.: Pleomorphic malignant fibrous histiocytoma at the site of an arthroscopic reconstruction of the anterior cruciate ligament. A case report. In: J Bone Joint Surg Am 87, 2005, S. 404–409. PMID 15687167
- ↑ J. J. Caron u. a.: Leiomyosarcoma of the distal femur after anterior cruciate ligament reconstruction. In: Clin Orthop Relat Res 419, 2004, S. 214–217. PMID 15021157
- ↑ a b S. L. Woo u. a.: Healing and repair of ligament injuries in the knee. In: Journal of the American Academy of Orthopaedic Surgeons 8, 2000, S. 364–372. PMID 11104400
- ↑ J. Andrish und R. Holmes: Effects of synovial fluid on fibroblasts in tissue culture. In: Clin Orthop Relat Res 138, 1979, S. 279–283. PMID 445911
- ↑ D. Amiel u. a.: Injury of the anterior cruciate ligament: the role of collagenase in ligament degeneration. In: J Orthop Res 7, 1989, S. 486–493. PMID 2544709
- ↑ D. B. Saris u. a.: Joint homeostasis. The discrepancy between old and fresh defects in cartilage repair. In: J Bone Joint Surg Br 85, 2003, S. 1067–1076. PMID 14516049
- ↑ M. Wiig u. a.: Type I procollagen gene expression in normal and early healing of the medial collateral and anterior cruciate ligaments in rabbits: an in situ hybridization study. In: J Orthop Res 9, 1991, S. 374–382. PMID 2010841
- ↑ R. M. Lyon u. a.: Ultrastructural differences between the cells of the medical collateral and the anterior cruciate ligaments. In: Clin Orthop 272, 1991, S. 279–286. PMID 1934745
- ↑ C. N. Nagineni Characterization of the intrinsic properties of the anterior cruciate and medial collateral ligament cells: an in vitro cell culture study. In: J Orthop Res 10, 1992, S. 465–475. PMID 1613622
- ↑ D. S. Gesink u. a.: Immunohistochemical localization of beta 1-integrins in anterior cruciate and medial collateral ligaments of human and rabbit. In: J Orthop Res 10, 1992, S. 596–599. PMID 1377240
- ↑ P. J. Schreck u. a.: Integrin display increases in the wounded rabbit medial collateral ligament but not the wounded anterior cruciate ligament. In: J Orthop Res 13, 1995, S. 174–183. PMID 7722754
- ↑ J. Lee u. a.: Growth factor expression in healing rabbit medial collateral and anterior cruciate ligaments. In: Iowa Orthop J 18, 1998, S. 19–25. PMID 9807704
- ↑ K. Kobayashi u. a.: Novel method for the quantitative assessment of cell migration: a study on the motility of rabbit anterior cruciate (ACL) and medial collateral ligament (MCL) cells. In: Tissue Eng 6, 2000, S. 29–38. PMID 10941198
- ↑ a b M. M. Murray u. a.: Histological changes in the human anterior cruciate ligament after rupture. In: J Bone Joint Surg Am 82, 2000, S. 1387–1397. PMID 11057466
- ↑ C. Frank u. a.: Healing of the medial collateral ligament of the knee. A morphological and biochemical assessment in rabbits. In: Acta Orthop Scand 54, 1983, S. 917–923. PMID 6670520
- ↑ K. P. Spindler u. a.: Expression of collagen and matrix metalloproteinases in ruptured human anterior cruciate ligament: an in situ hybridization study. In: J Orthop Res 14, 1996, S. 857–861. PMID 8982126
- ↑ M. M. Murray u. a.: Migration of cells from human anterior cruciate ligament explants into collagen-glycosaminoglycan scaffolds. In: J Orthop Res 18, 2000, S. 557–564. PMID 11052491
- ↑ M. M. Murray und M. Spector: The migration of cells from the ruptured human anterior cruciate ligament into collagen-glycosaminoglycan regeneration templates in vitro. In: Biomaterials 22, 2001, S. 2393–2402. PMID 11511036
- ↑ M. M. Murray u. a.: Enhanced histologic repair in a central wound in the anterior cruciate ligament with a collagen-platelet-rich plasma scaffold. In: J Orthop Res 25, 2007, S. 1007–1017. PMID 17415785
- ↑ A. J. Harrold: The defect of blood coagulation in joints. In: J Clin Path 14, 1961, S. 305–308. PMID 13711857
- ↑ D. Rosc u. a.: Post-traumatic plasminogenesis in intraarticular exudate in the knee joint. In: Medical Science Monitor 8, 2002, S. CR371–378. PMID 12011780
- ↑ M. E. Wiig u. a.: The early effect of high molecular weight hyaluronan (hyaluronic acid) on anterior cruciate ligament healing: an experimental study in rabbits. In: J Orthop Res 8, 1990, S. 425–434. PMID 2324860
- ↑ M. M. Murray u. a.: Collagen-platelet rich plasma hydrogel enhances primary repair of the porcine anterior cruciate ligament. In: J Orthop Res 25, 2007, S. 81–91. PMID 17031861
- ↑ P. Lobenhoffer u. a.: Rupturen des hinteren Kreuzbandes: heutiger Behandlungsstand. In: Unfallchirurg 99, 1996, S. 382–399. PMID 8767134
- ↑ A. Weiler u. a.: Arthroskopisch assistierte hintere Kreuzbandplastik und posterolaterale Stabilisierung mit Semitendinosus-Gracilissehnen. In: Unfallchirurg 109, 2006, S. 61–71. PMID 16385417
- ↑ F. R. Noyes und S. Barber-Westin: Posterior cruciate ligament replacement with a two-strand quadriceps tendon-patellar bone autograft and a tibial inlay technique. J Bone Joint Surg Am 87, 2005, S. 1241–1252. PMID 15930532
- ↑ J. Kvist: Rehabilitation following anterior cruciate ligament injury: current recommendations for sports participation. In: Sports Med 34, 2004, S. 269–280. PMID 15049718
- ↑ L. S. Lohmander u. a.: High prevalence of knee osteoarthritis, pain, and functional limitations in female soccer players twelve years after anterior cruciate ligament injury. In: Arthritis Rheum 50, 2004, S. 3145–3152. doi:10.1002/art.20589 PMID 15476248
- ↑ H. Seitz u. a.: Meniskusläsionen nach isolierter vorderer Kreuzbandruptur. In: Wien Klin Wochenschr 108, 1996, S. 727–730. PMID 9157718
- ↑ B. E. Øiestad u. a.: Knee osteoarthritis after anterior cruciate ligament injury: a systematic review. In: Am J Sports Med 37, 2009, S. 1434–1443. PMID 19567666 (Review)
- ↑ A. J. Hart u. a.: Assessment of osteoarthritis after reconstruction of the anterior cruciate ligament: a study using single-photon emission computed tomography at ten years. In: J Bone Joint Surg Br 87, 2005, S. 1483–1487. PMID 16260663
- ↑ R. A. Magnussen u. a.: Meniscus status at anterior cruciate ligament reconstruction associated with radiographic signs of osteoarthritis at 5- to 10-year follow-up: a systematic review. In: J Knee Surg 22, 2009, S. 347–357. PMID 19902731 (Review)
- ↑ J. Gillquist und K. Messner: Anterior cruciate ligament reconstruction and the long-term incidence of gonarthrosis. In: Sports Med 27, 1999, S. 143–156. PMID 10222538 (Review)
- ↑ S. M. Joy: Osteoarthritis after anterior cruciate ligament injury: the quadriceps question. In: Exerc Sport Sci Rev 37, 2009, S. 112. PMID 19550201
- ↑ L. S. Lohmander u. a.: The long-term consequence of anterior cruciate ligament and meniscus injuries: osteoarthritis. In: Am J Sports Med 35, 2007, S. 1756–1769. PMID 17761605
- ↑ S. L. Keays u. a.: Factors involved in the development of osteoarthritis after anterior cruciate ligament surgery. In: Am J Sports Med 38, 2010, S. 455–463. PMID 20051501
- ↑ a b H. Louboutin u. a.: Osteoarthritis in patients with anterior cruciate ligament rupture: a review of risk factors. In: Knee 16, 2009, S. 239–244. PMID 19097796 (Review)
- ↑ A. Friedl: Fußballer leben gefährlich. In: Berliner Morgenpost vom 10. Juni 2008
- ↑ B. Engström u. a.: Does a major knee injury definitely sideline an elite soccer player? In: Am J Sports Med 18, 1990, S. 101–105. PMID 2301681
- ↑ R. Bahr und T. Krosshaug: Understanding injury mechanisms: a key component of preventing injuries in sport. In: Br J Sports Med 39, 2005, S. 324–329. PMID 15911600 (Review)
- ↑ a b E. Alentorn-Geli u. a.: Prevention of non-contact anterior cruciate ligament injuries in soccer players. Part 2: a review of prevention programs aimed to modify risk factors and to reduce injury rates. In: Knee Surg Sports Traumatol Arthrosc 17, 2009, S. 859–879. PMID 19506834 (Review)
- ↑ J. Gilchrist u. a.: A randomized controlled trial to prevent noncontact anterior cruciate ligament injury in female collegiate soccer players. In: Am J Sports Med 36, 2008, S. 1476–1483. PMID 18658019
- ↑ aclprevent.com: PEP Program. Prevent injury, Enhance Performance = PEP, Beschreibung der Aufwärmübungen (englisch)
- ↑ M. K. Zebis u. a.: The effects of neuromuscular training on knee joint motor control during sidecutting in female elite soccer and handball players. In: Clinical Journal of Sports Medicine 18, 2008, S. 329–337. PMID 18614884
- ↑ Science of Soccer Online: Cutting-Edge Research: ACL Injury Prevention - Neuromuscular Training. Vom 29. Juli 2008, abgerufen am 6. März 2010
- ↑ T. E. Hewett u. a.: Prevention of anterior cruciate ligament injuries. In: Curr Womens Health Rep 1, 2001, S. 218–224. PMID 12112973
- ↑ G. Cerulli u. a.: Proprioceptive training and prevention of anterior cruciate ligament injuries in soccer. In: J Orthop Sports Phys Ther 31, 2001, S. 655–660. PMID 11720298
- ↑ A. Caraffa u. a.: Prevention of anterior cruciate ligament injuries in soccer. A prospective controlled study of proprioceptive training. In: Knee Surg Sports Traumatol Arthrosc 4, 1996, S. 19–21. PMID 8963746
- ↑ a b M. Gruber: Die neuromuskuläre Kontrolle des Kniegelenks vor und nach einem spezifischen sensomotorischen Training beim unverletzten Sportler. Dissertation, Universität Stuttgart, 2001, S. 53.
- ↑ R. M. Biedert u. a.: Sensomotorische Funktion des Kniegelenkes. In: Sportorthopädie – Sporttraumatologie 14, 1998, S. 186–194.
- ↑ a b O. E. Olsen u. a.: Exercises to prevent lower limb injuries in youth sports: cluster randomised controlled trial. In: BMJ 330, 2005, S. 449. PMID 15699058
- ↑ W. Petersen u. a.: A controlled prospective case control study of a prevention training program in female team handball players: the German experience. In: Arch Orthop Trauma Surg 125, 2005, S. 614–621. PMID 15703919
- ↑ H. J. Silvers u. a.: Anterior cruciate ligament tear prevention in the female athlete. In: Curr Sports Med Rep 4, 2005, S. 341–343. PMID 16282037
- ↑ H. Himmelreich u. a.: Prävention von Sportverletzungen und Sportschäden. In: Weißbuch Prävention – Beweglich? Verlag Springer, 2008, doi:10.1007/978-3-540-77274-3_7 ISBN 3-540-77273-1 S. 143–151. Eingeschränkte Vorschau in der Google Buchsuche
- ↑ J. W. Orchard und H. Seward: Decreased incidence of knee posterior cruciate ligament injury in Australian Football League after ruck rule change. In: Br J Sports Med 43, 2009, S. 1026–1030. PMID 19850572
- ↑ F. Povacz: Geschichte der Unfallchirurgie. Verlag Springer, 2007, S. 244, doi:10.1007/978-3-540-74845-8 (Eingeschränkte Vorschau in der Google Buchsuche).
- ↑ W. Weber und E. Weber: Mechanik der menschlichen Gehwerkzeuge: eine anatomisch-physiologische Untersuchungen. Dieterichsche Buchhandlung, Göttingen, 1835 (Volltext in der Google Buchsuche).
- ↑ a b J. Karlsson: History of Cruciate Ligament Repair. In: Repair and Regeneration of Ligaments, Tendons, and Joint Capsule W. R. Walsh (Editor), Humana Press, 2006, S. 135–142. ISBN 978-1-58829-174-5 doi:10.1385/1-59259-942-7:135 (Eingeschränkte Vorschau in der Google Buchsuche)
- ↑ A. Bonnet: Traité des maladies des articulations. Band 2, Verlag J. B. Baillière, 1945 (Volltext in der Google Buchsuche)
- ↑ R. D. Galway u. a.: Privot shift: A clinical sign of symptomatic anterior cruciate insufficiency. In: J Bone Jt Surg 54B, 1972, S. 763
- ↑ R. Galway: Lateral pivot shift injury of the knee. In: J Bone Jt Surg 53-B, 1971, S. 772–773.
- ↑ H. R. Galway und D. L. MacIntosh: The lateral pivot shift: a symptom and sign of anterior cruciate ligament insufficiency. In: Clin Orthop Relat Res 147, 1980, S. 45–50. PMID 7371314
- ↑ A. Bonnet: Traité de thérapeutique des maladies articulaires. Verlag J. B. Baillière, 1853 (Volltext in der Google Buchsuche).
- ↑ A. Bonnet: Traité de thérapeutique des maladies articulaires. Verlag J. B. Baillière, 1853. S. 345 (Volltext in der Google Buchsuche)
- ↑ F. H. Fu: Current Concepts in ACL Reconstruction. SLACK Incorporated, 2008, ISBN 1-55642-813-8 Eingeschränkte Vorschau in der Google Buchsuche
- ↑ J. Stark: Two cases of ruptured cucial ligaments of the knee joint. In: Edinburgh Med Surg 74, 1850, S. 267–269.
- ↑ E. Luciani: Eine in-vitro-Studie über die Zugkräfte im vorderen Kreuzband und vorderen Kreuzband-Ersatz (Ligamentum patellae- und Semitendinosus-Plastik). Dissertation. LMU München, 2003
- ↑ A. Poncet: Arrachement de l’epine du tibia a l’insertion du ligament croise anterieur. In: Bull et mem Soc de chir de Paris 1, 1875, S. 883–884.
- ↑ Sir Arthur Mayo-Robson, K.B.E., C.B.. In: Br Med J 3798, 1933, S. 761–762, PMID 12986638.
- ↑ A. W. Mayo Robson: Ruptured crucial ligaments and their repair by operation. In: Ann Surg 37, 1903, S. 716–718, PMID 17861289.
- ↑ W. Battle: A case after open section of knee joint for irreducible traumatic dislocation. In: Clin Soc London Trans 33, 1900, S. 232.
- ↑ H. Goetjes: Über Verletzungen der Ligamenta cruciata des Kniegelenkes. In: Dtsch Z Chir 123, 1913, S. 221–289.
- ↑ R. Jones: Disabilities of the knee joint. In: BMJ 2, 1916, S. 925–932.
- ↑ F. Baumgartl: Verletzungen der Kreuzbänder. In: Das Kniegelenk F. Baumgartl F (Hrsg.), Verlag Springer, 1964, S. 149.
- ↑ M. Lange: Behandlung von Gelenkschäden. In: Unfallorthopädie M. Lange (Hrsg.) Verlag Enke, S. 263.
- ↑ a b K. Lindemann: Über den plastischen Ersatz der Kreuzbänder durch gestielte Sehnenverpflanzung. In: Z Orthop 79, 1950, S. 316–334.
- ↑ F. Lutz: Erfahrungen und Ergebnisse beim plastischen Ersatz der Kreuzbänder am Kniegelenk nach Niederecker. In: Arch Orthop Unfallchir 46, 1954, S. 439–444.
- ↑ D. O'Donoghue: Surgical treatment of fresh injuries to the major ligaments of the knee. In: J Bone Joint Surg Am 32, 1950, S. 721–738, PMID 14784482.
- ↑ P. B. Roth: Fracture of the spine of the tibia. In: J Bone Joint Surg 10, 1928, S. 509–518.
- ↑ W. Müller: Die Entwicklung der operativen Behandlung der "Knie-Binnenläsionen". Abgerufen am 7. Februar 2010.
- ↑ E. Hesse: Über den Ersatz der Kreuzbänder des Kniegelenks durch freie Fascientransplantation. In: Verh Dtsch Ges Chir 43, 1914, S. 188–189.
- ↑ E. W. Hey-Groves: Operation for repair of the crucial ligament. In: Lancet 2, 1917, S. 674.
- ↑ E. W. Hey Groves: The crucial ligaments of the knee joint; their function, rupture and the operative treatment of the same. In: Br J Surg 7, 1920, S. 505–515.
- ↑ A. Heverhagen: Langzeitergebnisse nach vorderer Kreuzbandplastik mit Patellarsehnentransplantat. Dissertation, Philipps-Universität Marburg, 2009
- ↑ G. A. Snook: A short history of the anterior cruciate ligament and the treatment of tears. In: Clinical Orthopaedics 172, 1983, S. 11–13, PMID 6336998.
- ↑ A. Wittek: Kreuzbandersatz aus dem Lig. Patellae (nach zur Verth). In: Schweiz Med Wochenschr 65, 1935, S. 103–104.
- ↑ Zur Verth: Aussprache 27. Kongress, 5.-7. Sept. 1932, Mannheim. In: Verh Dtsch Orthop Ges 1933, S. 268–270.
- ↑ A. H. Edwards: Rupture and repair of the anterior cruciate ligament. In: Br J Surg 13, 1926, S. 432–438.
- ↑ S. Rupp u. a.: Ersatz des vorderen Kreuzbandes mit dem Patellarsehnentransplantat. In: Orthopäde 31, 2002, S. 751–757, PMID 12426753 (Review).
- ↑ H. Brückner: Eine neue Methode der Kreuzbandplastik. In: Chirurg 37, 1966, S. 413–414.

Bitte den Hinweis zu Gesundheitsthemen beachten! 
Dieser Artikel wurde am 9. Juni 2010 in dieser Version in die Liste der exzellenten Artikel aufgenommen. Kategorien:- Wikipedia:Exzellent
- Krankheitsbild in Orthopädie und Unfallchirurgie
- Therapeutisches Verfahren in Orthopädie und Unfallchirurgie
Wikimedia Foundation.