- Grüne Gentechnik
-
Die Grüne Gentechnik oder Agrogentechnik ist die Anwendung gentechnischer Verfahren im Bereich der Pflanzenzüchtung, deren Ergebnisse transgene Pflanzen oder gentechnisch veränderte Pflanzen genannt werden. Insbesondere bezeichnet der Begriff Verfahren zur Herstellung von pflanzlichen gentechnisch veränderten Organismen (GVO), in deren Erbgut gezielt einzelne Gene eingeschleust werden. Die Grüne Gentechnik ist somit Bestandteil der Grünen Biotechnologie, wobei sich die Bezeichnung „grün“ in Abgrenzung zur „roten“ Biotechnologie und „weißen“ Biotechnologie auf die Anwendung an Pflanzen bezieht.
Die Grüne Gentechnik unterscheidet sich von der herkömmlichen Züchtung, indem sie einzelne Gene gezielt transferieren und dabei Artgrenzen sowie andere Kreuzungshindernisse (wie etwa Unfruchtbarkeit) leichter überschreiten kann und aufgrund der speziellen mikrobiologischen Technik nur in speziell ausgerüsteten Laboratorien möglich ist. Die herkömmliche Pflanzenzüchtung hingegen nutzt meist spontane oder induzierte Mutationen, deren Ausprägung weniger gezielt in der Zelle, sondern durch äußere Einflüsse (z.B. Kälteschocks) hervorgerufen werden. In beiden Fällen ist vor weiterer Züchtung eine selektive Sichtung der Mutationen erforderlich.
Derzeit werden als gentechnisch veränderte Pflanzen insbesondere herbizid- und insektenresistente Pflanzensorten vermarktet.
Forschung und Techniken
Moderne Pflanzenphysiologie beschäftigt sich auch mit den molekularen Vorgängen innerhalb der Pflanzen. War es vor 100 Jahren gerade möglich, die Sauerstoffproduktion von Pflanzen und einige andere globale Parameter zu untersuchen, so kann man heute mit verschiedenen Techniken in das molekulare Geschehen einzelner Zellen hineinsehen. Eine sehr wichtige Rolle wird dabei der Gentechnik beigemessen, da sie es ermöglicht, das Verhalten von Genen in der Pflanze zu beeinflussen. Jede Pflanzenzelle enthält zwischen 20.000 und 60.000 Gene, von denen erst bei einem Bruchteil die Funktion bekannt ist. Selbst bei der bestuntersuchten Pflanze (Arabidopsis thaliana) ist noch mehr als die Hälfte der Gene ohne bekannte Funktion. Um die Funktion zu erkennen, ist es nötig, die Steuerung des Gens zu modifizieren.
So werden Effekte von Genen normalerweise durch einen Vergleich dreier Pflanzenpopulationen aufzuklären versucht. Die erste, unveränderte, Population wird als Wildtyp bezeichnet. Eine Population, die als Überexpressoren bezeichnet werden, produziert vermehrt das Genprodukt (meist ein Protein). Dies geschieht meist, indem das Gen hinter einen viralen Promotor kloniert und in die Pflanze übertragen wird. Virale Promotoren sind auf maximale Effizienz optimiert und werden deshalb für besonders geeignet gehalten, große Mengen Ribonukleinsäure (RNA) zu produzieren. Eine dritte, die so genannte „Knock out”-Population, produziert das Genprodukt in geringerem Maße oder gar nicht mehr. Hierfür gibt es verschiedene Techniken, wie etwa RNA-Interferenz (RNAi). Klassische „Knock out”-Pflanzen sind T-DNA-Insertionslinien, so dass entweder ein trunkiertes Protein entsteht, welches keine Funktion hat, oder der Promoter des Wildtyp-Gens ist durch die T-DNA-Insertion betroffen. Mit Hilfe der RNAi können „Knock down”-Pflanzen erzeugt werden, wenn zum Beispiel ein „Knock out” im homozygoten Zustand lethal ist. Ein „Knock down” durch RNAi bietet die Möglichkeit, verschiedene Expressionslevel des Wildtyp-Gens auf Grund der unterschiedlichen Effizienz verschiedener RNAi-Konstrukte zu untersuchen.
Auch komplizierte Regulationsmechanismen sollen aufgeklärt werden, indem nicht nur das Genprodukt, sondern auch die gesamten Änderungen innerhalb der Zelle bzw. Pflanze betrachtet werden. Diese Methoden sollen das klassische Durchmustern von Mutanten um eine viel gezieltere Technik erweitern, mit der es möglich ist, den Effekt von gefundenen „Kandidatengenen” direkt zu untersuchen.
Zusätzlich zu den oben genannten Techniken gehören auch deskriptive Techniken zur gentechnischen Pflanzenforschung. So werden über Polymerase-Kettenreaktionen (PCR) Gene kloniert, es werden Häufigkeiten von Transkripten (Bauanleitungen für Proteine) mittels quantitativer PCR bestimmt oder mittels so genannter DNA-Chips gleich die meisten Gene einer Pflanze in ihrer Ablesehäufigkeit bestimmt.
In der modernen Grünen Gentechnik ist der Agrobacterium-vermittelte Gentransfer eine wichtige Technik. Bei dieser gentechnischen Methode werden einzelne Erbfaktoren von Zellen eines Organismus in Zellen eines anderen Lebewesens übertragen. Sie wurde in den 1980er Jahren von Jozef Schell und Marc van Montagu entwickelt.
Die somatische Hybridisierung, eine weitere wichtige Methode, erlaubt es, gewünschte Merkmale verschiedener Elternpflanzen zu kombinieren. Im Vergleich zum Agrobacterium-vermittelten Gentransfer müssen hierbei keine spezifischen Gene identifiziert und isoliert werden. Außerdem wird damit die Einschränkung der Transformation überwunden, nur wenige Gene in ein vorgegebenes Erbgut einführen zu können. Auch kann bei der Zellfusion die Chromosomenzahl der Zellen multipliziert werden, also die Anzahl der Chromosomensätze (Ploidiegrad) erhöht werden. Dies kann die Ertragsfähigkeit von Pflanzen steigern (Heterosiseffekt). Molekulare Marker oder biochemische Analysen werden genutzt, um aus der somatischen Hybridisierung hervorgegangene Pflanzen zu charakterisieren und zu selektieren.
Methoden der Gentransformation
Es existieren eine Reihe von Methoden zur Herstellung transgener Pflanzen. Zur Anwendung kommen neuere Methoden des Gentransfers und der klassischen induzierten Genmutation (Mutation, Deletion, Insertion und Chromosomenaberration beispielsweise mit Einsatz von Colchizin).
Breite Anwendung haben drei Transfermethoden gefunden, bei denen unterschiedliche Vektoren zum Einsatz kommen.[1]
Transfer durch Agrobacterium tumefaciens
Agrobacterium tumefaciens ist ein Bodenbakterium, das ein spezielles Plasmid in das pflanzliche Genom integriert. Auf diesem Weg werden bei Pflanzen Gallen am Wurzelhals als Lebensraum und zugleich die Produktion bestimmter Nährstoffe, so genannter Opine, ausgelöst. Dies macht man sich in der Gentechnik zunutze, indem man das Plasmid, das Tumorbildung und Opinproduktion auslöst, stilllegt und um ein kleineres Plasmid mit Fremdgenen ergänzt, das zuvor in Escherichia coli zusammengesetzt wurde (binäres Vektorsystem).[2] Anschließend werden Pflanzenstücke mit diesen Bakterienstämmen infiziert, transgene Gewebe selektiert und mittels In-vitro-Kultur wieder zu vollständigen Pflanzen herangezogen.[3][4][5]
Damit Agrobacterium tumefaciens Pflanzenzellen transformieren kann, müssen diese als Folge einer Verletzung phenolische Substanzen ausschütten, die als „Lockstoff“ für das Bakterium dienen. Da nur sehr wenige einkeimblättrige Pflanzen dies tun, ist der Einsatz weitgehend auf zweikeimblättrige Pflanzen begrenzt, allerdings konnte durch Zugaben entsprechender Stoffe (z.B. Acetosyringon)[6] das Anwendungsgebiet auf einige Einkeimblättrige und sogar Pilze vergrößert werden. Eine weitere Einschränkung ist, dass Agrobacterium tumefaciens sich ausschließlich zur Transformation der Chromosomen des Zellkerns eignet.[3]
Biolistische Transfers
Ein biolistischer Transfer ist im Gegensatz dazu eine rein mechanische Methode des Gentransfers. Hier wird DNA auf Gold- oder Wolframpartikel aufgebracht, die anschließend mit Geschwindigkeiten von mehr als 1.300 m/s in die Zellen geschossen werden.[3] Dies wird mit Hilfe einer Genkanone durchgeführt.
Da die Partikel sehr klein sind, bleiben Zelle und Zellwand dabei weitgehend unbeschädigt. Weitere Vorteile sind, dass das Verfahren für Zellen jedweder Lebewesen geeignet ist, auch auf die DNA von Mitochondrien und Plastiden angewandt werden kann und dass die mögliche Anzahl der transferierten Gene relativ hoch ist. Problematisch ist allerdings, dass der Gentransfer relativ instabil ist, häufig kommt es nur zu einer sogenannten „transienten Expression“, die eingefügte DNA ist also nur vorübergehend aktiv und verliert sich später wieder, auch kommt es manchmal dazu, dass nur Teile des erzielten Gewebes aus transformierten Zellen bestehen.[3] [7][8]
Protoplastentransformation
Ein dritter möglicher Weg ist die Protoplastentransformation. Hierbei werden die Zellen des zu transformierenden Gewebes zuerst durch Pektinasen vereinzelt (siehe Protoplastenkultur) und anschließend durch Zellulasen die Zellwände aufgelöst (Protoplastenisolation). So erhält man nur noch durch die Zellmembran zusammengehaltene Protoplasten.[3]
Für den eigentlichen Gentransfer wird diesen Protoplasten entweder Polyethylenglykol hinzugefügt oder es erfolgt ein Transfer nach einem kurzen Stromstoß (Elektroporation), wodurch die Membran durchlässig für die DNA wird. Die Methode ist zwar bei allen Pflanzen anwendbar, allerdings ist es äußerst schwierig, anschließend aus den Protoplasten wieder Pflanzen zu regenerieren.[3]
Merkmale, Anwendungen
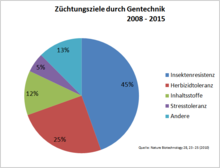
Züchtungsziele durch Gentechnik (Stand: 2010)[9] Gv-Sorten nach Pflanzenart (Stand: 2010)[9]
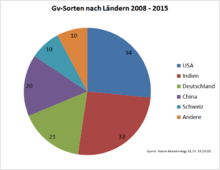
Gv-Sorten nach Pflanzenart (Stand: 2010)[9] Gv-Sorten nach Ländern (Stand: 2010)[9]
Gv-Sorten nach Ländern (Stand: 2010)[9]
Die Ziele der Grünen Gentechnik unterscheiden sich prinzipiell nicht von denjenigen jahrtausendealter traditioneller Pflanzenzucht. Es geht um eine Verbesserung der Eigenschaften von Pflanzen, die anhand folgender Einteilung unterschieden werden können[10]:
- Gv-Pflanzen der ersten Generation, bei denen die Schädlingskontrolle und die Fitness der Pflanze in widrigen Bedingungen erhöht werden soll, z.B. Trocken-, Säure- und Salztoleranz sowie Widerstandsfähigkeit gegen extreme Temperaturen. Dadurch sollen Kosten gesenkt und/oder Erträge gesteigert und damit Deckungsbeiträge erhöht werden.
- Gv-Pflanzen der zweiten Generation, die auf die Verbesserung des Nährstoffgehalts und eine höhere Verarbeitungsqualität abzielen, z.B. Erhöhung des Gehalts von Omega-3-Fettsäuren, Erhöhung und Veränderung des Zuckergehalts, bessere Farbeigenschaften. Hierzu zählt der goldene Reis.
- Gv-Pflanzen der dritten Generation, bei der die Pflanze Industrierohstoffe (Biokraftstoffe, biologisch abbaubares Plastik, Enzyme oder Schmieröle) oder pharmazeutische Produkte wie Hormone, Impfstoffe oder Antikörper herstellen soll.
Die konventionelle Züchtung beruht dabei auf dem Prinzip von Kreuzung und anschließender Selektion. Bei Kreuzungen wird jeweils das gesamte Erbgut der Elternorganismen gemischt. Das Erbgut in den Tochterorganismen lässt sich dabei nicht exakt vorhersagen. Deshalb müssen in den weiteren Generationen die Organismen mit den gewünschten Eigenschaften selektiert werden. Im Gegensatz dazu werden mit der Grünen Gentechnik gezielt aus anderen Arten oder Organismen Gene hinzugefügt, die für eine bestimmte Eigenschaft verantwortlich sind. Es wird darauf hingewiesen,[11] dass
- diese Methode gezielter sei und
- sich Eigenschaften züchten lassen, die sich auf konventionellem Weg nicht erreichen lassen (s. Präzisionszucht)
Im Mittelpunkt der bisherigen Anwendung der Grünen Gentechnik stehen weltweit vier Agrarpflanzen (Anteil GVO 2009 in %): Soja (77 %), Baumwolle (49 %), Mais (26 %) und Raps (21 %). In Nordamerika kommen noch Zuckerrüben hinzu (dort 95 %).[12] Jeder Gentransfer wird mit dem Ziel ausgeführt, den Pflanzen ein gewünschtes Merkmal (engl. trait) zu übertragen. Man unterscheidet Input Traits, das sind Eigenschaften, die für den Anbau interessant sind, und Output Traits, welche den Konsumenten als Zielgruppe haben. Gelingt eine Transformation, so spricht man von einem Event (engl. für Ereignis). Verschiedene Events können zu demselben Merkmal führen.
Input Traits
Herbizidresistenz
Die meisten Herbizide wirken selektiv gegen einzelne unerwünschte Pflanzenarten. Daneben gibt es Breitbandherbizide, welche den Stoffwechsel fast aller Pflanzen hemmen. Durch Übertragung von Genen des Bodenbakteriums Agrobacterium tumefaciens werden Nutzpflanzen erzeugt, die gegen Glyphosat (Markenname Roundup von Monsanto) resistent sind. Das PAT-Gen (Phosphinothricin Acetyl-Transferase) aus Streptomyces viridochromogenes erzeugt ein Protein, das eine Resistenz von Glufosinat-Ammonium (Markenname Liberty von Bayer) bewirkt. Seit 1999 gibt es Pflanzen (z.B. Markenname Clearfield von BASF) mit Resistenz gegen Imidazolinon (aus der Gruppe der ALS-Hemmer), die durch konventionelle Züchtung (Mutagenese) entstanden sind. Transgene Soja mit dieser Eigenschaft wird für 2011 erwartet.[13][14] Herbizidresistenz ist 2009 die zweithäufigste Anwendung mit etwa 15 Events.[15]
Insektenbekämpfung
Von dem Bakterium Bacillus thuringiensis übertragene Gene bewirken, dass die Pflanzen eigenständig Gifte gegen bestimmte Schädlinge erzeugen. Dieses sogenannte Bt-Konzept wird bislang vor allem bei Mais und Baumwolle eingesetzt. Bt-Toxine werden als Präparate seit Jahrzehnten im biologischen Pflanzenschutz oder der Bekämpfung von Stechmücken eingesetzt. Mit über 30 Events ist dieses Merkmal 2009 das häufigste.[15]
Rothamsted Research entwickelte einen transgenen Weizen, der ein Gen aus der Pfefferminze enthält, welches ein Alarmpheromon synthetisiert, das Blattläuse vertreibt. Die ersten Feldversuche sind für 2012 geplant.[16]
Virusresistenz
Als erste Anwendung wurde in den 1990er Jahren an Universitäten in den USA virusresistente Papaya erzeugt.
An der Wiener Universität für Bodenkultur wird Virusresistenz gegen Scharka an der Aprikose durch Einbringung des Gens für die Virushülle des Plum Pox-Virus untersucht.[17]
An der Universität Kapstadt wurde in Zusammenarbeit mit Pannar Seed eine Resistenz gegen den Maize Streak Virus beim Mais entwickelt; sie befindet sich noch in der Testphase.[18]
Das brasilianische EMBRAPA entwickelte eine transgene Gartenbohne, die gegen das Golden Mosaic Virus resistent ist. Sie wurde im September 2011 zugelassen und könnte 2014 erstmals angebaut werden.[19]
Pilzresistenz
Algenähnliche Pilze wie die Gattung Phytophthora infestans gehören zu den Pflanzenschädlingen, die die höchsten Ernteschäden verursachen, etwa bei Tomaten und Kartoffeln. Mit konventionellen Züchtungsmethoden erreicht man zwar hier durch Einkreuzung mexikanischer Wildrassen eine gewisse Resistenz, jedoch werden auch unerwünschte Eigenschaften übertragen, die dann in langwierigen Verfahren wieder herausgezüchtet werden müssen. Alternativ werden chemische Fungizide ausgebracht – pro Anbausaison bis zu sechzehn mal – oder etwa im Biolandbau Kupfersulfate, die aber zu einer starken Bodenbelastung führen.
Von BASF wurde mit gentechnischen Methoden einer Kartoffelsorte („Fortuna“) zwei Resistenzgene aus einer südamerikanischen Wildkartoffelsorte übertragen. Fortuna wurde in Gewächshausversuchen bereits erfolgreich getestet und wird seit 2006 in Schweden, den Niederlanden, Großbritannien, Deutschland und Irland im Freiland getestet. BASF schätzt, dass die Sorte 2014/15 auf den Markt kommen könnte.[20]
Trockentoleranz
Unzureichende Wasserversorgung durch klimatische Veränderungen oder singulär auftretende Trockenperioden führen zu erheblichen Ernteausfällen. Neben der Vermeidung dieser Ausfälle sind weitere Ziele die Ausweitung der Anbauflächen auf klimatisch ungünstige Regionen sowie allgemein eine Verringerung des Wasserverbrauchs in der Landwirtschaft. Als erstes Produkt wird 2012 Trockentoleranter Mais erwartet. Auch bei Baumwolle kennt man Biotechvarietäten mit verbesserter Trockentoleranz. Sie bilden eine Pyrophosphatase, welche aus der mit der Ackerschmalwand (Arabidopsis thaliana) verwandten Salzkresse (Thellungiella halophila) stammt und bei der Aufrechterhaltung des Ionengleichgewichts im Zellplasma eine Rolle spielt.[21]
Die bisherigen Feldversuche zur Trockenresistenz lieferten bei der Firma Monsanto für Mais eine Mehrproduktion von 6,7 % bis 13,4 % gegenüber herkömmlichen Maissorten.[22]
Salz- und Aluminiumtoleranz
Die landwirtschaftliche Produktivität ist auf versalzten Böden stark beeinträchtigt. Weltweit sind mehr als 60 Millionen ha Ackerland von der Bodenversalzung betroffen. Beim Raps konnte man zeigen, dass Individuen, welche ein aus der Ackerschmalwand stammendes Ionentransportprotein (AtNHX1) exprimieren, noch bei einer Natriumchloridkonzentration von 200 Millimol/l wachsen können. Das Wachstum von gewöhnlichem Raps ist bei dieser Konzentration schwer beeinträchtigt, und dies gilt auch für die meisten anderen Ackerpflanzen. Je stärker der Transporter in den Rapspflanzen exprimiert wird, desto höher ist ihre Salztoleranz. Phänotypisch unterscheiden sich bei hoher Salzkonzentration wachsende transgene Rapspflanzen vom Wildtyp kaum.[23] Diese salztoleranten transgenen Rapspflanzen sind insofern interessant, als sie zeigen, dass die gezielte Übertragung eines einzigen neuen Merkmals die Salztoleranz einer Kulturpflanze ohne erkennbare Beeinträchtigung anderer Eigenschaften signifikant verbessern kann. Da dies nur gentechnisch möglich ist, liefern salztolerante transgene Pflanzen auch überzeugende Beispiele für das Entwicklungspotential einer modernen, gentechnische Verfahren einschließenden Pflanzenzüchtung. Unter sauren Bedingungen werden im Boden aus Aluminiumsilikaten dreiwertige Aluminiumionen (Al3+) freigesetzt, die für viele Pflanzen stark toxisch wirken. Da saure Ackerböden 30 bis 40 Prozent der ackerbaulich nutzbaren Landfläche der Erde ausmachen, stellt dies eine schwerwiegende Beeinträchtigung des Anbaus vieler Kulturpflanzen dar. Bei Arabidopsis, Raps und manchen anderen Pflanzen kann die Aluminiumtoleranz durch Überexpression bestimmter Enzyme des Energiestoffwechsels verbessert werden. Allerdings sind diese Entwicklungen von der Anwendungsreife noch weit entfernt.[24]
Das australische Forschungsinstitut ACPFG berichtete im September 2010, dass es gelungen sei, die Salztoleranz von Reis zu erhöhen. Dazu wurde mithilfe der Gentechnik der Salzgehalt in den Wurzeln der Pflanze erhöht.[25]
Output Traits
Eines der ersten Gv-Lebensmittel mit veränderter Produktqualität war in den 1990er Jahren die FlavrSavr-Tomate, bei der ein Gen für die Bildung des Reife-Enzyms Polygalacturonase blockiert war und die Früchte dadurch länger haltbar wurden. Auf Grund unzureichender Qualität im Anbau (geringe Erträge und Widerstandskraft) wurde die Vermarktung nach wenigen Jahren eingestellt.[26]
Ein weiteres Beispiel für veränderte Inhaltsstoffe ist die zur Stärkeproduktion vorgesehene Amflora-Kartoffel.
Die in der grünen Gentechnik am häufigsten verwendete Baumart ist die Pappel. Ziele der Forschung sind ein verminderter Ligningehalt, um in der Papier- und Zellstoffherstellung mit weniger Bleichmitteln auszukommen, schnelleres und stärkeres Wachstum zur Nutzung als Energiepflanzen sowie Aufnahme von Umweltgiften zur biologischen Reinigung belasteter Böden.
Bioverfügbarkeit von Phosphat und Eisen
Der an sich für die menschliche und tierische Ernährung ausreichende Phosphorgehalt von Getreide und Ölsaaten ist größtenteils in Phytinsäure gebunden. Phytinsäure (Inositolhexakisphosphat) ist der Hexaphosphorsäureester des Inositols (Cyclohexanhexols), eines sechswertigen zyklischen Alkohols. Rinder und andere Wiederkäuer können die Phytinsäure nutzen. Nicht wiederkäuende Nutztiere scheiden mit der Nahrung aufgenommene Phytinsäure unverdaut wieder aus. Dies ist der Grund dafür, dass Gülle vom Schwein und anderen Haustieren soviel Phosphat enthält. Die unverdaut ausgeschiedene Phytinsäure wird als Hauptquelle der Phosphatverschmutzung und Eutrophierung der Gewässer durch die Landwirtschaft angesehen.
Um die Nahrungsansprüche von Schweinen und Geflügel zu befriedigen, ergänzt man Tierfutter oft entweder mit Phosphat, das aus Gesteinsmehl stammt oder durch Zugabe von Phytase, eines Phytinsäure zerlegenden Enzyms aus Mikroorganismen. Da die Supplementierung kostspielig ist, wird versucht, das Problem an der Wurzel anzupacken, indem man Pflanzen züchtet, deren Samen einen möglichst niedrigen Phytinsäuregehalt haben. Dabei sind gegenwärtig vor allem zwei Ansätze erkennbar: die Expression rekombinierter Phytasegene in den Keimblättern des Embryos und die Stilllegung von Genen, welche zur Synthese oder Speicherung der Phytinsäure erforderliche Enzyme oder Transportproteine kodieren.
Transgene Sojapflanzen, deren Samen eine bakterielle Phytase exprimieren, können im Samen so viel Phytase bilden, dass die Phytinsäure nahezu vollständig in Phosphat und Inositol umgewandelt wird. Es gibt ferner transgene Maispflanzen, welche die Phytase eines Schimmelpilzes exprimieren, entweder ausschließlich oder in Kombination mit dem Eisen bindenden Protein Ferritin. In aus Körnern dieser Pflanzen hergestelltem Maismehl sind bis zu 95 % der Phytinsäure abgebaut, wodurch der Phosphor bioverfügbar wird. Maispflanzen, welche zusätzlich das Eisen bindende Protein Ferritin im Korn bilden, haben zudem einen wesentlich höheren Eisengehalt. Die Expression rekombinierter Phytase- und Ferritingene in transgenem Mais könnte somit genutzt werden, um Phosphat- und Eisenmangel, wie er bei vegetarischer Ernährung leicht auftreten kann, vorzubeugen.[27]
Proteinqualität und -gehalt
Wie die bereits vermarktete Sorte LY038 zeigt, kann der Lysinmangel des Maiskorns durch Eingriffe in die Regulation der Lysinsynthese verringert werden. Davon abgesehen werden noch weitere Möglichkeiten untersucht. Ein Gen einer in Bolivien beheimateten Wildkartoffel kodiert ein pollenspezifisches Protein mit besonders hohem Lysingehalt. Wird es in den Mais eingeführt, so erhält man ein Korn, in dem der Lysingehalt um 16 bis 55 Prozent erhöht ist. Im Gegensatz zu LY038 wird hier nicht der Gehalt an freiem Lysin erhöht, sondern der des proteingebundenen Lysins bei gleichzeitiger Steigerung des Proteinanteils im Korn.[28]
Im Jahr 2003 gelang es indischen Forschern des Central Potato Research Institute, den Proteingehalt einer Kartoffel durch Transfer eines Amaranthgens um 60 % zu erhöhen. Die Eigenschaft wurde bereits in sieben Kartoffelsorten übertragen, welche dann über mehrere Jahre hinweg getestet wurden. Manche Sorten steigerten durch die genetische Modifikation ihren Proteingehalt auf das doppelte und den Gehalt mehrere essentieller Aminosäuren; der Ertrag lag zudem um 15 bis 25 % höher als bei den unveränderten Sorten.[29]
Entfernung von Allergenen bei Soja und Futtergräsern
Ein signifikanter Teil der Bevölkerung reagiert allergisch auf bestimmte Lebensmittel. Die Allergene der Sojabohne sind insofern besonders problematisch, als die Verwendung von Sojaprodukten wegen des hohen Ernährungswerts der Sojaproteine in der Lebensmittelproduktion zunehmende Verbreitung gefunden hat. Dies führt dazu, dass es für Sojaallergiker immer schwieriger wird, sojafreie Lebensmittelprodukte zu bekommen. Auch bei Schweinen und Kälbern findet man Sojaallergien. Lebensmittelallergene sind fast immer natürlich vorkommende Proteine. Eines der allergenen Samenproteine der Sojabohne trägt die Bezeichnung Gly-m-Bd-30-K. Es macht etwa ein Prozent des Gesamtproteins des Samens aus. Auf dieses Protein reagieren mehr als 65 Prozent der Sojaallergiker. Es ist möglich, das Gen dieses Proteins stillzulegen und Sojalinien zu entwickeln, die dieses Allergen nicht mehr enthalten.[30] Die Eliminierung von Allergenen ist auch bei anderen Pflanzen möglich. Die Expression des wichtigsten Proteinallergens des Weidelgrases (Lolium spec.), eines der verbreitetsten Weidegräser mit stark allergenem Pollen, kann unterdrückt werden, ohne Vitalität oder Nutzwert der Pflanze zu beeinträchtigen.[31] Andererseits ist kein Fall bekannt geworden, wo eine Biotechpflanze ein in ihrem konventionellen Vorläufer nicht vorhandenes Allergen gebildet hätte.
Qualitätsverbesserung von Ölen
Vitamin E (Tocopherol) ist ein Sammelbegriff für eine Gruppe von acht fettlöslichen Substanzen, von denen α-Tocopherol die höchste biologische Aktivität besitzt. Wichtige Vitamin-E-Lieferanten für den Menschen sind Keimöle und kaltgepresste Speiseöle, ferner Milch, Eier, aber auch einige Gemüsesorten. Viele medizinische Studien weisen darauf hin, dass α-Tocopherol Herz-Kreislauferkrankungen, Entzündungsreaktionen und Krebs vorbeugen oder den Verlauf dieser Krankheiten günstig beeinflussen kann. Allerdings ist die tägliche Aufnahme therapeutisch wirksamer Vitamin-E-Mengen ohne den Verbrauch großer Mengen mit dem Vitamin angereicherter Lebensmittel schwierig. Seit einigen Jahren versucht man deshalb, die pflanzliche Tocopherolsynthese zu optimieren und Pflanzen mit hohem α-Tocopherolgehalt zu züchten. Vor allem Ölpflanzen wie Raps und Soja kommen dafür in Betracht, da diese die bedeutendsten Vitamin-E-Lieferanten sind.
Den Syntheseweg der Tocopherole kennt man seit über 30 Jahren. Da α-Tocopherol das Endprodukt der Tocopherolsynthese bildet und die übrigen Tocopherole Zwischenprodukte der α-Tocopherolsynthese sind, könnte die Überexpression von Enzymen, die Zwischenschritte der Tocopherolsynthese katalysieren, geeignet sein, die biologisch weniger wirksamen β-, γ- und δ-Tocopherole in α-Tocopherol umzuwandeln. Bisherige Versuche, die α-Tocopherolsynthese zu optimieren, beruhen auf diesem Prinzip.[32] Die Überexpression des γ-Tocopherol-Methyltransferase-Gens von Perilla frutescens, einer in Ostasien heimischen Ölpflanze, im Sojasamen liefert Pflanzen, deren Samen gegenüber dem Wildtyp den zehnfachen Gehalt an α-Tocopherol und den 15-fachen an β-Tocopherol haben, was einer ca. fünffachen Steigerung der Vitamin-E-Aktivität entspricht.[33]
Mehrere Firmen haben transgene Ölpflanzen entwickelt, deren Fetteigenschaften gesundheitliche Vorteile bringen sollen. So hat eine von Pioneer Hi-Bred entwickelte und bereits vom USDA zum Anbau zugelassene transgene Sojabohne eine längere Haltbarkeit und erhöhte Hitzebeständigkeit, was den Anteil von trans-Fettsäuren beim Braten oder Frittieren reduziert.[34]
Essentielle Fettsäuren wie Arachidonsäure, Eicosapentaensäure, Docosapentaensäure und Docosahexaensäure können vom menschlichen Körper nicht synthetisiert und müssen deshalb mit der Nahrung aufgenommen werden. Die ausreichende Versorgung mit essentiellen Fettsäuren ist eine wichtige Voraussetzung zur Verhinderung permanenter prä- und neonataler Entwicklungsstörungen, da sich nur so die an molekularen Membranen reichen Gewebe des Gehirns, Nerven- und Gefäßsystems normal entwickeln können. Mehrfach ungesättigte Fettsäuren mit mehr als 19 Kohlenstoff-Atomen findet man vor allem in tierischen Fetten. Die Produktion essentieller Fettsäuren in Pflanzen würde der Lebensmittelindustrie eine neue und kostengünstige Quelle dieser ernährungsphysiologisch wichtigen Nahrungsbestandteile erschließen.
Arachidonsäure (AA), Eicosapentaensäure (EPA) und Docosahexaensäure (DHA) kommen im Rapsöl nicht vor. Die Samen des Braunen Senfs (Brassica juncea), einer mit dem Raps eng verwandten asiatischen Ölpflanze, enthalten aber Linolsäure und Linolensäure, welche in drei konsekutiven Schritten in AA und EPA umgewandelt werden können. Man kennt beim Braunen Senf transgene Linien, deren Samenöl im Mittel 4 % AA, 8 % EPA und 0,2 % DHA enthält. Diese Pflanzen tragen drei bis neun an der Biosynthese langkettiger Fettsäuren beteiligte Enzymgene, die aus verschiedenen Organismen stammen. Sie sind blockweise in einem einzigen Transformationsschritt übertragen worden. Dies bedeutet eine wesentliche Verringerung des Transformationsaufwands. Wenn auch die Ausbeuten noch gering sind, so zeigen diese Experimente doch, dass es prinzipiell möglich sein muss, den pflanzlichen Lipidstoffwechsel so umzubauen, dass sich essentielle Fettsäuren in Ölpflanzen wirtschaftlich produzieren lassen.[35]
Entgiftung des Baumwollsamens
Beim Abernten eines Baumwollfeldes fallen für jedes Kilogramm Fasern ca. 1,6 kg Samen an. Nach Tonnage gerechnet ist Baumwolle damit nach der Sojabohne die wichtigste Ölpflanze. Die Samen enthalten ca. 21 % Öl und 23 % relativ hochwertiges Protein, das aber wegen seines Gehalts an Gossypol und anderen Terpenoiden als Nahrungs- oder Futtermittel nur eingeschränkt verwertbar ist. Gossypol schädigt Herz und Leber. Theoretisch könnten 44 Megatonnen (Mt) Baumwollsaat, die weltweit jährlich geerntet werden und 9 Mt Protein enthalten, den Jahresproteinbedarf (50g/Tag) einer halben Milliarde Menschen decken. Da Baumwollsamen zur Ölgewinnung gepresst wird, wird der Gossypol-haltige Presskuchen als giftig entsorgt. Dieser Presskuchen von Gossypol-freien Samen wäre einfach als Futtermittel oder Nahrungsmittel zu verwenden. Erste Versuche in den 1970er Jahren Gossypol aus der gesamten Baumwollpflanze zu entfernen, hatten hohe Ertragseinbußen zur Folge, da Gossypol einen wichtigen Fraßschutz darstellt. 2006 berichtete ein Forscherteam von der Texas A & M University[36] selektiv im Baumwollsamen die Gossypolsynthese durch Stilllegung eines der ersten biochemischen Schritte des Gossylpolsynthesewegs mittels RNA-Interferenz unterbrochen zu haben, während sie in den übrigen Pflanzenorganen normal verläuft.[37] In diesen Pflanzen ist der Gossypolgehalt um bis zu 99 % reduziert. Er liegt weit unter dem Grenzwert von 600 ppm (parts per million), den die Weltgesundheitsorganisation (WHO) bei Baumwollsaaten, die zur Verwendung in Lebensmitteln bestimmt sind, für unbedenklich hält.
Neben der Baumwolle kennt man mehrere andere Kulturpflanzen, deren Wert als Nahrungsmittel durch den Gehalt an giftigen Verbindungen stark gemindert wird. Die Samen der Saatplatterbse (Lathyrus sativus), einer tropisch/subtropischen Gemüsepflanze, enthalten ein natürliches Nervengift, das β-N-oxalylamino-L-alanin. Der dauerhafte Genuss ihres Mehls verursacht bei der armen Bevölkerung vieler Länder Asiens und von Teilen Afrikas eine als Lathyrismus bekannte chronische Erkrankung des Nervensystems. Cassava (Maniok) und Favabohnen enthalten cyanogene (Blausäure entwickelnde) Glycoside. Die gentechnische Entgiftung dieser Kulturpflanzen würde nicht nur die Lebensmittelsicherheit verbessern, sondern auch die Versorgung der wachsenden Weltbevölkerung, ohne dass Erträge oder Anbauflächen vergrößert werden müssten.[38]
Biofortifikation
Biofortifikation, die Anreicherung mit Nährstoffen, ist unter anderem mit gentechnischen Methoden möglich.
In den 1990er Jahren wurde von Ingo Potrykus und Peter Beyer durch Einführung von drei Genen aus der Carotinoidsynthese die Reissorte Golden Rice erzeugt, welche deutlich mehr Beta-Karotin, eine Vorstufe zu Vitamin A, sowie einen erhöhten Eisengehalt im Reiskorn enthält.[39] In Ländern, in denen Reis das Hauptnahrungsmittel ist, soll hiermit den weit verbreiteten Mangelerkrankungen begegnet werden. Die an der Entwicklung beteiligte Firma Syngenta verzichtet auf fällige Lizenzzahlungen bei humanitären Projekten, so dass Saatgut für solche Anwendungen kostenlos bezogen werden kann.[40]
2011 entwickelte ACPFG mithilfe der Gentechnik eine nährstoffangereicherte Reislinie, deren Eisengehalt hoch genug ist, um den täglichen Bedarf zu decken. Der Reis enthält das vierfache an Eisen und das doppelte an Zink von konventionellem Reis. Ein derart hoher Eisengehalt ließ sich bisher nicht erzielen und ist mit konventionellen Methoden nicht möglich. Die WHO schätzt, dass weltweit mehr als zwei Milliarden Menschen an Eisenmangel leiden. An dem Forschungsprojekt waren Wissenschaftler der Universitäten von Adelaide, Melbourne und South Australia sowie der Flinders University beteiligt, finanziert wurde es vom Australian Research Council und HarvestPlus.[41]
Antigene und Antikörper
Seit etwa 1999 sind zwei in biochemischen Laboratorien viel gebrauchte rekombinierte Proteine auf dem Markt, die in transgenem Mais produziert werden: Avidin, ein Protein aus Hühnereiweiß und β-Glucuronidase, ein bakterielles Enzym des Kohlenhydratstoffwechsels.[42] Auch das menschliche Proinsulin, die Vorstufe des Insulins, lässt sich nicht nur in transformierten Bakterien sondern auch im Endosperm transgener Maiskörner produzieren.[43] Anfangserfolge gibt es auch bei der Züchtung transgener Mais- und anderer Kulturpflanzen, welche Antigene produzieren, mit denen bei oraler Anwendung eine aktive, die Bildung körpereigener Antikörper auslösende, Schutzimpfung gegen gefährliche Infektionskrankheiten möglich ist. Die Produktion von Impfstoffen in Pflanzen hat gegenüber derjenigen in Tieren oder Mikroorganismen mehrere Vorteile: Die Gefahr einer Kontaminierung des Impfstoffs mit Allergenen oder Krankheitserregern ist weitaus geringer. Die Produktion ist billig, und der Impfstoff ist leicht anzuwenden und deshalb auch in Ländern ohne entwickelte hygienische und medizinische Infrastruktur leicht einsetzbar.[44][45] TGEV, das übertragbare Gastroenteritis-Virus (Transmissible Gastroenteritis Virus), erzeugt bei jungen Schweinen Durchfallerkrankungen. Wenn man Jungschweine mit TGEV-Mais füttert, welcher ein TGEV-Antigen exprimiert, sind die Tiere gegen das Virus geschützt.[46]
Ebenso wie die Herstellung von Antigenen ist auch die Produktion von Antikörpern in Pflanzen im Hinblick auf Kosten, Skalierbarkeit der Produktion und Anwendungssicherheit attraktiv. Antikörper werden für Vorbeugung, Behandlung und Diagnose vieler Krankheiten eingesetzt. In der biomedizinischen Grundlagenforschung braucht man sie für eine Vielzahl analytischer Nachweismethoden. Hergestellt wurden Antikörper pflanzlicher Herkunft bisher vor allem im Tabak, aber auch in Kartoffel, Soja, Alfalfa, Reis und Mais. Allerdings sind darunter nur wenige, die für die Therapie am Menschen in Frage kommen. Ein im Tabak gebildeter Antikörper gegen ein Oberflächenantigen von Streptococcus mutans, dem Hauptverursacher der Zahnkaries, hat sich bei lokaler Anwendung als wirksam erwiesen und kann die Rückbesiedelung der Zahnoberfläche durch die Bakterien wirksam verhindern.[47] Verschiedene andere von Pflanzen gebildete Immunglobuline befinden sich in der klinischen Testphase.[44][48]
Stacked Events
Pflanzen mit einer Kombination aus mehreren Eigenschaften lassen sich oft sehr leicht durch konventionelle Kreuzung transgener Sorten erzeugen. Man spricht hier von Stacked Events (engl. für gestapelt). Auf Grund der Einfachheit dieser Methode werden in Zukunft eine Vielzahl neuer Sorten erwartet.
Marktdaten
Für 2007 wird die Marktgröße transgener Pflanzen auf 6,9, für 2025 auf 50 Mrd. USD geschätzt.[49] Höhere Erträge und bessere Futtermittel sind neben Pflanzen, die beim Anbau weniger Pflanzenschutzmittel benötigen, die Hauptmärkte der Zukunft.[50][51]
Saatguterzeuger
Der weltweite Markt für Saatgut (konventionell und gentechnisch verändert) wird auf 42 Mrd $ geschätzt (2010; EUR/USD = 1,30).[52] und stellt sich als stark fragmentiert dar, wie eine Auflistung der bedeutendsten Hersteller zeigt:
Monsanto (USA) Pioneer Hi-Bred/DuPont (USA) Syngenta (CH) Groupe Limagrain (F) KWS SAAT (D) Bayer CropScience (D) (Rest) Umsatz 2010 (109 $) 7,611[53] 5,300[54] 2,805[55] 1,263[56] 0,950[57] 0,654[58] (2009) Marktanteil 18,1 % 12,6 % 6,7 % 3,0 % 2,3 % 1,6 % 55,7 % Die Zahlen beziehen sich ausschließlich auf den jeweiligen Bereich Saatgut. Der Anteil an GVO-Saat wird von den Firmen in der Regel nicht gesondert angegeben. Der Weltmarkt für GVO-Saatgut wächst deutlich. 2009 ergab sich ein Anstieg von 6,7 % auf 11,2 Mrd. $.[59]
Anbau
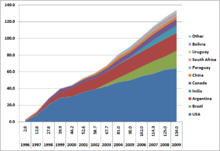
Seit 1996 werden gentechnisch veränderte Pflanzen kommerziell angebaut. Weltweit fand 2010 der Anbau in 29 Ländern durch 15 Millionen Landwirte (davon 90 % in Entwicklungs-/Schwellenländern) auf 148 Millionen Hektar statt.[59] Das entspricht 10,7 % des weltweit nutzbaren Ackerlandes (laut FAO-Definition 1,38 Milliarden Hektar [2008])[60] bzw. dem 7,9-fachen der gesamten deutschen Landwirtschaftsfläche (18,8 Millionen Hektar [2008]).[61]
Die bedeutendsten Anbauländer sind (Anteil der gesamten Landwirtschaftsfläche [2008])[62]:
Rang Land Fläche (106 ha) Anteil Pflanzen 1 USA 66,8 39 % Sojabohne, Mais, Baumwolle, Raps, Kürbis, Papaya, Luzerne, Zuckerrüben 2 Brasilien 25,4 42 % Soja, Mais, Baumwolle 3 Argentinien 22,9 72 % Soja, Mais, Baumwolle 4 Indien 9,4 6 % Baumwolle 5 Kanada 8,8 20 % Raps, Mais, Soja, Zuckerrüben 6 China 3,5 3 % Baumwolle, Tomaten, Pappeln, Petunien, Papaya, Paprika 7 Paraguay 2,6 62 % Soja 8 Pakistan 2,4 12 % Baumwolle 9 Südafrika 2,2 15 % Soja, Mais, Baumwolle 10 Uruguay 1,1 67 % Soja, Mais Zulassung, Kennzeichnung und Koexistenz
Bestehende Regelungen
Es gibt kein weltweit einheitliches Verfahren für die Zulassung von Gv-Pflanzen zum Anbau oder zur Verwendung als Lebens- und Futtermittel. Jedes Land hat seine eigenen Gesetze dazu. Einige Länder regulieren Gv-Pflanzen auf Basis bestehender Gesetzgebung, andere erschaffen neue Gesetze, die spezifisch für Gv-Pflanzen gelten. Eine Herangehensweise ist das in der EU befolgte Vorsorgeprinzip. Lebensmittel mit Gv-Anteil werden aufgrund des Herstellungsprozesses als neuartige Lebensmittel behandelt (prozessbezogen, process based). Ein neues Gv-Produkt gilt unabhängig von seiner Zusammensetzung zunächst als riskant, bis ausreichende Tests durchgeführt wurden, um seine Sicherheit zu gewährleisten. Eine Kennzeichnung von Lebensmitteln mit gv-Anteilen ist außerhalb festgelegter Beimischungsgrenzen verpflichtend. Im Gegensatz basieren die Regeln in den USA in erster Linie auf dem Prinzip der Substanziellen Äquivalenz. Lebensmittel mit Gv-Anteil werden wie Lebensmittel ohne Gv-Anteil behandelt, wenn dieselbe Zusammensetzung im Endprodukt besteht (produktbezogen, product based). Kennzeichnung ist freiwillig. Andere Länder folgen entweder dem EU- oder dem US-Modell, oder einer Kombination.[63], oder einer eigenen Regelung.
EU
Die in der EU maßgeblichen Anforderungen für eine Genehmigung sind die Freisetzungsrichtlinie[64] (Zulassung zum Anbau) und die Verordnung (EG) Nr. 1829/2003[65] (Zulassung als Lebens- und Futtermittel). Zur Zulassung wird zunächst ein Antrag bei national zuständigen Behörden eingereicht, der unter anderem Angaben zu durchgeführten Studien enthalten muss, die zeigen, dass keine nachteiligen Auswirkungen auf Mensch, Tier und Umwelt zu erwarten sind, und einer Analyse, dass das Gv-Lebensmittel sich nicht wesentlich von konventionellen Vergleichsprodukten unterscheidet. Der Antrag wird nach Prüfung durch die nationale Behörde an die Europäische Behörde für Lebensmittelsicherheit (EFSA) weitergeleitet. Die EFSA prüft den Antrag, ergänzt ihn um Vorschläge zur Kennzeichnung, zum Monitoring und Nachweisverfahren und gibt innerhalb von sechs Monaten eine Stellungnahme auf Basis des Gutachtens eines unabhängigen Expertengremiums (GMO Panel) ab. Danach wird der Antrag an die EU-Kommission weitergeleitet. Die Kommission legt den Antrag dem Ständigen Ausschuss für die Lebensmittelkette vor, in dem alle Mitgliedsstaaten vertreten sind. Mit qualifizierter Mehrheit kann der Ausschuss eine Stellungnahme zum Antrag abgeben. Erfolgt die Stellungnahme nicht oder weicht sie vom Antrag ab, leitet die Kommission ihren Entscheidungsvorschlag an den Ministerrat weiter und informiert das EU-Parlament. Der Ministerrat hat dann 90 Tage Zeit, über den Beschlussvorschlag der Kommission mit qualifizierter Mehrheit zu entscheiden. Lehnt der Rat den Vorschlag der Kommission ab, arbeitet die Kommission einen neuen Vorschlag aus. Andernfalls setzt die Kommission den von ihr vorgeschlagenen Rechtsakt in Kraft.[66]
2003 wurden die Leitlinien für die Koexistenz gentechnisch veränderter, konventioneller und ökologischer Kulturen (Richtlinie 2003/556/EG vom 23. Juli 2003) formuliert.[67] Dabei wurde seitens der EU, die es bis in die 2000er abgelehnt hatte, EU-weite Regelungen und klare Haftungsbestimmungen zu Herstellung und Inverkehrbringen von Produkten aus oder durch GVO zu erarbeiten, weil sie keine pauschalen Einschränkungen einer wirtschaftlichen Maßnahme erlaubt, der Begriff der Koexistenz geschaffen, der in der Kernaussage bedeutet, „dass die Landwirte unter Einhaltung der Etikettierungs- und Reinheitsvorschriften eine echte Wahl zwischen konventionellen, ökologischen oder GV-Produktionssystemen haben“ sollen.[68] 2008 wurde das Europäische Büro für Koexistenz (am Institute for Prospective Studies des JRC, kurz IPTS-JRC, in Sevilla) eingerichtet, das die Wirksamkeit technischer Koexistenzmaßnahmen weiter verbessern soll.
Um einen bewussten Einsatz der Gentechnik von einer zufälligen, technisch nicht mehr beeinflussbaren Beimischung rechtlich abzugrenzen, werden Schwellenwerte eingeführt. In der EU beträgt dieser Wert für Futter- und Lebensmittel 0,9 %, auch für Bio-Lebensmittel. Dieser Wert gilt allerdings nur dann, wenn der betreffender Hersteller nachweisen kann, dass es sich bei den Beimischungen um zufällige GVO-Einträge handelt. Bei Überschreitung besteht eine Kennzeichnungspflicht. Zusatzstoffe sind hiervon grundsätzlich ausgenommen, ebenso die Erzeugnisse konventioneller Nutztiere, die mit Gv-Futtermitteln gefüttert wurden.[69] In Deutschland gibt es die freiwillige Kennzeichnung Ohne Gentechnik, die Vermischungen bis zum EU-Schwellenwert sowie die Fütterung mit Gv-Futterpflanzen bis zu einem bestimmten Zeitpunkt vor der Schlachtung/Eiablage toleriert.[70]
Für Saatgut existiert ein Vorschlag der EU-Kommission. Der Wert soll so bemessen sein, dass die Ernteprodukte mit Sicherheit unter der Kennzeichnungspflicht liegen. Für Raps sollen 0,3 % nicht überschritten werden, für Zuckerrüben, Mais und Kartoffeln 0,5 %. Von Kritikern wird ein Wert von 0,1 % gefordert, ab der eine quantitative Bestimmung technisch möglich ist.[71] Für in der EU nicht zugelassene Gv-Pflanzen gilt eine Nulltoleranz, auch wenn sie in anderen Ländern erlaubt sind oder wenn es sich um eine Kreuzung zugelassener Sorten handelt. Die Europäische Kommission und mehrere Mitgliedsstaaten drängten in der Vergangenheit auf eine Anhebung der Toleranzschwelle auf 0,1%; diese Vorschläge fanden jedoch bisher keine Mehrheit.[72] Auf Grund der noch herrschenden Rechtsunsicherheit kommt es immer wieder zu Berichten in den Medien, weil Behörden auf die geringfügige Beimischung von GVO-Saatgut in konventionellen Chargen uneinheitlich reagieren.[73]
Die Auflagen der EU sind damit die strengsten der Welt. Zudem dürfen Mitgliedsstaaten weitere Auflagen bestimmen. Die Abstandsregelungen für Gv-Felder variieren daher stark zwischen den EU-Ländern. In Spanien, dem EU-Staat mit der größten Gv-Anbaufläche (etwa 50 % des Maisanbaus in Katalonien und Aragonien ist bereits transgen), ist für Mais ein Abstand zu konventionellen Feldern von 50 m vorgeschrieben. In Deutschland gilt ein Mindestabstand von 150 m zwischen gv- und konventionellen Maisfeldern, und 300 m zwischen gv- und ökologischen Maisfeldern. In Österreich gelten die strengsten Koexistenzregeln: Hier müssen Landwirte für jedes Feld und jede Pflanze eine behördliche Genehmigung ersuchen, wenn sie transgenes Saatgut verwenden wollen. Zudem müssen spezielle Trainingskurse absolviert werden, und es gelten strenge Haftungsregelungen. Der Europäische Gerichtshof erklärte den Versuch mehrerer österreichischer Bundesländer, sich als gentechnikfreie Regionen nach der Charta von Florenz zu etablieren, als Verstoß gegen die Wahlfreiheit von Landwirten und Verbrauchern.[74] Die Empfehlung 2010/C 200/01,[67] die die alte 2003/556/EG aufhebt, schlägt hingegen vor, dass Mitgliedsstaaten in Zukunft Verbote auch aus nichtwissenschaftlichen Gründen verfügen dürfen. [75] EU-Parlament und Ministerrat haben noch nicht über diese Empfehlung abstimmt und es wurden verschiedene Bedenken gegen sie geäußert, wie mögliche Verstöße gegen die Welthandels- und EU-Binnenmarktverträge.[76] Laut einem im November 2010 vorgelegten Gutachten des juristischen Dienstes des Europäischen Rats verstoßen die Pläne der EU-Kommission gegen die Welthandelsverträge und die Verträge des Europäischen Binnenmarkts.[77] Als problematisch gelten daneben mögliche Begründungen, die ein Land laut dem Komissionsvorschlag für ein nationales Anbauverbot nutzen könnte. Wissenschaftliche Zweifel an der Sicherheit von Gv-Pflanzen sind in dem Vorschlag nicht vorgesehen, sie sollen weiter einheitlichen Zulassungsverfahren für alle EU-Länder bindend beantwortet werden.[78]
Andere Länder
In den USA sind für die Regulation von Gv-Pflanzen das USDA, die EPA und die FDA verantwortlich. Die Gesetzgebung ist produktbezogen (product based), Kennzeichungen sind freiwillig, und die Beimischungsgrenze beträgt 5 %.[63]
In Kanada, Taiwan, Bangladesch, auf den Philippinen sowie in Argentinien und Südafrika ist die Gesetzgebung ebenfalls produktbezogen (product based). Im Vereinigten Königreich, in Australien, Neuseeland, China, Japan, Indien, Brasilien, Mexiko, Burkina Faso, Ägypten, Kenia, Sambia und Nigeria ist die Gesetzgebung prozessbezogen (process based). Kennzeichnung ist freiwillig in Kanada, auf den Philippinen, in Argentinien und Südafrika; verpflichtend im Vereinten Königreich, in Australien, Neuseeland, China, Japan, Taiwan, Chile, Brasilien und Mexiko. Die Beimischungsschwelle liegt bei 5 % in Kanada, Japan, Taiwan, und auf den Philippinen. In anderen Ländern, für die Informationen vorliegen, liegt sie bei 1 %.[63]
Viele Entwicklungsländer haben noch keine umfassenden gesetzlichen Grundlagen für die Zulassung von und den Verkehr mit transgenen Pflanzen geschaffen.
Internationale Abkommen
Die nationale Gesetzgebung bewegt sich innerhalb von Spielräumen, die durch internationale Abkommen abgesteckt sind, welche eine Harmonisierung vorantreiben sollen:[63]
- Die WTO zielt auf einen Abbau von Handelsbarrieren. Das Abkommen über sanitäre und phytosanitäre Maßnahmen (SPS) setzt Richtlinien bezüglich Lebensmittelsicherheit und Pflanzengesundheit. Das Übereinkommen über technische Handelshemmnisse (TBT) soll den Abbau von unnötigen Vorschriften zu Zulassungen, Tests und Standards vorantreiben, die den Handel behindern.
- Der Internationale Vertrag über pflanzengenetische Ressourcen für Ernährung und Landwirtschaft der FAO soll Nutzung und Austausch von pflanzengenetischen Ressourcen regeln.
- Der Codex Alimentarius der FAO bietet Empfehlungen und Richtlinien bezüglich der Lebensmittelsicherheit. Schlichtungsverfahren (Adjudication) der WTO greifen auf den Codex zurück.
- Das Cartagena-Protokoll regelt den internationalen Verkehr von GVO, wenn dieser mögliche Auswirkungen auf die Biodiversität hat.
- Die OECD ist bestrebt, internationale Regulationen und Standards zu harmonisieren.
Unterschied zwischen USA und EU: Gründe
In den USA dauert der Zulassungsprozess eines transgenen Events durchschnittlich 15 Monate, in der EU 40.[79] Für die deutlichen Unterschiede zwischen den USA und der EU bei der Regulierung der Grünen Gentechnik gibt es in der Wissenschaft unterschiedliche Erklärungsansätze, die seit Jahren diskutiert werden. Einige gehen davon aus, dass die Konsumenten in der EU der Gentechnik gegenüber negativer eingestellt wären als US-Konsumenten, dass Lebensmittelskandale (z.B. BSE oder Dioxin) in den 1990er Jahren stärkere Regulierung zur Folge hatten, oder dass das Vertrauen der Konsumenten in die Regulierungsbehörden in der EU niedriger ist. Andere Forscher argumentieren, dass die Regulierung in den USA deswegen weniger strikt ist, weil die dortigen Landwirte aus der Grünen Gentechnik einen größeren Nutzen ziehen könnten als EU-Landwirte. Ein weiterer Erklärungsansatz lautet, der Unterschied sei durch die relative Stärke europäischer Unternehmen auf dem traditionellen Pflanzenschutzmarkt begründet, zu dem die transgenen Pflanzen der ersten Generation in Konkurrenz stehen. Jeder dieser Erklärungsversuche weist jedoch Schwächen auf; es besteht in der Wissenschaft keine Einigkeit über die Ursachen für die Unterschiede.[80]
Ein weitere Erklärung zur restriktiven Haltung der EU sehen Tait und Barker (2011) in einer erheblichen Einflussnahme von Nichtregierungsorganisationen und Branchenvertretern der Ökologischen Landwirtschaft, welche die Grüne Gentechnik ablehnen. Die Möglichkeit dieser Einflussnahme sei in den 1980er Jahren geschaffen worden, als Europa sich von einer Top-down-Regierung auf eine Bottom-up-Governance hinbewegte, in welcher der Staat nicht mehr primär der alleinige Macher von Politik ist, sondern die Interaktionen zwischen gesellschaftlichen Gruppen fördert. Mitte der 1980er Jahre setzte sich zudem das aus Deutschland stammende Vorsorgeprinzip zur Regulierung neuer Technologien in Europa durch. Die Folge sei ein großer Einfluss politisch motivierter Akteure, die die Grüne Gentechnik auf nichtwissenschaftlicher Basis seit Mitte der 1990er Jahre erfolgreich behindern.[81]
Kritik der Restriktion
Viele Wissenschaftler kritisieren die starken rechtlichen Einschränkungen der Entwicklung und des Einsatzes von transgenen Pflanzen in einigen Ländern. Durch eine solche Überregulierung entstünden insbesondere in Entwicklungsländern hohe Kosten durch den entgangenen Nutzen.[81][82] Auch hätten viele Vorschriften, wie Abstandsregelungen, schlichtweg keine wissenschaftliche Basis.[74][81][83] Insbesondere in Europa würde ein repressives System mögliche Risiken betonen und dabei positive Folgen für Wirtschaft, Umwelt und Gesundheit außer Acht lassen.[63][84] Eine Kernempfehlung einer von der päpstlichen Akademie der Wissenschaften im Mai 2009 einberufenen Expertenrunde lautet, die Grüne Gentechnik von „exzessiver und unwissenschaftlicher Regulierung zu befreien“. Insbesondere spricht sie sich für eine Revision des Cartagena-Protokolls aus, das europäisch geprägte Regulierung in Entwicklungsländer exportiere (der Vatikan erklärte, das Abschlussdokument dürfe nicht als Erklärung der päpstlichen Akademie der Wissenschaften oder des Vatikans verstanden werden.[85]).[86] Verbraucherorganisationen fordern hingegen strengere Zulassungsverfahren und Kennzeichnungspflichten.[87]
Zulassung
Vor der Zulassung neuer transgener Sorten müssen oft jahrelange Versuchsreihen durchgeführt werden. Es wird geschätzt, dass die Kosten für die Zulassung einer transgenen Maissorte in einem Land zwischen 6 und 15 Millionen US$ betragen. Diese Summen werden vom Antragsteller bezahlt.[88] Die hohen Kosten reduzieren die Innovationsraten und behindern insbesondere die Verbreitung von transgenen Pflanzen in kleineren Ländern mit schwächerer Nachfrage. Die hohen Kosten tragen auch zu einer Konzentration der Saatgutindustrie bei, da kleinere Firmen und öffentliche Forschungseinrichtungen die hohen Summen oft nicht leisten können.[81][82]
Zusätzlich entstehen Kosten, die sich durch den entgangenen Nutzen einer möglicherweise sicheren, aber noch nicht zugelassenen Sorte ergeben (Fehler 2. Art). Es wird geschätzt, dass ein zweijähriger Verzug der Zulassung einer Bt-Baumwollsorte in Indien Verluste für die Landwirte von mehr als 100 Millionen US$ bedeutet.[89]
Laut Ingo Potrykus ist die über 10-jährige Verzögerung der Zulassung des Goldenen Reis für den Verlust von Millionen Menschenleben verantwortlich. Er bezeichnet die extreme Auslegung des Vorsorgeprinzips anstelle einer wissenschaftlich gerechtfertigten Regulierung als Verbrechen gegen die Menschheit.
Verbraucher- und Umweltschutzorganisationen fordern strengere Zulassungskriterien, da ungeklärte Gesundheits- und Umweltrisiken bestünden.[87]
Kennzeichnungspflicht
Da transgene Lebensmittel als gesundheitlich unbedenklich eingestuft sind, wenn sie zugelassen werden, sei eine Kennzeichnungspflicht unsinnig. Wenn Konsumenten für gentechnikfreie Nahrungsmittel mehr bezahlen wollen, würden die Lebensmittelhersteller freiwillig kennzeichnen. In der EU besteht hingegen eine Kennzeichnungspflicht, die erstens deutlich teurer ist und zweitens suggeriere, dass transgene Lebensmittel ein gesundheitliches Risiko bergen.[90] Diese Pflicht wird begründet mit dem Right-to-know-Prinzip, welches im Gegensatz zum Need-to-know-Prinzip zur Rechtfertigung der Vermittlungspflicht praktisch jeder Art von Information verwendet werden kann und daher kritisiert wird.[91]
Verbraucher- und Umweltschutzorganisationen hingegen befürworten eine Kennzeichnungspflicht, da ungeklärte Gesundheitsrisiken bestünden und der Verbraucher daher ein Informationsrecht habe.[87]
Koexistenz
Die EU-Richtlinien zur Koexistenz (2003/556/EC)[67] sehen vor, dass Abstandsregeln den wissenschaftlichen Kenntnisstand bezüglich der Beimischungswahrscheinlichkeit widerspiegeln sollen. Wissenschaftler kritisieren, dass sich viele EU-Mitgliedsstaaten darüber hinwegsetzen, und dass die Mindestabstände willkürlich, exzessiv und politisch motiviert seien.[74][81][83] So gilt in Luxemburg ein Mindestabstand von 600 m für Mais, während er in den Niederlanden bei 25 m liegt. In Spanien sind 50 m vorgeschrieben, in Portugal 200 m.[92] In Lettland ist für Raps ein Abstand von 4 km (bzw. 6 km zu ökologischen Feldern) vorgeschrieben. Dies würde erhebliche Kosten für Landwirte darstellen, die transgenes Saatgut verwenden wollen, und ihre Wahlfreiheit unnötig einschränken. Eine Metaanalyse von Auskreuzungsstudien bei Mais kam zu dem Schluss, dass ein Abstand von 50 m ausreichen würde, um eine Auskreuzung unter 0,5 % sicherzustellen.[74]
Probleme im Agrarhandel
Die teils schnelle Einführung der Grünen Gentechnik in anderen Ländern der Welt und die restriktive Zulassungspraxis in Europa führen zu immer größeren Problemen im Agrarhandel. Die USA, Kanada und Argentinien hatten 2003 die EU vor der WTO verklagt und bekamen 2005 in den meisten Punkten Recht. Seither wird über eine Regelung verhandelt.[93] Nachdem die EU im März 2009 die Einfuhr von gentechnisch verändertem T45-Raps als Lebens- und Futtermittel erlaubt hatte,[94] legten im Juli 2009 Kanada und die EU ihren Streit nieder und vereinbarten, sich zweimal jährlich zu weiteren Konsultationen zu treffen.[95]
Ein Gutachten der Gemeinsamen Forschungsstelle der EU-Kommission befürchtet, dass die Preise für Agrarprodukte ohne Beimischungen der zahlreichen Gv-Pflanzen, die in anderen Ländern angebaut werden, deutlich steigen werden. Bis 2015 wird ein Anstieg der kommerziell genutzten Gv-Merkmale von 30 auf 120 im Jahr 2009 erwartet.[96] Eine Arbeitsgemeinschaft Innovativer Landwirte sieht sich gegenüber der Konkurrenz aus anderen Ländern zunehmend benachteiligt.[97]
Der europäischen Tierhaltung und Futtermittelbranche entstünde laut Deutscher Verband Tiernahrung e. V. ein Schaden von 3,5 bis 5 Mrd. €, da immer wieder Lieferungen mit Spuren von GVO zurückgewiesen werden müssten. Im außereuropäischen Ausland könnten dieselben Futtermittel verwendet werden und damit erzeugte tierische Lebensmittel hätten im Prinzip ungehindert Marktzutritt in Europa.[98]
Sozioökonomische Auswirkungen
Produktivitätszuwachs
Nach Schätzungen der FAO der Vereinten Nationen waren 2010 etwa 925 Millionen Menschen unterernährt.[99] Die Weltbank erwartet, dass im Jahr 2030 ungefähr 50 % mehr Lebensmittel benötigt werden als heute.[100] Aufgrund der steigenden globalen Bevölkerung von ca. 6,7 Mrd. Menschen 2008 auf ca. 8,3 Mrd. Menschen bis 2030[101] auf der einen Seite, und der global begrenzten landwirtschaftlichen Nutzfläche andererseits, wird es in unmittelbarer Zukunft zu steigender Nachfrage nach Lebensmitteln kommen. Eine steigende Nachfrage nach Lebensmitteln bei immer langsamer steigender Produktivität der konventionellen Züchtung führt zu steigenden Lebensmittelpreisen. Dies wiederum führte in den armen Regionen der Welt wie Afrika und Asien zu einem Anstieg in der Zahl hungernder Menschen.[102][103]
Angesichts von Ressourcenknappheit und wachsender Weltbevölkerung seien Produktivitätszuwächse somit unabdinglich für eine ausreichende Verfügbarkeit von Nahrungsmitteln und anderen Rohstoffen.[104] Ertragszuwächse bei Pflanzen der ersten Generation wurden beobachtet für Baumwolle, Soja, Mais und Raps.[105] Ein 2010 veröffentlichtes Review von 49 Studien ergab, dass in 74 % der Ergebnisse Ertragszuwächse beobachtet wurden. 19 % der Ergebnisse sind neutral, und 7 % negativ. In Entwicklungsländern wurden dabei deutlich stärkere Ertragszuwächse (16-30 %) als in Industrieländern (0-7 %) festgestellt. Die negativen Ergebnisse traten dabei in den ersten Jahren nach der Zulassung auf und sind dadurch zu erklären, dass die transgenen Eigenschaften anfangs in nur wenige Sorten eingebracht wurden, die damit und aufgrund langer Zulassungsprozesse nicht mehr auf dem neuesten Züchtungsstand und nicht lokal angepasst waren. Nachdem die transgenen Eigenschaften nach einigen Jahren in einer weitaus größeren Zahl von Sorten verfügbar war, konnten auch kaum noch negative Ergebnisse beobachtet werden.[106]
Dem Argument, Gentechnik zur Bekämpfung des Hungers einzusetzen, wird entgegnet, dass der Hunger nicht nur ein Produktions- sondern vor allem ein Verteilungsproblem sei. Der Soziologe Jean Ziegler sagt unter Berufung auf Daten der FAO, dass mit derzeitigen und konventionellen Mitteln bis zu 12 Milliarden Menschen ausreichend ernährt werden könnten, und bezeichnet jeden Hungertod als Mord.[107]
Die Auffassung, dass eine Steigerung der landwirtschaftlichen Produktivität keinen wichtigen Beitrag zur Hungerbekämpfung leiste, wird in der Wissenschaft nicht geteilt.[108] So zeigt die Erfahrung der Grünen Revolution, dass hierdurch geschätzte 187 Millionen Menschen vor Hunger bewahrt wurden.[109]
Einkommensverbesserung
Einkommenszuwächse konnten bei transgener Baumwolle, transgenem Mais, transgenem Raps und transgener Sojabohne nachgewiesen werden. Ein 49 Studien umfassendes Review der wissenschaftlichen Literatur zu den Auswirkungen von transgenen Pflanzen auf landwirtschaftliche Einkommen zeigt in 72 % der Resultate einen positiven, in 11 % einen neutralen, und in 16 % einen negativen Einfluss. In Entwicklungsländern ist der Anteil positiver Ergebnisse signifikant höher (ca. 75 %) als in Industrieländern (ca. 65 %). Hinzu kommen nicht-monetäre Nutzenzuwächse in Form von Arbeitseinsparungen, erhöhter Flexibilität, geringerem Risiko, sowie größerer Sicherheit, die für die USA auf durchschnittlich $12 pro Hektar für herbizidresistente Pflanzen bzw. $10 für insektenresistente Pflanzen geschätzt wurden.[106] Zudem profitierte der konventionelle Anbau vom Anbau insektenresistenter Pflanzen in seiner Umgebung (siehe Abschnitt Umweltschutz).
In Studien, die Einkommensverbesserungen durch Gv-Pflanzen entlang unterschiedlicher Betriebsgrößen gemessen haben, ergaben sich zumeist insbesondere Vorteile für Haushalte mit geringerem Landbesitz. Hinzu kommt eine Verringerung des Einkommensrisikos, das für Kleinbauern vergleichsweise wertvoller ist als für größere Betriebe, die über mehr Instrumente zur Risikoreduktion verfügen.[106]
Die FAO erwartet, dass transgene Pflanzen ebenso wie andere verbesserte Saatguttechnologien in der Vergangenheit in Zukunft eine wichtige Rolle bei ländlicher Einkommenssteigerung und Armutsbekämpfung spielen werden.[110][111][112]
Dominanz multinationaler Konzerne
Heute befinden sich mehr als 75 % aller Patente der Grünen Biotechnologie in privater Hand, größtenteils von wenigen multinationalen Konzernen.[113] Diese Möglichkeit stellt einen Anreiz für die Forschung dar. Gleichzeitig hat dies dazu geführt, dass die Entwicklung neuer transgener Sorten durch Nichtinhaber relevanter Patente häufig mit hohen Transaktionskosten und Lizenzgebühren verbunden ist.[114] Dies könnte den Konzentrationsprozess weiter verstärken. Durch eine sinkende relative Bedeutung von öffentlicher Forschung und Entwicklung könnte insbesondere die gentechnische Verbesserung von weniger verbreiteten Pflanzenarten sowie in kleinen Entwicklungsländern vernachlässigt werden.[115][116][112]
Tewolde Berhan Gebre Egziabher wirft Saatgutherstellern vor, sie würden Landwirte in eine Abhängigkeit nach ihren Produkten zwingen und bezeichnet dies als effektiven Kolonialismus.[117] Ronald Herring hat während der raschen Adoption von Bt-Baumwolle in Indien beobachtet, dass legale Bt-Saaten unter starken Konkurrenzdruck gerieten, wenn die Preise zu hoch waren oder die Beschaffung zu bürokratisch. Die massenhafte unautorisierte Vermehrung von Bt-Pflanzen und Einkreuzung in lokale Sorten durch die Landwirte widersetze sich den „europäischen Erzählungen von Macht über Bio-Eigentum“.[118]
Den Fragen, ob die Grüne Gentechnik Konzentrationsprozesse in der Saatgutindustrie verstärkt hat und ob Konzentrationsprozesse die Innovation verlangsamt haben, ging eine Untersuchung (2011) im Auftrag der niederländischen Kommission für genetische Modifikation (COGEM) nach. Eine deutliche Konsolidierung hat in den letzten Jahren stattgefunden, so lag der Marktanteil der neun größten Saatgutunternehmen 1985 bei 12,7 % und 1996 bei 16,7 %, während der Marktanteil der drei größten Saatgutunternehmen 2009 auf 34 % angestiegen war. Neben Fortschritten der Pflanzenwissenschaften und -züchtung haben geistige Eigentumsrechte im Bereich der Pflanzenzüchtung und Biotechnologie sowie steigende Ausgaben für Forschung und Entwicklung zu diesem Konsolidierungsprozess beigetragen. Da sich auch in Märkten mit von der Gentechnik nicht berührten Züchtungstechnologien Konzentrationen ereigneten, variiert die Bedeutung der Gentechnik als Treiber dieser Prozesse. Befragungen von 11 Topmanagern der Saatgutindustrie ergaben, dass geistige Eigentumsrechte und Patente von einigen als förderlich und von anderen als behindernd für Innovation gesehen werden. Einer ökonomischen Analyse der relativ stark konzentrierten Saatgutmärkte für Baumwolle, Mais und Sojabohne in den USA zufolge hatte die Konzentration keine negativen Auswirkungen auf die Innovationsraten. Die Autoren der Studie erwarten, dass hohe Kosten für Forschung und Entwicklung sowie für Zulassungen, Monitoring und Beimischungen kleinere Unternehmen und öffentliche Forschungseinrichtungen behindern und weitere Konzentration der Saatgutindustrie befördern werden.[119]
Lebensmittelpreise
In einem im Jahr 2010 veröffentlichten Arbeitspapier äußert Professors Edward Yu von der Universität Tennessee die Vermutung, dass Gentechnik sozioökonomische Vorteile bietet, indem sie einen preismindernden Einfluss auf die globalen Lebensmittelpreise ausübt. Die Preise von Mais, Sojabohnen und Raps sollen demnach um 5,8 %, 9,6 % bzw. 3,8 % niedriger sein, als sie es ohne den Einsatz dieser Technik wären.[120]
Regionaler Strukturwandel
Der Verzicht auf gentechnisch veränderte Produkte kann auf einzelne Industrien bzw auf bestimmte Regionen große Auswirkungen haben. In Österreich und in Deutschland kam es in den letzten Jahren beispielsweise zu einem beschleunigten Strukturwandel in der landwirtschaftlichen Produktion von Schweinen bedingt durch hohe Futtermittel- und Energiekosten.[121][122] So sank die Anzahl der Österreichischen Schweineproduzenten seit 1980 von über 200.000 auf unter 40.000.[123] In Deutschland verringerte sich die Anzahl der Schweine haltenden Landwirte um 10 % auf 73.100 in nur einem Jahr[124] und bedroht somit ganze Regionen wie Nordwestdeutschland, wo fast ein Drittel der Arbeitsplätze von der Schweineproduktion abhängen.[125]
Resistenzbildung
Ein bekanntes Problem des Pflanzenschutzes ist die Resistenzbildung von Schädlingen gegen Pflanzenschutzmittel über den natürlichen Mechanismus von Mutation und Selektion. Dass Schadinsekten bzw. Unkräuter auch bei Einsatz der grünen Gentechnik Resistenzen gegen Bt-Toxine bzw. Herbizide entwickeln können, ist wissenschaftlich unbestritten. Verschiedene Gegenmaßnahmen, wie Refugienflächen und die Kombination mehrerer Wirkstoffe, erschweren die Resistenzbildung.[126][127]
Resistenz gegen Glyphosat
Eine zwischen 2000 und 2004 durchgeführte britische Studie untersuchte, inwiefern herbizidresistenter Raps seine Resistenzeigenschaft auf verwandte Arten überträgt. Im ersten Versuchjahr konnte bei einer Untersuchung von 95.459 artverwandten Pflanzen eine Auskreuzung des Resistenzgens auf zwei Rübsenpflanzen festgestellt werden. Im Folgejahr konnte in den Versuchsfeldern die Auskreuzung der Resistenz auf eine Acker-Senf-Pflanze nachgewiesen werden.[128] Die an der Studie beteiligten Wissenschaftler betonen hingegen, dass keine zweite Studie eine Auskreuzung feststellen konnte, dass die Wahrscheinlichkeit einer Auskreuzung sehr gering sei, und dass die Auskreuzung in wilde Verwandte kein Problem darstelle, da Herbizidresistenz in der Wildnis keinen Fitnessgewinn bringe.[128] Sie weisen aber darauf hin, dass der Anbau herbizidresistenter Raps-Sorten dazu führen könne, dass herbizidresistenter Durchwuchsraps (d.h. Rapspflanzen, die als Folge des Überlebens von Rapssamen in Folgekulturen wieder heranwachsen) die Unkrautbekämpfung bei der Folgefrucht erschweren könnte, insbesondere, wenn in der Fruchtfolge andere herbizidresistente Ackerfrüchte verwendet werden.[128] Die Schweizer Arbeitsgruppe Gentechnik (SAG) fügt hinzu, dass mehrfach resistenter Raps (d.h. Rapssorten, die nach der Übertragung von Genen aus anderen Sorten neue und damit mehrfache Resistenzen gegen Herbizide ausgebildet haben) ebenfalls agronomische Probleme bereiten könne, und behauptete 2003, dass transgener Durchwuchsraps in manchen Gegenden Kanadas schon zu den häufigsten Unkräutern gehöre.[129] Drei Viertel der kanadischen Landwirte, die transgenen Raps anbauen, gaben 2005 in einer Umfrage an, dass die Kontrolle von Durchwuchs bei gentechnisch verändertem Raps kein größeres Problem darstellt als bei konventionellem Raps.[130]
Wahrscheinlicher als eine Auskreuzung des für die Herbizidresistenz verantwortlichen Gens von transgenen Nutzpflanzen auf Unkräuter ist die Herausbildung von Resistenzen durch zufällige Mutation und natürliche Selektion von Unkräutern. Resistenzen gegen Glyphosat in Feldern mit herbizidresistenten transgenen Nutzpflanzen wurden bis 2008 bei 9 Arten beobachtet, davon fast alle in den USA. Resistenzen gegen Glyphosat in Feldern ohne herbizidresistente transgene Nutzpflanzen wurden bis 2008 bei 6 Arten in 12 Ländern auf allen Kontinenten beobachtet.[131] Laut der Organisation WeedScience gibt es weltweit 19 glyphosatresistente Unkräuter (Stand: 2010). Mit 107 resistenten Unkrautarten ist die Gruppe der ALS-Inhibitoren (Acetolactat-Synthase), welche die Grundlage für andere häufig verwendete chemische Unkrautbekämpfungsmittel sind, am stärksten betroffen. Bei allen Herbizidkategorien zusammengenommen sind es 347 (Stand: 2010).[132] Wissenschaftler fordern eine stärkere Diversifikation der Unkrautbekämpfung, etwa mithilfe von Herbiziden, in denen Glyphosat mit anderen Wirkstoffen kombiniert wird, mithilfe von transgenen Nutzpflanzen mit entsprechend zusätzlichen Herbizidresistenzen, und nicht-Herbizid-basierten Unkrautbekämpfungsmaßnahmen. So soll die Resistenzentwicklung von Unkräutern verlangsamt werden, damit Glyphosat weiter effektiv verwendet werden kann.[131] Die in den USA beobachtete Glyphosatresistenz des Unkrauts Amaranthus palmeri beruht auf einer starken Genamplifikation des EPSPS Gens, und nicht durch Auskreuzung des Trangens.[133]
Resistenz gegen Bt-Toxine
Ebenso wie sich in der Vergangenheit Resistenzen von Schadinsekten gegen chemische Insektizide gebildet haben, könnten sich in Zukunft Resistenzen gegen Bt-Toxine entwickeln. Im Feld wurde diese Möglichkeit 2002 für Schmetterlinge dokumentiert. In Mississippi und Arkansas hat die Empfindlichkeit des Baumwollkapselbohrers gegenüber dem in den ersten Bt-Sorten vorrangig eingesetzten Bt-Toxin Cry1Ac bereits deutlich abgenommen. Eine Resistenzbildung wurde nicht in anderen Regionen der USA, oder in China, Spanien oder Australien festgestellt. Auch bei 5 anderen wichtigen Schädlingen wurden bisher keine Resistenzen gegen Bt-Toxine beobachtet.[134][135]
Um Resistenzbildungen zu verzögern, werden sogenannte „refuge strategies“ (Zuflucht-Strategien) empfohlen. So schreibt die EPA die Entwicklung und Umsetzung von Resistenzvermeidungsstrategien bei Bt-Pflanzen vor. Auch in Indien wird die Einhaltung von Refugienflächen empfohlen. Hierbei wird auf einem Teil des Bt-Felds (5-20 %) konventionelles Saatgut gesät. Hierdurch können Bt-empfindliche Individuen überleben und sich mit Bt-resistenten Individuen paaren, womit die Entwicklung von Resistenzen verlangsamt wird.[136][134] Eine weitere Option zur Unterdrückung der Resistenzbildung ist die Freisetzung von sterilen Schadinsekten, was laut Computersimulationen möglich ist und in einem vierjährigen Feldversuch bestätigt wurde.[137]
In vier Distrikten des indischen Bundesstaats Gujarat wurden Anfang 2010 erstmals Resistenzen des Roten Baumwollkapselwurms gegen Bt-Baumwollsorten der ersten Generation (Bollgard I, seit 2002) beobachtet. Dies könnte auf die mangelhafte Einhaltung von Refugienflächen, oder auch auf den illegalen Anbau von Bt-Sorten mit geringerem Toxingehalt zurückzuführen sein. Für die zweite Generation von Bt-Sorten (Bollgard II, seit 2006), die zwei Bt-Gene enthält, wurden keine Resistenzen festgestellt. Derzeit entwickelt wird Bollgard III, das drei Bt-Gene aufweist. Mehrere voneinander unabhängige Insektizide erschweren die Resistenzbildung.[138]
Der Mechanismus der Resistenzbildung ist wissenschaftlich noch unzureichend geklärt. Im Falle einer unspezifischen Resistenz gegen alle Bt-Toxine müssten Landwirte Bt-Pflanzen und konventionelle Pflanzen abwechselnd verwenden, damit die Resistenz in den Schädlingspopulationen zurückgeht. Falls sich Resistenzen spezifisch gegen einzelne Bt-Toxine entwickeln, könnte eine Bt-Maissorte mit einer anderen der über 200 Cry Proteine genutzt werden. Sorten mit mehreren Cry Proteinen (stacked traits) könnten in diesem Fall möglicherweise ebenfalls helfen.[139][140]
Eine im Juni 2011 veröffentlichte Untersuchung von seit 1996 weltweit aufgetretenen Resistenzen kommt zu dem Schluß, daß eine high-dose/refuge-Strategie, also die Kombination aus Pflanzen, welche eine hohe Dosis bt-Proteine exprimieren, mit Refugien nichtexprimierender Pflanzen die Resistenzbildung erfolgreich verhindern kann. Besondere Bedeutung sollte in einer Fortführung dieser Strategie Pflanzen zukommen, welche mehrere bt-Proteine kombinieren.[141]
Umweltauswirkungen
Umweltschutz
Globale Einsparungen von Pestiziden und Kraftststoffen durch transgene Pflanzen, 1996–2008[142] Pflanze Einsatz von
Pestiziden
(Millionen kg)Umweltbelastung
durch
Pestizide (%)Verbrauch von
Kraftstoff
(Millionen Liter)Herbizidresistente Sojabohne -50,45 -16,6 -835 (USA) /
-1.636 (Argentinien) /
-196 (Rest)Herbizidresistenter Mais -111,58 -8,5 Herbizidresistenter Raps -13,74 -24,3 -347 (Kanada) Herbizidresistente Baumwolle -6,29 -5,5 Bt-Mais -29,89 -29,4 Bt-Baumwolle -140,60 -24,8 -125 Herbizidresistente Zuckerrübe +0,13 -2,0 Gesamt -352,42 -16,3 -3.139 Transgene Pflanzen können den Umweltschutz verbessern, was bereits in Anbauländern nachgewiesen wurde. Durch die Verwendung von transgenen Pflanzen wurde der Einsatz von Pflanzenschutzmitteln im Zeitraum 1996–2008 um geschätzte 352 Millionen kg (8,4 %) reduziert, was einem Rückgang der Umweltbelastung durch Pestizide in diesen Pflanzen um 16,3 % entspricht. Dabei spielte einerseits die Reduktion der ausgebrachten Menge eine Rolle, als auch die Reduktion der Toxizität der ausgebrachten Mittel. Die Reduktion der Emissionen von Treibhausgasen war 2008 equivalent zum Ausstoß von 6,9 Millionen Autos.[142] Die Adoption von herbizidresistenten Pflanzen führte zu einer Reduktion der Toxizität der ausgebrachten Herbizide und einer Ausweitung der pfluglosen Bewirtschaftung, wodurch Bodenerosion, Kraftstoffverbrauch und Treibhausgasemissionen zurückgingen.[143][144] Die Adoption von Bt-Pflanzen führte zu einem starken Rückgang des Insektizideinsatzes, insbesondere dem der giftigsten Substanzen. So wird geschätzt, dass zwischen 1996 und 2008 durch den Einsatz von Bt-Baumwolle 140 Millionen kg an Pestiziden eingespart wurden, was einem Rückgang der Umweltbelastungen durch Pestizidanwendungen bei Baumwolle von knapp 25 % gleichkommt.[142] Ein 2010 veröffentlichtes Review der wissenschaftlichen Literatur ergab, dass die Insektizidanwendungen durch insektenresistente Pflanzen um 14-75 % zurückgingen, und in keinem Fall stiegen. Häufig wurden auch weniger giftige Insektizide und Herbizide ausgebracht, als in konventionellen Feldern.[106]
Durch den geringeren Insektizideinsatz bei Bt-Pflanzen überleben mehr Nichtzielorganismen. Eine Metastudie von 42 Feldexperimenten kommt zu dem Schluss, dass wirbellose Nichtzielorganismen in Bt-Mais und -Baumwollfeldern häufiger vorkommen als in Feldern, die mit Insektiziden behandelt werden (jedoch seltener als in Feldern, die nicht mit Insektiziden behandelt werden).[145]
Zudem kann die Grüne Gentechnik die Sortenvielfalt fördern, da sich einzelne Eigenschaften relativ leicht in lokal angepasste Sorten einbauen lassen. Die konventionelle Züchtung benötigt für einen ähnlichen Prozess mehr Zeit und finanziellen Aufwand. Anstatt lokal angepasste Sorten zu ersetzen, erhöhte sich in den Anbauländern die Zahl der Sorten mit transgenen Eigenschaften schnell.[146]
Längerfristige Beobachtungen von Schädlingspopulationen in den USA und China haben ergeben, dass die Verwendung von Bt-Baumwolle nicht nur zu einem geringeren Schädlingsbefall in den Bt-Feldern, sondern auch zu einem geringeren Schädlingsbefall in konventionellen Baumwoll- und anderen Nutzpflanzenfeldern geführt hat (Positive Externalität).[144] US-amerikanische Maisbauern, die keinen Bt-Mais anbauten, haben auf diese Weise massiv vom Anbau des Bt-Mais durch andere Bauern profitiert.[147]
Umweltrisiken
Umweltorganisationen vertreten die Position, dass beim Anbau von transgenen Pflanzen verschiedene Umweltrisiken bestehen. Sie gehen davon aus
- dass neben den Zielinsekten auch weitere Organismen durch Bt-Toxine geschädigt werden können,
- dass ein Anbau von transgenen Pflanzen durch Auskreuzungen auf wilde Artverwandte die Biodiversität verringern könnte.
2010 veröffentlichte die Europäische Kommission ein Kompendium, in dem sie die Ergebnisse von EU-finanzierten Studien durch über 400 unabhängige Arbeitsgruppen aus dem Zeitraum 2001–2010 zusammentrug.[148] Seit über 25 Jahren Forschung gibt es bisher keine wissenschaftlichen Hinweise dafür, dass gentechnisch veränderte Pflanzen mit höheren Risiken für die Umwelt verbunden seien als konventionelle.[149] Ein 2007 veröffentlichtes Review von wissenschaftlicher Literatur und Studien internationaler Organisationen aus 10 Jahren kam zu dem Schluss, dass bisher keine wissenschaftlichen Beweise für Umweltschäden durch die bisher kommerzialisierten transgenen Pflanzen existierten.[150] Vor der Zulassung einer neuen transgenen Sorte zum Anbau sind umfangreiche Sicherheitsstudien erforderlich, die in der Regel mehrere Jahre dauern. Eine neue Sorte darf nur dann zugelassen werden, wenn eine Unbedenklichkeit für die Umwelt bestätigt wurde. Nach dem Beginn des kommerziellen Anbaus einer neuen Sorte ist in der EU zudem ein anbaubegleitendes Monitoring vorgesehen.[151]
Nichtzielorganismen
Das Bt-Toxin Cry1Ab ist für einige Arten der Ordnung Schmetterlinge giftig. Anders als der Maiszünsler ernähren sich nur sehr wenige Schmetterlingsarten von Mais, könnten aber theoretisch indirekt über Bt-Maispollen geschädigt werden, die auf ihrer Nahrung landen. Eine 1999 veröffentlichte Laborstudie stellte eine Schädigung von Monarchfaltern fest, wenn sie mit Bt-Maispollen des Events 11 gefüttert wurden.[152] Daraus wurden in der Öffentlichkeit Befürchtungen abgeleitet, der Anbau von Bt-Mais könnte Populationen des Monarchfalters reduzieren. Wissenschaftler hingegen betonten, dass das Fütterungsexperiment diese Befürchtungen nicht rechtfertige. Weitere Laborexperimente fanden, dass Pollen des Events 176 Monarchfalterlarven schädigen, woraufhin das Event vom Markt genommen wurde. Feldstudien hingegen fanden keine Effekte auf Larven durch die verbreiteten Bt-Maisevents (MON810 und Bt 11), die 80mal weniger Toxin produzieren als Event 176. Feldstudien zeigten zudem, dass die in den Laborstudien verwendeten Pollenmengen unter Feldbedingungen unrealistisch hoch seien, und suggerierten, dass die Pollen von Event 11 möglicherweise mit anderen Pflanzenteilen vermischt wurde. Für die derzeit zugelassenen Events seien extrem hohe Pollendichten notwendig, um eine Schädigung von Larven zu erreichen. Zudem fanden Felduntersuchungen, dass nur ein geringer Anteil von 0,8 % der Monarchfalterpopulation Bt-Maispollen ausgesetzt sei. Die natürlich Mortalität von 80 % während der Larvenphase müsse zudem berücksichtigt werden, ebenso wie andere Faktoren, wie Verluste durch Habitatzerstörung, Einsatz von Insektiziden sowie Kollisionen mit Autos.[150] Eine 2010 veröffentlichte Simulation suggeriert, dass selbst unter pessimistischen Annahmen ein flächendeckender Anbau von Bt-Mais in Europa kaum negative Effekte auf Schmetterlingsarten hätte. In allen Regionen war die maximale errechnete Sterblichkeitsrate bei Tagpfauenauge und Admiral weniger als einer von 1572 Schmetterlingen, bei der Kohlmotte eine von 392. Im Mittel aller Regionen lag sie für Tagpfauenauge und Admiral bei einem von 5000, für die Kohlmotte bei einer auf 4367.[153].[154]
Zudem wurden die Auswirkungen auf Nützlinge wie natürliche Feinde und Bestäuber untersucht. Bt-Mais gilt als unbedenklich für Honigbienen.[150][155][156] In Labor- und Gewächshausstudien waren natürliche Feinde wie Florfliegen lediglich dann negativ betroffen, wenn ihre Beute durch Bt-Toxine geschädigt wird. Feldstudien zeigten, dass natürliche Feinde aufgrund der geringeren Beuteverfügbarkeit in Bt-Feldern seltener vorhanden waren, diese Reduktion jedoch keine Auswirkungen auf die Population habe. Florfliegen und andere natürliche Feinde sind polyphag, und daher von der Reduktion bestimmter Beutearten nicht stark betroffen.[150] Zudem würden auch andere Instrumente der Schädlingsbekämpfung das Nahrungsangebot von natürlichen Feinden beeinflussen, und die meisten gegenwärtig genutzten Insektizide (vor allem Breitbandinsektizide wie Pyrethroide und Organophosphate) hätten stärkere negative Auswirkungen auf natürliche Feinde als Bt-Toxine. Bei zahlreichen Untersuchungen konnten keine negativen Effekte von Bt-Pflanzen auf Bodenmakroorganismen (Fadenwürmer, Springschwänze, Landasseln, Milben und Regenwürmer) festgestellt werden.[150][157][158]
Biodiversität
In Mexiko ist der Anbau von transgenem Mais seit 1998 verboten, um Landrassen und wilde Verwandte vor möglichen Auskreuzungen zu schützen. Nach Zeitungsberichten widersetzen sich mexikanische Bauern jedoch diesem Verbot und bauen Bt-Mais an. 2001 veröffentlichte Nature eine kontroverse Studie, die über einen Fund von Transgenen in mexikanischen Mais-Landrassen berichtete. Nature zog die Veröffentlichung wenige Monate später zurück, da „die Datenlage die Veröffentlichung nicht rechtfertige“.[159] Eine 2009 veröffentlichte Studie fand in 1 % von über 100 untersuchten Feldern in Mexiko Bt-Gene in Mais-Landrassen. Dabei ist unklar, ob eine gentechnische Einbringung des Bt-Gens in Landrassen illegalerweise vorgenommen wurden, oder ob die Gene von regulären, illegal angebauten Bt-Maissorten unbeabsichtigt ausgekreuzt wurden.[160] Nach einer Verknappung des Maisangebots Anfang 2007 forderte der mexikanische Bauernverband die Zulassung von transgenem Mais für den Anbau.[161] Im Oktober 2009 wurden zwei Genehmigungen für den Versuchsanbau von transgenem Mais auf knapp 13 ha erteilt. Thema der Untersuchungen ist unter anderem die Frage, ob Mexiko mit transgenen Sorten seine Abhängigkeit von Importen verringern kann.[162] Fast 2000 Wissenschaftler protestierten in einer Petition gegen die Genehmigungen, da ihrer Ansicht nach Auskreuzungen auf Landrassen nicht verhindert werden können.[163] Die Zulassungsbehörden hingegen betonen, dass ein Abstand von 500 m zu konventionellen Feldern eingehalten wird. Zudem soll die Aussaat zu unterschiedlichen Zeitpunkten stattfinden, und umliegende Bauern bezüglich möglicher Auskreuzung befragt werden.[163] Es gibt bisher keine wissenschaftlichen Hinweise dafür, dass eine mögliche Auskreuzung von Transgenen die Biodiversität des Mais verringern könnte. Der Genfluss, der Austausch von Genen zwischen Kultur- und Wildsorten, ist ein natürlicher Vorgang. Ob sich Gene aus konventionellen Hochleistungssorten oder transgenen Sorten in Landsorten dauerhaft etablieren und dadurch die Biodiversität verringern, hängt letztlich davon ab, ob sie den Nachkommen einen Selektionsvorteil verleihen. Laut dem internationalen Mais- und Weizenforschungsinstitut nimmt die Vielzahl der Maisrassen in Mexiko allein durch Einkreuzungen aus Kultursorten nicht ab.[164]
Gesundheitliche Auswirkungen
Gesundheitsschutz
Durch die verminderte Anwendung von Pflanzenschutzmitteln hat sich bei transgenen Pflanzen der ersten Generation die Zahl der Vergiftungsfälle durch direkten Kontakt mit Pestiziden reduziert. Dieser Effekt ist besonders stark in Ländern wie China, Südafrika und Indien, wo Pestizide häufig mit Gartenspritzen ausgebracht werden.[165][166][167]
Auch kann die Grüne Gentechnik die Lebensmittelqualität erhöhen. So wurden für Bt-Mais signifikant geringere Spuren von Mykotoxinen gefunden, was auf die verbesserte Schädlingskontrolle zurückzuführen ist.[168]
Mithilfe der Grünen Gentechnik kann der Gehalt von Allergenen in Nahrungsmitteln vermindert werden, was bereits für Tomaten und Erdnüsse ohne Ertragseinbußen möglich ist.[169]
Mangelernährung
Ernährungsphysiologisch verbesserte Pflanzen können die Gesundheit von Konsumenten erhöhen.[170][171] So wird geschätzt, dass der goldene Reis die Kosten der Vitamin A-Versorgung in Indien um 60 % senken würde.[172] Übersetzt man eine gesteigerte Gesundheit in Arbeitsproduktivität, wird ein globaler Wohlfahrtszuwachs von 15 Milliarden US$ pro Jahr geschätzt, das meiste davon in Asien. In China würde der goldene Reis einen Wachstumseffekt von schätzungsweise 2 % bedeuten.[173] Auch für transgene Pflanzen mit erhöhtem Gehalt an Nährstoffen wie Eisen oder Zink, sowie erhöhtem Gehalt an essentiellen Aminosäuren, werden positive ökonomische und gesundheitliche Effekte erwartet.[174]
Gesundheitsrisiken
Verbraucherorganisationen befürchten, dass transgene Pflanzen Gesundheitsrisiken bergen, wie zum Beispiel ein verminderter Nährstoffgehalt oder ein erhöhter Toxingehalt. Transgene Pflanzen könnten bisher unbekannte Allergene produzieren, oder den Gehalt von bekannten Allergenen verändern. Auch könnte der Einsatz von Antibiotika-Resistenzgenen als Marker Antibiotikaresistenzen bei pathogenen Bakterien nach sich ziehen.[87]
Während der Erforschung möglicher Transgene für die Kartoffelzüchtung Ende der 90er Jahre führte der britische Forscher Árpád Pusztai Fütterungsversuche durch. Es sollte getestet werden, ob transgene Kartoffeln, die Lektin bilden, ein mögliches Gesundheitsrisiko darstellten. Lektin ist ein gegen Schadinsekten wirksames Protein aus Schneeglöckchen, das für den Menschen als unbedenklich angesehen wird. Pusztai erklärte, dass die mit den transgenen Kartoffeln gefütterten Ratten weniger gesund seien als die übrigen Versuchstiere. Dies löste eine Kontroverse unter Wissenschaftlern aus. Dabei wurde die statistische Signifikanz der Ergebnisse infrage gestellt, auf mögliche Fehler im Versuch hingewiesen, und die Erklärung der Ergebnisse in anderen Faktoren als dem Gentransfer vermutet. Pusztai blieb in der Folge bei seiner Interpretation, dass der Gentransfer zur Produktion neuer Toxine geführt hätte.[175][176]
Es ist kein Fall einer Einbringung eines Allergens in zugelassene transgene Pflanzen bekannt. In der Entwicklungsphase einer transgenen Sojabohne mit erhöhtem Methioningehalt stellte der Hersteller Pioneer Hi-Bred im Jahr 1996 jedoch fest, dass es sich bei dem aus der Paranuss eingebrachten Gen um das bis dato nicht identifizierte Hauptallergen der Paranuss handelte. Die Produktentwicklung wurde daraufhin abgebrochen.[177]
Laut Wissenschaftlern sei es extrem unwahrscheinlich, dass sich die in der Grünen Gentechnik als Marker verwendeten Antibiotika-Resistenzgene auf Krankheitserreger des Menschen übertragen könnten, da ein entsprechendes Resistenzgen erstens im Verdauungstrakt nicht zersetzt werden dürfe, zweitens in Kontakt mit einem körpereigenen Bakterium kommen müsse, ohne von dessen Restriktionsenzymen zerschnitten zu werden, und drittens sich mit dem Bakterienchromosom rekombinieren müsse, und zwar an einer ganz bestimmten Stelle und auf eine ganz bestimmte Weise. Viertens müsse das körpereigene Bakterium dann noch das Antibiotika-Resistenzgen auf ein krankheitserregendes Bakterium übertragen. Jeder einzelne dieser Schritte sei für sich genommen schon sehr unwahrscheinlich, die Wahrscheinlichkeit des Zusammentreffens aller Schritte extrem gering.[178][179][180] Um selbst dieses minimale Risiko auszuschalten, setzt die Grüne Gentechnik Antibiotika-Resistenzgene nicht mehr als Marker ein.[181]
Ähnlich gering sei das Risiko des Einsatzes von Promotoren. Promotoren müssen verwendet werden, um ein Gen zu aktivieren. So wird ein Promotor eines Blumenkohlvirus verwendet, um das Bt-Gen zu aktivieren. Dieser Promotor funktioniert jedoch nur in Pflanzen, Hefe und Bakterien, und wird in menschlichen Zellen nicht exprimiert. Da Menschen seit Jahrtausenden Viren und Bakterien sowie Blumenkohl zu sich nehmen, ohne dass deren Promotoren einen negativen Einfluss gehabt hätten, seien die Bedenken fehl am Platz.[178] Um dennoch das geringste Risiko auszuschalten, würden ab der zweiten Generation nur noch artenspezifische Promotoren verwendet.[181]
Wissenschaftler erklären zudem, die Gentechnik sei nicht so künstlich oder unpräzise wie oft angenommen. Es würden Verfahren genutzt, die auch in der Natur vorkommen und diese würden ständig verbessert.[182][183] Auch die Eigenschaften der Zielgene seien sehr genau bekannt und die resultierenden Pflanzen würden strenger überwacht als die konventionell erzeugten, und Sorten, die nicht die gewünschten oder gar negative Eigenschaften besitzen, würden nicht weiterentwickelt.[184][185] Bis 2007 gab es weltweit über 270 Studien zur Sicherheit von GVO.[186] Für die Überwachung zuständige Behörden belegen mit umfangreichen Untersuchungen die Umweltsicherheit und Politiker wie Bundesforschungsministerin Schavan oder Forscher wie die Nobelpreisträgerin Christiane Nüsslein-Volhard vertreten die Ansicht, dass es nach 20 Jahren Forschung keine wissenschaftlichen Hinweise für eine Gefährdung durch die Gentechnik gäbe.[187][188][189]
Ein 2001 veröffentlichtes Review der Europäischen Kommission von 81 Studien aus 15 Jahren fand keine Hinweise auf Gesundheitsrisiken durch transgene Pflanzen.[190] 2010 veröffentlichte die Europäische Kommission erneut ein Kompendium, in dem sie die Ergebnisse von EU-finanzierten Studien durch über 400 unabhängige Arbeitsgruppen aus dem Zeitraum 2001–2010 zusammentrug.[148] Seit über 25 Jahren Forschung gibt es keine wissenschaftlichen Hinweise dafür, dass gentechnisch veränderte Pflanzen mit höheren Risiken für die menschliche Gesundheit verbunden seien als konventionelle.[149] Die FAO, WHO, OECD, sowie deutsche, französische und britische Wissenschaftsakademien und die US-amerikanische FDA kamen zum selben Ergebnis. Zukünftige Gesundheitsschäden vollständig auszuschließen, sei wissenschaftlich unmöglich. Kritiker fordern häufig einen „Beweis“ der Sicherheit. Dies ist laut Befürwortern jedoch unverhältnismäßg, nach einem derart strengen Standard dürfte keine Technologie zugelassen werden, weder neue noch existierende.[190][191]
Ethische Aspekte
In der von den Anthroposophen begründeten biologisch-dynamischen Landwirtschaft wird das Ziel verfolgt, die Pflanze „wesensgemäß“ zu züchten. Dies schließt nicht nur Kreuzungen von Weizen und Dinkel aus, sondern auch jede Anwendung der Gentechnik.
Laut Joachim von Braun ist es im Kampf gegen den Welthunger ethisch erforderlich, die grüne Gentechnik Bauern in Entwicklungsländern zur Verfügung zu stellen.
Der Nuffield Council on Bioethics kam in Bezug auf eine möglicherweise unethische Unnatürlichkeit von transgenen Pflanzen zu dem Schluss, dass der Unterschied zur konventionellen Züchtung nicht groß genug sei, um eine inhärente moralische Fragwürdigkeit der Grünen Gentechnik festzustellen. Im Bezug auf das Vorsorgeprinzip sei es angebracht, die Risiken des Status quo zu berücksichtigen. Da der Status quo erheblichen Schaden unter Hungernden und Armen anrichte und die Grüne Gentechnik Chancen biete, diesen Schaden zu verringern, sei eine Einschränkung der Grünen Gentechnik nicht unbedingt konsistent mit dem Vorsorgeprinzip.
Rezeption in der Öffentlichkeit
Im Gegensatz zur Roten Biotechnologie trifft die Grüne Gentechnik insbesondere in der Öffentlichkeit von Industriestaaten auf Ablehnung. Umweltschutzorganisationen wie Greenpeace oder Friends of the Earth verstehen sich als grundsätzlichen Gegner der Technik. Verbände der ökologischen Landwirtschaft treten für eine gentechnikfreie Landwirtschaft ein. Auch einige politische Parteien äußern Vorbehalte. In Deutschland lehnen beispielsweise Bündnis 90/Die Grünen und die Linke den Anbau von transgenen Nahrungsmittelpflanzen ab. Der Protest gegen gentechnisch veränderte Pflanzen kommt unter anderem in sogenannten Feldbefreiungen zum Ausdruck, wobei entsprechende Anbaugebiete rechtswidrig von Umweltaktivisten besetzt oder beschädigt werden.
In einer Meinungsumfrage von 2000 in 35 Ländern wurden 35.000 Menschen gefragt, ob die Vorteile von transgenen Nahrungspflanzen größer als die Risiken seien. Transgene Nahrungspflanzen fanden wenig Zustimmung bei Bürgern reicher Nationen wie Japan und Frankreich mit nur 22 %. In Indien und China lag die Zustimmung mit über 65 % deutlich höher, am höchsten war sie in Kuba und Indonesien mit etwa 80 %.[192] Einer 2006 durchgeführten Befragung von Menschen, die sich der Existenz GVO bewusst waren, zufolge glaubten 89 % der Griechen, dass GVO schädlich seien, hingegen nur 33 % der Südafrikaner.[190] Umfragen (2001, 2003) ergaben, dass in den USA die Akzeptanz von Gv-Lebensmitteln geringer ist bei Menschen über 64, Frauen und niedrigem Bildungsabschluss. Ablehnung von gentechnisch veränderten Lebensmitteln ist positiv korreliert mit vegetarischer/veganer Ernährungsweise. Die Akzeptanz von Gv-Lebensmitteln ist etwas geringer bei Menschen, die kaum verarbeitete Lebensmittel ohne künstliche Farb- und Geschmacksstoffe, aus ökologischer und lokaler Erzeugung sowie kalorien-, fett- cholesterin-, zucker- und salzarme Lebensmittel bevorzugen. Die Ablehnung von Gv-Lebensmittln ist am geringsten bei Menschen mit postgradualen Abschlüssen. 94 % der Amerikaner sprachen sich 2003 sich für eine Kennzeichnung von Gv-Lebensmitteln aus.[193] Dem Eurobarometer 1999 zufolge nahm die Ablehnung von gv-Lebensmitteln in allen 16 europäischen Ländern gegenüber 1996 zu. Am stärksten war die Ablehnung 1999 in Griechenland (81 %), am schwächsten in den Niederlanden (25 %). Gegenüber gv-Pflanzen war die Zustimmung in Portugal und Spanien am höchsten und in Norwegen, Luxemburg und Österreich am geringsten. Gegner von gv-Lebensmitteln gaben zu über 80 % an, Gv-Lebensmittel gefährdeten die „natürliche Ordnung“, seien „fundamental unnatürlich“, mit „unakzeptablen Risiken“ und „Gefahren für zukünftige Generationen“ verbunden.[194] Laut dem Eurobarometer 2010 ist die Bevölkerung in allen EU-Ländern gegenüber gentechnisch veränderten Lebensmitteln überwiegend negativ eingestellt. Mit wenigen Ausnahmen hat die Ablehnung in den letzten Jahren zugenommen. Als wichtigste Gründe, Gv-Lebensmittel abzulehnen, werden angeführt, sie seien „nicht sicher“ und „unnatürlich“.[195][196]
Einige Wissenschaftler sehen eine Teilerklärung für diese Auffassung, dass gentechnisch veränderte Lebensmittel ein Gesundheitsrisiko darstellen, in einem Mangel an Wissen über die Grüne Gentechnik.[178] Umfragen Ende der 90er Jahre ergaben, dass 35 % der EU-Bürger und 65 % der US-Amerikaner glaubten, dass nicht-transgene Tomaten keine Gene enthielten.[197] Eine andere Umfrage zeigte, dass ein Viertel der Europäer glaubte, dass der Verzehr einer transgenen Pflanze eine Veränderung der menschlichen Gene nach sich ziehen könne.[198] Die Ablehnung der Grünen Gentechnik in reicheren Ländern sei deswegen stärker, weil sich aus der ersten Generation gentechnisch veränderter Pflanzen hauptsächlich Nutzen für Landwirte in Entwicklungsländern, aber kaum Vorteile für reiche Konsumenten ergeben würden.[199][190]
Seitens der Wissenschaft wird die Vorgehensweise der Kritiker selbst kritisiert. So kommt die Union der deutschen Akademien der Wissenschaften zu dem Schluss, Kampagnen gegen die Grüne Gentechnik mangele es an wissenschaftlicher Grundlage.[200]
2009 gab es eine «Gemeinsame Erklärung der Wissenschaftsorganisationen zur Grünen Gentechnik»[201] (eine Erklärung der Allianz der Wissenschaftsorganisationen) und eine «Stellungnahme der Deutschen Akademie der Naturforscher Leopoldina»,[202] in denen von der Politik gefordert wurde, für eine Versachlichung der Diskussion einzutreten und verlässliche Rahmenbedingungen für die Forschung zu schaffen. Eine von der Päpstlichen Akademie der Wissenschaften im Mai 2009 einberufene Expertenrunde hält es für einen moralischen Imperativ, den Nutzen der Grünen Gentechnik einer größeren Zahl von Armen zugänglich zu machen, und erinnert die Gegner an den Schaden, die ein Vorenthalten der Technologien für die Bedürftigsten bedeute.[86] (der Vatikan erklärte, das Abschlussdokument dürfe nicht als Erklärung der päpstlichen Akademie der Wissenschaften oder des Vatikans verstanden werden und er distanzierte sich von der Befürwortung des Anbaus gentechnisch veränderter Nutzpflanzen durch die Expertenrunde.[203])
Der Bund für Lebensmittelrecht und Lebensmittelkunde stellte in einem Positionspapier fest, dass bereits heute Lebensmittel mit gentechnisch veränderten Inhaltsstoffen in deutschen Supermärkten weit verbreitet seien. Schätzungen zufolge seien 60 % bis 70 % aller Lebensmittel in ihrer Produktion mit Gentechnik in irgendeiner Weise in Kontakt gekommen.[204]
Literatur
- Deutsche Forschungsgemeinschaft: Grüne Gentechnik (Informationsbroschüre, 2009).
- Nina Fedoroff & Nancy Brown: Mendel in the Kitchen. John Henry Press: Washington, D.C. 2004.
- Frank Kempken: Mit Grüner Gentechnik gegen den Hunger?, in APuZ 6-7/2009, S. 21–26.
- Peggy G. Lemaux: Genetically Engineered Plants and Foods: A Scientist's Analysis of the Issues (Part I). Annual Review of Plant Biology. Band 59, S. 771-812, 2008.
- Peggy G. Lemaux: Genetically Engineered Plants and Foods: A Scientist's Analysis of the Issues (Part II). Annual Review of Plant Biology. Band 60, S. 511-59, 2009.
- Ingo Potrykus & Klaus Ammann (Hg.): Transgenic plants for food security in the context of development – proceedings of a study week of the pontifical academy of sciences. New Biotechnology, Volume 27, Nr. 5, November 2010.
- Matin Qaim: The Economics of Genetically Modified Crops. Annual Review of Resource Economics, Vol. 1, S. 665-694, 2009.
Weblinks
Einzelnachweise
- ↑ Frank Kempken, Renate Kempken: Gentechnik bei Pflanzen, 2. Auflage, 2003, S. 83. ISBN 3-540-01216-8.
- ↑ ADDIN EN.REFLIST Frame, B. R., H. X. Shou, et al. (2002). „Agrobacterium tumefaciens-mediated transformation of maize embryos using a standard binary vector system.“ Plant Physiology 129(1): 13-22.
- ↑ a b c d e f Frank Kempken, Renate Kempken: Gentechnik bei Pflanzen, 3. Auflage, 2006, S. 83-91, ISBN 3-540-33661-3
- ↑ Frame, B. R., H. X. Shou, et al. (2002). „Agrobacterium tumefaciens-mediated transformation of maize embryos using a standard binary vector system.“ Plant Physiology 129(1): 13-22.
- ↑ Sidorov, V., L. Gilbertson, et al. (2006). „Agrobacterium-mediated transformation of seedling-derived maize callus.“ Plant Cell Reports 25(4): 320-328.
- ↑ James, D. J., S. Uratsu, et al. (1993). „ACETOSYRINGONE AND OSMOPROTECTANTS LIKE BETAINE OR PROLINE SYNERGISTICALLY ENHANCE AGROBACTERIUM-MEDIATED TRANSFORMATION OF APPLE.“ Plant Cell Reports 12(10): 559-563.
- ↑ Frame, B. R., H. Y. Zhang, et al. (2000). „Production of transgenic maize from bombarded type II callus: Effect of gold particle size and callus morphology on transformation efficiency.“ In Vitro Cellular & Developmental Biology-Plant 36(1): 21-29.
- ↑ Brettschneider, R., D. Becker, et al. (1997). „Efficient transformation of scutellar tissue of immature maize embryos.“ Theoretical and Applied Genetics 94(6-7): 737-748.
- ↑ a b c nature.com: International trade and the global pipeline of new GM crops (englisch)
- ↑ Agricultural Biotechnology – Overview and Opportunities
- ↑ Hahlbrock, S. 162 ff.
- ↑ Globale Anbauflächen 2009
- ↑ Pressemeldung BASF vom 30. Januar 2009: BASF and Embrapa’s biotech soybeans on track for Brazilian market launch from 2011 onward (englisch)
- ↑ BASF and Embrapa’s Cultivance®soybeans receive approval for commercial cultivation in Brazil (englisch)
- ↑ a b European Commission, Joint Research Centre, Institute for Prospective Technological Studies The global pipeline of new GM crops: implications of asynchronous approval for international trade (englisch)
- ↑ A new generation of insect resistant GM crops: transgenic wheat synthesising the aphid alarm signal. Rothamsted Reserach.
- ↑ Website zum BOKU-Projekt „Trangenes Steinobst“
- ↑ Gunjan Sinha (2007): GM Technology Develops in the Developing World. Science 315 (5809), S. 182-183.
- ↑ Jeff Tollefson (2011): Brazil cooks up transgenic bean. Nature 478: 138.
- ↑ Kraut- und Knollenfäule bei Kartoffeln
- ↑ S. L. Lv u. a.: Overexpression of Thellungiella halophila H+-PPase (TsVP) in cotton enhances drought stress resistance of plants. In: Planta. 2009, Band 229, S. 899–910.
- ↑ Monsanto: Yield Stress Update (PDF, englisch)
- ↑ H.-X. Zhang u. a.: Engineering salt-tolerant Brassica plants: characterization of yield and seed oil quality in transgenic plants with increased vacuolar sodium accumulation. In: Proceedings of the National Academy of Sciences USA. 2001, Band 98, S. 12832–12836.
- ↑ V. M. Anoop u. a.: Modulation of citrate metabolism alters aluminum tolerance in yeast and transgenic canola overexpressing a mitochondrial citrate synthase. In: Plant Physiology. 2003, Band 132, S. 2205–2217.
- ↑ Salt-tolerant rice offers hope for global food supply. ACPFG, 10. September 2010.
- ↑ Ausgereift – und dennoch länger haltbar
- ↑ G. Drakakaki u. a.: Endosperm-specific co-expression of recombinant soybean ferritin and Aspergillus phytase in maize results in significant increases in the levels of bioavailable iron. In: Plant Molecular Biology. 2005, Band 59, S. 869–880.
- ↑ J. Yu u. a.: Seed-specific expression of the lysine-rich protein gene sb401 significantly increases both lysine and total protein content in maize seeds. In: Food and nutrition bulletin. 2005, Band 26, S. 427–431.
- ↑ Transgenic Indian superspuds pack more protein, 20. September 2010.
- ↑ E. M. Herman u. a.: Genetic Modification Removes an Immunodominant Allergen from Soybean. In: Plant Physiology. 2003, Band 132, S. 36–43.
- ↑ P. L. Bhalla u. a.: Antisense-mediated silencing of a gene encoding a major ryegrass pollen allergen. In: Proceedings of the National Academy of Sciences U. S. A. 2008, Band 96, S. 11676–11680.
- ↑ S. E. Sattler u. a.: From Arabidopsis to agriculture: engineering improved Vitamin E content in soybean. In: Trends in Plant Science. 2004, Band 9, S. 365–367.
- ↑ V. S. Tavva u. a.: Increased alpha-tocopherol content in soybean overexpressing the Perilla frutescens gamma-tocopherol methyltransferase gene. In: Plant Cell Reports. 2007, Band 26, S. 61–70.
- ↑ Waltz, E. (2010): Food firms test fry Pioneer’s trans fat–free soybean oil. Nature Biotechnology. Vol. 28, Nr. 8, S. 769-70.
- ↑ "M. Yusuf und N. B. Sarin: Antioxidant value addition in human diets: genetic transformation of Brassica juncea with gamma-TMT gene for increased alpha-tocopherol content. In: Transgenic Research. 2007, Band 16, S. 109–113.
- ↑ http://ipgb.tamu.edu/keerti-rathore-ph-d/
- ↑ Sunilkumar, g., CAMPBELL, L. M., Puckhaber, L. & Rathore K. S. (2006) Engineering cottonseed for use in human nutrition by tissue-specific reduction of toxic gossypol. Proceedings of the National Academy of Sciences, USA 103: 18054-18059
- ↑ G. Sunilkumar u. a.: Engineering cottonseed for use in human nutrition by tissue-specific reduction of toxic gossypol. In: Proceedings of the National Academy of Sciences USA. 2006, 26, Band 103, S. 18054–18059.
- ↑ goldenrice.org: History of the Golden Rice Programme (englisch)
- ↑ goldenrice.org: A Public-Private Partnership and Humanitarian Licences (englisch)
- ↑ High iron and zinc rice gives hope to micronutrient deficient billions. 8. September 2011.
- ↑ E. E. Hood u. a.: Molecular farming of industrial proteins from transgenic maize. In: Advances in experimental medicine and biology. 1999, Band 464, S. 127–147.
- ↑ C. S. Farinas u. a.: Aqueous extraction of recombinant human proinsulin from transgenic maize endosperm. In: Biotechnology Progress. 2005, Band 21, S. 1466–1471.
- ↑ a b H. Daniell u. a.: Medical molecular farming: production of antibodies, biopharmaceuticals and edible vaccines in plants. In: Trends in Plant Science. 2001, Band 6, S. 219–226.
- ↑ G. Giddings u. a.: Transgenic plants as factories for biopharmaceuticals. In: Nature Biotechnology. 2000, Band 18, S. 1151–1155.
- ↑ J. A. Howard u. a.: Commercialization of plant-based vaccines from research and development to manufacturing. In: Animal Health Research Reviews. 2004, Band 5, S. 243–245.
- ↑ J. K. Ma u. a.: Characterization of a recombinant plant monoclonal secretory antibody and preventive immunotherapy in humans. In: Nature Medicine. 1998, Band 4, S. 601–606.
- ↑ E. Stoger u. a.: Recent progress in plantibody technology. In: Current pharmaceutical design. 2005, Band 11, S. 2439–2457.
- ↑ Agrobioinstitute (ABI): Co-existence and socioeconomic aspects (PDF, englisch)
- ↑ Monsanto / BASF: Working Jointly For Higher Yields (PDF, englisch)
- ↑ Bayer, Evogene: Bayer CropScience und Evogene weiten Zusammenarbeit zur Verbesserung von Erträgen bei Reis aus
- ↑ International Seed Federation: Seed Statistics („Value of the Domestic Market for Seed in Selected Countries“; PDF, englisch)
- ↑ Monsanto – Fiscal Year 2010: Total Seeds and Genomics (englisch)
- ↑ DesMoinesRegister.com – Pioneer’s seed sales rose 14 percent, DuPont says (englisch)
- ↑ Syngenta Financial Information – Jahresabschluss 2010: Seeds [1] (PDF)
- ↑ Limagrain Fact Sheet M€ 971 (Saatgut, 72 % von M€ 1349) [2] (PDF)
- ↑ KWS SAAT Reports and presentations: Seite 62 M€ 731 (External sales sugarbeet, corn, cereals) [3] (PDF, englisch)
- ↑ Bayer CropScience Key figures „BioScience“, M€ 503 (englisch)
- ↑ a b James, Clive: Global Status of Commercialized Biotech/GM Crops: 2010. (englisch)
- ↑ FAO Statistical Yearbook 2010
- ↑ Statistische Ämter des Bundes und der Länder: Flächennutzung
- ↑ FAO: FAOSTAT: Resources: ResourceSTAT: Land: Arable Land (Updated: 9. September 2010) [4]
- ↑ a b c d e Ramessar, K., Capell, T., Twyman, R., Quemada, H., Christou, P. (2009): Calling the tunes on transgenic crops: the case for regulatory harmony. Molecular Breeding, Vol. 23, S. 99-112.
- ↑ Freisetzungsrichtlinie gemäß EU-Recht
- ↑ Lebens- und Futtermittel (GVO). Verordnung (EG) Nr. 1829/2003 auf europa.eu
- ↑ Der lange Weg vom Antrag bis zur Entscheidung. Transgen.de, 12. Januar 2010.
- ↑ a b c Empfehlung 2003/556/EG der Kommission vom 23. Juli 2003 mit Leitlinien für die Erarbeitung einzelstaatlicher Strategien und geeigneter Verfahren für die Koexistenz gentechnisch veränderter, konventioneller und ökologischer Kulturen. Bekannt gegeben unter Aktenzeichen K(2003) 2624, ABl. Nr. L 189 vom 29. Juli 2003 (Webdokument. In: umwelt-online.de. Abgerufen am 28. Oktober 2010.
Aufgehoben mit Leitlinien für die Entwicklung nationaler Koexistenz-Maßnahmen zur Vermeidung des unbeabsichtigten Vorhandenseins von GVO in konventionellen und ökologischen Kulturpflanzen. Empfehlung der Kommission vom 13. Juli 2010 2010/C 200/01 (pdf, bmg.gv.at), cf. Bericht der Kommission an den Rat und das Europäische Parlament über die Koexistenz gentechnisch veränderter, konventioneller und ökologischer Kulturen. {SEK(2009) 408 KOM/2009/0153 endg. CELEX:52009DC0153 (pdf, eur-lex) - ↑ Leitlinien der EU. In: →Umweltsituation →Gentechnik →Koexistenz →Leitlinien der EU. Umweltbundesamt, abgerufen am 30. Oktober 2010.
- ↑ Nicht kennzeichnungspflichtig. Transgen.de, 10. Januar 2007.
- ↑ Ohne Gentechnik – was ist erlaubt? Transgen.de, 14. September 2010.
- ↑ Saatgut: Grundsatzkonflikt um Schwellenwert. Transgen.de.
- ↑ EU: Entscheidung über Gentechnik-Spuren in Futtermittelimporten erneut verschoben. Transgen.de, 9. Februar 2011.
- ↑ Ergebnisse von bundesweitem GVO-Saatgut-Monitoring liegen vor. um.baden-wuerttemberg.de
- ↑ a b c d Ramessar, K., Capell, T., Twyman, R., Christou, P. (2010): Going to ridiculous lengths- European coexistance regulations for GM crops. In: Nature Biotechnology Vol. 28, Nr. 2, Februar 2010 (pdf).
- ↑ Vorschlag für eine VERORDNUNG DES EUROPÄISCHEN PARLAMENTS – PDF-Dolument
- ↑ Nationale „Selbstbestimmung“ bei gentechnisch veränderten Pflanzen: Schon gescheitert? Transgen.de, 27. September 2009.
- ↑ Gutachten: EU-Pläne für nationalen Gentechnik-Anbau verstoßen gegen WTO. Transgen.de, 9. November 2010.
- ↑ Gentechnik-Anbau: Ministerrat schiebt nationale Verbote auf die lange Bank. Transgen.de, 12. Dezember 2010.
- ↑ US Department of Agriculture. GAIN Report: EU-27 Biotechnology. GE Plants and Animals (USDA, Washington, DC, 2009).
- ↑ Johan F.M. Swinnen & Thijs Vandemoortele (2010): Policy Gridlock or Future Change? The Political Economy Dynamics of EU Biotechnology Regulation. AgBioForum, Band 13, Nr. 4.
- ↑ a b c d e Joyce Tait & Guy Barker (2011): Global food security and the governance of modern biotechnologies. EMBO reports 12: 763-768.
- ↑ a b Qaim, M. (2009): The Economics of Genetically Modified Crops. In: Annual Review of Resource Economics Vol. 1, S. 665–694.
- ↑ a b Devos, Y., Demont, M., Dillen, K., Reheul, D., Kaiser, M., Sanvido, O. (2009): Coexistence of Genetically Modified and Non-GM Crops in the European Union: A Review. In: Lichtfouse, E., Navarrete, M., Debaeke, P., Souchère, V., Alberola, C. (Hrsg.): Sustainable Agriculture. Springer, 2009.
- ↑ Maite Sabalza, Bruna Miralpeix, Richard M Twyman, Teresa Capell, Paul Christou (2011): EU legitimizes GM crop exclusion zones. Nature Biotechnology, Band 29, S. 315–317. doi:10.1038/nbt.1840.
- ↑ http://www.oecumene.radiovaticana.org/ted/Articolo.asp?c=443562
- ↑ a b Vatican panel backs GMOs. Nature Biotechnology, Vol. 29, Nr. 1, S. 11.
- ↑ a b c d Consumers International, 2007.
- ↑ Kalaitzandonakes N., Alston, J., Bradford, K.: Compliance costs for regulatory approval of new biotech crops. In: Nature Biotechnology Vol. 25/2007, S. 509–11.
- ↑ Pray, C., Bengali, P., Ramaswami, B. (2005): The cost of biosafety regulations: the Indian experience. In: Quarterly Journal of International Agriculture Vol. 44, S. 267-89.
- ↑ Golan, E., Kuchler, F., Mitchell, L. (2001): Economics of food labeling. In: Journal of Consumer Policy Vol. 24, S. 117–84.
- ↑ Moschini, G. (2008): Biotechnology and the development of food markets: retrospect and prospects. In: European Review of Agricultural Economics Vol. 35, S. 331–55.
- ↑ Coexistence of genetically modified crops with conventional and organic agriculture. Website der Europäischen Kommission. ec.europa.eu.
- ↑ WTO Dispute Settlement: EC — Approval and Marketing of Biotech Products. USA, Kanada, Argentinien, alle wto.org (englisch)
- ↑ EU erlaubt Einfuhr von gentechnisch verändertem T45-Raps. Transgen.de
- ↑ EU and Canada settle WTO case on Genetically Modified Organisms. europa.eu (englisch).
- ↑ Regionale Unterschiede in der Gentechnik-Politik führen zu Problemen im Agrarhandel. Transgen.de.
- ↑ Innovative Landwirte fordern Wahlfreiheit. mz-web.de.
- ↑ Ungelöstes Problem GVO-Nulltoleranz belastet Futtermittelbranche und Veredlung. In: Agrar-Nachrichten, proplanta.de.
- ↑ FAO: Hunger (englisch)
- ↑ Alex Renton (2009): Our culture of wasting food will one day leave us hungry. The guardian. Sunday 8 February 2009.
- ↑ United Nations: World Population Prospects (englisch)
- ↑ FAO: Number of hungry people rises to 963 million (englisch)
- ↑ Financial Times Deutschland: El Niño bedroht Konjunkturerholung
- ↑ von Braun, J. (2007): The world food situation: new driving forces and required actions. Food Policy Report 18. International Food Policy Reserach Institute. Washington, DC.
- ↑ Focus on yield – Biotech crops; evidence, outcomes and impacts 1996–2006 (englisch)
- ↑ a b c d Peer-reviewed surveys indicate positive impact of commercialized GM crops. Nature Biotechnology, Vol. 28, Nr. 4, April 2010. S. 319-21.
- ↑ „Dass ich hier bin, ist ein reines Wunder“ Interview von Rudolf Burger. Tagesanzeiger, 17. März 2009
- ↑ Alston, J., Beddow, J., Pardey, P. (2009): Agricultural Research, Productivity, and Food Prices in the Long Run. Science, Vol. 325, pp. 1209–1210.
- ↑ Evenson, R. & Gollin, D. (2003): Assessing the Impact of the Green Revolution, 1960 to 2000. Science, Vol. 300, Mai 2003, pp. 758-762.
- ↑ Fan, S., Chan-Kang, C., Qian, K., Krishnaiah, K. (2005): National and international agricultural research and rural poverty: the case of rice research in India and China. Agricultural Economics. Vol. 33, pp. 369–79.
- ↑ Hazell, P., Ramasamy, C. (1991): The Green Revolution Reconsidered: The Impact of High-Yielding Rice Varieties in South India. Baltimore, MD: Johns Hopkins University Press.
- ↑ a b FAO (2004): The State of Food and Agriculture 2003-04; Agricultural Biotechnology: Meeting the Needs of the Poor? Rome: FAO.
- ↑ Graff, G., Cullen, S., Bradford, K., Zilberman, D., Bennett, A. (2003): The public-private structure of intellectual property ownership in agricultural biotechnology. Nature Biotechnology, Vol. 21, pp. 989–95.
- ↑ Santaniello, V., Evenson, R., Zilberman, D., Carlson, G. (hrsg.) (2000): Agriculture and Intellectual Property Rights: Economic, Institutional and Implementation Issues in Biotechnology. Oxfordshire, UK: CABI Publishing.
- ↑ Lipton, M. (2001): Reviving global poverty reduction: what role for genetically modified plants? Journal of International Development, Vol. 13, pp. 823–46.
- ↑ Qaim, M., Krattiger, A., von Braun, J. (hrsg.) (2000): Agricultural Biotechnology in Developing Countries: Towards Optimizing the Benefits for the Poor. New York: Kluwer.
- ↑ Interview mit Tewolde Egziabher, 23. Oktober 2002, veröffentlicht von: Greenpeace Redaktion/
- ↑ upenn.edu: Suicide Seeds? Biotechnology Meets the Developmental State (englisch)
- ↑ Drivers of Consolidation in the Seed Industry and its Consequences for Innovation (CGM 2011-01). COGEM, 29. März 2011.
- ↑ card.iastate.edu: Graham Brookes, Tun-Hsiang (Edward) Yu, Simla Tokgoz, Amani Elobeid: The Production and Price Impact of Biotech Crops. Working Paper 10-WP 503, Januar 2010, Volltext (PDF)
- ↑ Zentralverband der Deutschen Schweineproduktion e.V. [5]
- ↑ ISN – Interessengemeinschaft der Schweinehalter Deutschlands [6]
- ↑ Landwirt.com [7]
- ↑ Animal-health-online.de [8]
- ↑ Thüringer Landesanstalt für Landwirtschaft Jena [9]
- ↑ Tabashnik, Bruce E.; Van Rensburg, J.B.J.; Carrière, Yves. Field-Evolved Insect Resistance to Bt Crops: Definition, Theory, and Data. Journal of Economic Entomology, Volume 102, Number 6, December 2009 , pp. 2011–2025(15)
- ↑ agbioforum.org: Herbicide Resistant Crops--Diffusion, Benefits, Pricing, and Resistance Management
- ↑ a b c Monitoring movement of herbicide resistant genes from farm-scale evaluation field sites to populations of wild crop relatives (englisch)
- ↑ Schweizerische Arbeitsgruppe Gentechnologie
- ↑ biosicherheit.de: Gentechnisch veränderter Raps in Kanada: Zehn Jahre Anbau – eine Bilanz
- ↑ a b Powles, S. (2008): Evolved glyphosate-resistant weeds around the world: lessons to be learnt. Pest Management Science, Vol. 64, S. 360-5.
- ↑ Herbicide Resistant Weeds Summary (englisch)
- ↑ Powles SB. Gene amplification delivers glyphosate-resistant weed evolution, Proc Natl Acad Sci U S A. 2010 Jan 19;107(3):955-6
- ↑ a b "Insect resistance to Bt crops: evidence versus theory"in „Nature Biotechnology“ (Bd. 26, S. 199; doi: 10.1038/nbt1382)
- ↑ http://www.isb.vt.edu/news/2008/aug08.pdf Bruce E. Tabashnik, Aaron J. Gassmann, David W. Crowder, Yves Carrière: Field-Evolved Insect Resistance to Transgenic Bt Crops
- ↑ Hurley, T. (2005): Bacillus thuringiensis resistance management: experiences from the USA. In: Wesseler, Justus (ed.): Environmental Costs and Benefits of Transgenic Crops. Springer: Dordrecht, the Netherlands.
- ↑ Bruce E Tabashnik, Mark S Sisterson, Peter C Ellsworth, Timothy J Dennehy, Larry Antilla, Leighton Liesner, Mike Whitlow, Robert T Staten, Jeffrey A Fabrick, Gopalan C Unnithan, Alex J Yelich, Christa Ellers-Kirk, Virginia S Harpold, Xianchun Li, Yves Carrière (2010): Suppressing resistance to Bt cotton with sterile insect releases. Nature Biotechnology, 7. November 2010 (online veröffentlicht).
- ↑ Resistente Schädlinge in Indien nachgewiesen. Trangen, 16. März 2010.
- ↑ Stockstad, E. (2001): First Light on Genetic Roots of Bt Resistance. Science. Vol. 293, August 3, 2001, p.778.
- ↑ Fedoroff, N. & Brown, N. (2004): Mendel in the Kitchen. John Henry Press: Washington, D.C.
- ↑ Success of the high-dose/refuge resistance management strategy after 15 years of Bt crop use in North America (englisch)
- ↑ a b c Brookes, G., & Barfoot, P. (2010). Global impact of biotech crops: Environmental effects, 1996–2008. AgBioForum, 13(1), 76-94.
- ↑ Qaim, M. & Traxler, G. (2005): Roundup Ready soybeans in Argentina: farm level and aggregate welfare effects. Agricultural Economics, Vol. 32, pp. 73–86.
- ↑ a b National Research Council (2010): The Impact of Genetically Engineered Crops on Farm Sustainability in the United States. Washington, D.C.: The National Academies Press.
- ↑ Marvier, M., McCreedy, C., Regetz, J., Kareiva, P. (2007): A Meta-Analysis of Effects of Bt Cotton and Maize on Nontarget Invertebrates. Science. Vol. 316, June 2007, pp. 1475–1477.
- ↑ Qaim, M., Pray, C., Zilberman, D. (2008): Economic and social considerations in the adoption of Bt crops. Kapitel 12 in: Romeis, J., Shelton, A., Kennedy, G. (hrsg.) (2008): Integration of Insect-Resistant Genetically Modified Crops within IPM Programs. New York: Springer.
- ↑ W. D. Hutchison, E. C. Burkness, P. D. Mitchell, R. D. Moon, T. W. Leslie, S. J. Fleischer, M. Abrahamson, K. L. Hamilton, K. L. Steffey, M. E. Gray, R. L. Hellmich, L. V. Kaster, T. E. Hunt, R. J. Wright, K. Pecinovsky, T. L. Rabaey, B. R. Flood, E. S. Raun, (2010): Areawide Suppression of European Corn Borer with Bt Maize Reaps Savings to Non-Bt Maize Growers. Science, 8. Oktober 2010.
- ↑ a b Europäische Kommission (2010): A decade of EU-funded GMO research (2001–2010).
- ↑ a b Kommission veröffentlicht Sammlung von Ergebnissen EU-unterstützter Forschung über genetisch veränderte Nutzpflanzen. 9. Dezember 2010
- ↑ a b c d e Sanvido O., Romeis J., Bigler F.(2007): Ecological impacts of genetically modified crops: ten years of field research and commercial cultivation. Advances in biochemical engineering/biotechnology. Vol 107, pp. 235-78.
- ↑ Bt-Mais: Sicher für Mensch und Umwelt? Biosicherheit.de 14. Mai 2008
- ↑ Losey, J., Rayor, L., Carter, M. (1999): Transgenic pollen harms monarch larvae. Nature, Vol. 399, S. 214.
- ↑ J. N. Perry, Y. Devos, S. Arpaia, D. Bartsch, A. Gathmann, R. S. Hails, J. Kiss, K. Lheureux, B. Manachini, S. Mestdagh, G. Neemann, F. Ortego, J. Schiemann, J. B. Sweet (2010): A mathematical model of exposure of nontarget Lepidoptera to Bt-maize pollen expressing Cry1Ab within Europe. Proceedings of the Royal Society, online veröffentlicht.
- ↑ Selbst bei flächendeckendem Anbau von Bt-Mais kaum Gefährdung für Schmetterlinge. Biosicherheit.de, 7. Juni 2010.
- ↑ Projektleiter: Prof. Dr. Hans-Hinrich Kaatz: Auswirkungen von BT-Maispollen auf die Honigbiene- Schlussbericht 2004
- ↑ Biosicherheit.de – Honigbiene
- ↑ Langzeit-Studie: Anbau von Bt-Mais ohne Einfluss auf Regenwürmer. Biosicherheit.de, 18. Mai 2010.
- ↑ FAL-Daten zeigen keine Gefahr von Gen-Mais für Bodenmikroorganismen
- ↑ Transgenic DNA discovered in native Mexican corn, according to a new study by UC Berkeley researchers. Press Release, 29. November 2001, UC Berkeley.
- ↑ Dalton, R. (2008): Modified genes spread to local maize. Nature, Vol. 456, published online 12. November 2008
- ↑ Mexiko: Spuren von gentechnisch verändertem Mais bestätigt. Biosicherheit, 11. März 2009
- ↑ Mexico issues first permits to grow GM corn (englisch)
- ↑ a b Mexico's transgenic maize under fire. Nature, Vol. 462, Nr. 404, 2009.
- ↑ Fremdgene in Landsorten: Gefahr für die biologische Vielfalt? 10.Februar 2003.
- ↑ Huang, J., Hu, R., Pray, C., Qiao, F., Rozelle, S. (2003): Biotechnology as an alternative to chemical pesticides: a case study of Bt cotton in China. Agricultural Economics, Vol. 29, pp. 55–68.
- ↑ Bennett, R., Morse, S., Ismael, Y. (2003): Bt cotton, pesticides, labour and health: a case study of smallholder farmers in the Makhathini Flats, Republic of South Africa. Outlook Agriculture, Vol. 32, pp. 123–28.
- ↑ Shahzad Kousera & Matin Qaim: Impact of Bt cotton on pesticide poisoning in smallholder agriculture: A panel data analysis. Ecological Economics 70: 2105–2113.
- ↑ F. Wu: Bt corn's reduction of mycotoxins: regulatory decisions and public opinion. Kapitel 9 In: R. Just, J. Alston, D. Zilberman (hrsg.): Regulating Agricultural Biotechnology: Economics and Policy., New York, Springer, 2006.
- ↑ Singha, M. & P. Bhallaa: Genetic engineering for removing food allergens from plants., In: Trends in Plant Science, Volume 13, Issue 6, 2008, pp. 257-260.
- ↑ Bouis, H. (2007): The potential of genetically modified food crops to improve human nutrition in developing countries. Journal of Developmen Studies. Vol. 43, pp. 79–96.
- ↑ Unnevehr, L., Pray, C., Paarlberg, R. (2007): Addressing micronutrient deficiencies: alternative interventions and technologies. AgBioForum, Vol. 10, pp. 124–34.
- ↑ Stein, A., Sachdev, H., Qaim, M. (2008): Genetic engineering for the poor: Golden Rice and public health in India. World Development, Vol. 36, pp. 144–58.
- ↑ Anderson K., Jackson L,., Nielsen, C. (2005): Genetically modified rice adoption: implications for welfare and poverty alleviation. Journal of Economic Integration, Vol. 20, pp. 771–88.
- ↑ Qaim, M., Stein, A., Meenakshi, J. (2007): Economics of biofortification. Agricultural Econonmics, Vol. 37, pp. 119–33.
- ↑ Stanley Ewen & Arpad Pusztai (1999): Effect of diets containing genetically modified potatoes expressing Galanthus nivalis lectin on rat small intestine. The Lancet 354: 1353-4.
- ↑ Irrtum der Wissenschaftler oder Beweis für Sicherheitslücken. Transgen, 20. Dezember 2002.
- ↑ Goodman, R., Vieths, S., Sampson, H., Hill, D., Ebisawa, M., Taylor, S.,van Ree, R. (2008): Allergenicity assessment of genetically modified crops—what makes sense? Nature Biotechnology, Vol. 26, Nr. 1.
- ↑ a b c Fedoroff, N. & Brown, N. (2004): Mendel in the Kitchen. John Henry Press: Washington, D.C.
- ↑ Gentransfer: Von Pflanze zu Bakterien: 1:100000000000000000000. Transgen. 26. Oktober 2007.
- ↑ Gutachten des Wissenschaftlichen Gremiums für gentechnisch veränderte Organismen über die Verwendung von Antibiotikaresistenzgenen als Markergene in gentechnisch veränderten Pflanzen
- ↑ a b Zimmermann, M. & Porceddu, E. (2005): Agricultural Biotechnology: Concepts, Evolution, and Applications. In: Cooper, J., Lipper, L., Zilberman, D. (eds.): Agricultural Biodiversity and Biotechnology in Economic Development. Springer: New York.
- ↑ Agrobakterien: Natürlicher Austausch von Genen über Artgrenzen
- ↑ Rekombination: Neue Arrangements der Gene
- ↑ Addressing safety concerns (englisch)
- ↑ Pflichtaufgabe: Monitoring
- ↑ 270+ published safety assessments on GM foods and feeds (englisch)
- ↑ Stellungnahme des BVL
- ↑ Schavan – Gentechnik muss sein
- ↑ Verteufeln wir die grüne Gentechnik zu Unrecht?
- ↑ a b c d Paarlberg, R. (2008): Starved for Science: How Biotechnology is Being Kept Out of Africa. Cambridge, MA: Harvard Univ. Press.
- ↑ Thompson, L. (2000): Are Bioengineered Foods Safe? FDA Consumer magazine. January-February, 2000.
- ↑ Thomas J. Hoban (2004):Public Attitudes towards Agricultural Biotechnology. ESA Working Paper No. 04-09. Agricultural and Development Economics Division. FAO.
- ↑ Hallman, W. et al. (2003): Public Perception of Genetically Modified Foods: A National Study of American Knowledge and Opinion. Food Policy Institure, Cook College, Rutgers University.
- ↑ Gaskell, G. et al. (2000): Biotechnology and the European public. Nature Biotechnology, Vol. 18, pp. 935-938.
- ↑ Europäische Kommission. Eurobarometer Spezial- Biotechnologie-Bericht
- ↑ Gaskell et al (2010): Europeans and Biotechnology in 2010. Winds of change? European Union, 2010.
- ↑ Hoban, T. (1998): Trends in Consumer Attitudes about Agricultural Biotechnology. Ag-BioForm. Vol. 1, No. 1, pp. 3-7.
- ↑ Marchant, R. (2001): From the Test Tube to the Table. European Molecular Biology Organization Reports. Vol. 2, No. 5.
- ↑ Miller, H. & Conko, G. (2004): The Frankenfood Myth—How Protest and Politics Threaten the Biotech Revolution. Westport, CT: Praeger.
- ↑ „Kampagnen gegen die Grüne Gentechnik entbehren wissenschaftlicher Grundlage” – Stellungnahme der Union der deutschen Akademien der Wissenschaften
- ↑ Gemeinsame Erklärung der Wissenschaftsorganisationen zur Grünen Gentechnik
- ↑ Für eine neue Politik in der Grünen Gentechnik
- ↑ http://www.oecumene.radiovaticana.org/ted/Articolo.asp?c=443562
- ↑ bll.de: Grundsatzposition der deutschen Lebensmittelwirtschaft zur Grünen Gentechnik
Wikimedia Foundation.